Строение и свойства координационных соединений меди(II) с некоторыми О, N – содержащими лигандами
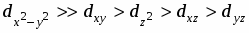
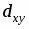
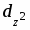
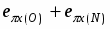
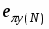
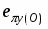
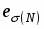
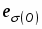
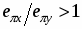
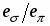
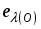
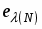
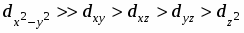
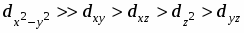
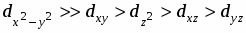
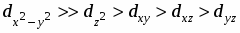
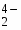
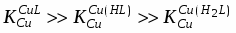
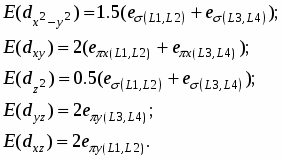
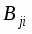
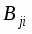
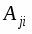
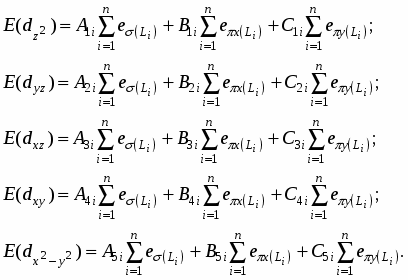 Строение и свойства координационных соединений меди(II) с некоторыми О, N – содержащими лигандами
Строение и свойства координационных соединений меди(II) с некоторыми О, N – содержащими лигандами
Скляр Александр Александрович
Автореферат диссертации на соискание ученой степени кандидата химических наук
Краснодар 2006
Работа выполнена на кафедре общей и неорганической химии Кубанского государственного университета
Общая характеристика работы
Актуальность работы:
Медь является необходимым следовым элементом в теле человека, при этом большинство ионов меди(II) в человеческой плазме крови найдено в форме смешанных комплексов с молекулами аминокислот, пептидов и других органических молекул. Несмотря на то, что изучение комплексообразования меди(II) с биологически активными лигандами является предметом исследования на протяжении нескольких последних десятилетий, ряд аспектов является до конца невыясненным. Это обусловлено, в первую очередь, сложностью рассматриваемых систем, поскольку процессы протекают в многокомпонентных системах, часто с участием молекул – полимеров, имеющих в своем составе большое количество функциональных групп. Одним из способов решения рассматриваемой задачи является моделирование физиологических процессов на примере взаимодействия ионов металлов, обладающих спектральными свойствами, и лигандов, имеющих в своем составе те же функциональные группы, что и рассматриваемый биологический объект.
Большинство органических лигандов, являющихся аналогами природных соединений, способных взаимодействовать с ионами меди, содержат в своем составе кислород- и (или) азот- содержащие группы, за счет которых и возможна координация. При этом координация может осуществляться различными способами, что связано как со строением молекулы лиганда (взаимным расположением донорных групп), так и с влиянием условий протекания реакции комплексообразования.
Наиболее распространенным методом исследования комплексообразования в растворе является метод потенциометрического титрования, который, обладая рядом положительных характеристик, имеет недостаток, связанный с тем, что выбор схемы равновесия делается, как правило, априорно. Напротив, применение спектральных методов, позволяет конкретизировать состав и строение образующихся в растворе комплексов. Однако извлечение химической информации из спектральных данных представляет собой довольно сложную и не всегда выполнимую задачу. Поэтому актуальной является работа по расширению границ использования спектроскопических методов к исследованию комплексных соединений, усовершенствованию способов обработки спектров с помощью современной вычислительной техники.
Диссертационная работа выполнена в соответствии с темой научно-исследовательской работы кафедры общей и неорганической химии Кубанского государственного университета (№ государственной регистрации 01178695675) в соответствии с координационным планом РАН по направлению 2.17. по теме “Координационные соединения и материалы на их основе” и при финансовой поддержке РФФИ (грант 06-03-32881-а).
Цель и задачи работы.
Целью настоящей работы являлась разработка новых теоретических и экспериментальных подходов для изучения комплексообразования меди(II) с органическими соединениями, содержащими в качестве донорных атомы азота и кислорода.
В ходе выполнения исследования решались следующие задачи:
Разработка методик расчета характеристик комплексных соединений в растворе методами потенциометрического титрования и электронной спектроскопии при наличии равновесий различного типа без ограничения количества и состава частиц.
Изучение зависимости состава и свойств комплексов N-фосфонометилглицина с медью(II) от рН.
Изучение строения комплексов меди(II) с 1,2-дигидро-4Н-3,1-бензоксазинами в растворе.
Определение способа координации галактаровой кислоты с медью(II) по данным ИК спектров.
Научная новизна работы:
С помощью разработанных компьютерных программ обработаны полученные экспериментальные данные, что позволило рассчитать характеристики комплексных соединений, определить строение и свойства соединений меди(II) с рядом органических лигандов, содержащих в качестве донорных атомы кислорода и азота.
Практическая значимость работы. Созданные компьютерные программы расчетов и экспериментальные данные диссертационной работы могут быть использованы в научной деятельности, а также при проведении лекционных и семинарских занятий по химии координационных соединений в Кубанском, Казанском, Ростовском, Иркутском и др. университетах.
Апробация работы. Результаты работы представлены на IV международной научно-практической конференции «Компьютерные технологии в науке, производстве, социальных и экономических процессах» (Новочеркасск, 2003), VII Международного семинаре по магнитному резонансу (спектроскопия, томография и экология) (Ростов н/Д, 2004), IV международной науч.-практ. конференции «Моделирование. Теория, методы и средства» (Новочеркасск, 2004), Национальных Конференциях «Информационно-вычислительные технологии в решении фундаментальных научных проблем и прикладных задач химии, биологии, фармацевтики и медицины»: ИВТН-2004 и ИВТН-2005 (Екатеринбург, 2004, 2005), XXII Международной Чугаевской конференции по координационной химии (Кишинев, 2005), XV Российской студенческой научной конференции «проблемы теоретической и экспериментальной химии» (Екатеринбург 2005), IV Всероссийской конференции молодых ученых “Современные проблемы теоретической и экспериментальной химии” (Саратов, 2003).
Публикации. Основное содержание работы нашло отражение в 14 публикациях.
Структура и объем работы. Диссертация состоит из введения, 3 глав, выводов и списка цитируемой литературы (130 наименования). Работа изложена на 115 страницах, включает 14 рисунков и 13 таблиц.
Основное содержание работы
Во введении обоснована актуальность работы, сформулированы цели и задачи исследования.
В первой главе приведен обзор имеющихся литературных данных о спектроскопических методах изучения комплексных соединений, интерпретации экспериментальных спектров ЭПР, электронных и ИК спектров. Проведен анализ методик исследования строения и свойств и расчета параметров комплексных соединений с использованием ЭВМ.
Во второй главе представлены результаты теоретического исследования, в ходе которого разработана методика определения состава, строения и свойств комплексных соединений металлов на основе совместного применении методов потенциометрического титрования и электронных спектров, предложены новые компьютерные программы для: обработки электронных, ЭПР спектров и pH потенциометрических кривых растворов, содержащих ион металла и лиганд(ы), с учетом возможности образования комплексов с различными формами лигандов; предложена методика разделения электронных спектров комплексов на составляющие методом гауссиан анализа и нахождение спектральных характеристик; определения частот и форм нормальных колебаний комплексных соединений по данным ИК спектров.
В программе обработки спектров и pH кривых в блоке расчета мольных долей компонентов системы применяется метод Бринкли, модифицированный для расчета при известной концентрации ионов водорода. Данный метод добавляет ряд контролирующих инструкций к решению системы уравнений по схеме Ньютона-Рафсона, что исключает получение результатов, не имеющих физического смысла. Блок оптимизации искомых параметров включает в себя методы сканирования, координатного и градиентного спуска.
Таким образом, разработанный нами программный комплекс для интерпретации экспериментальных спектров, позволяет автоматически определять константы устойчивости комплексов из спектров ЭПР, электронных спектров и кривых потенциометрического титрования, а также другие параметры ЭПР и электронных спектров.
Для нахождения числа электронных переходов и их характеристик по данным электронных спектров нами создана программа ГАЭС (Гауссиан Анализ Электронных Спектров), позволяющая находить спектральные параметры компонент теоретического спектра, как в ручном так и в автоматическом режиме.
Разработана методика определения строения комплексных соединений из анализа электронного спектра в области d-d-переходов, в основе которого лежит модель углового перекрывания (МУП), выделяющая радиальные параметры, учитывающие степень связывания или разрыхления σ– и π–связей металл-лиганд и угловые множители, зависящие от геометрии молекулы.
Для сложных молекул MLn энергетические уровни находится суммированием возмущений d-орбиталей, вызываемых каждым из лигандов с учетом ориентации этих орбиталей относительно связей металл-лиганд:
(1)
где - , - , - угловые множители, j=1..5 – порядковый номер d-орбитали; i=1..n – порядковый номер лиганда; n-количество лигандов.
При наиболее распространенном октаэдрическом окружении иона металла лигандами угловые координаты лигандов будут иметь значения, приведенные в таблице 1.
Таблица 1.
Угловые координаты лигандов.
Лиганд
Θ
φ
L1
90
0
L2
90
180
L3
90
90
L4
90
270
L5
0
0
L6
180
0
Расчет угловых множителей по данным угловых координат лигандов (таблица 1) приводит выражения для энергии d – орбиталей комплекса (1) к виду:
(2)
Таким образом, приравнивая энергию переходов между d-орбиталями, выраженную через параметры МУП, со значениями этих энергий, найденными из гауссиан анализа экспериментального электронного спектра, получаем систему уравнений для каждого варианта расположения энергетических уровней. Решая полученные уравнения относительно радиальных параметров МУП и анализируя их значения, характерные для координационных соединений, определяется правильный вариант расположения энергетических уровней.
Предложена также методика для расчета частот и форм нормальных колебаний молекул, исходя из данных об их геометрическом строении и силовом поле с использованием решения прямой колебательной задачи путем нахождения собственных значений и собственных векторов в уравнении Шредингера методом приведения к матрице Хессенберга и использованием QR алгоритма с неявными сдвигами. Встроенная в программу база данных по геометрии фрагментов молекул и молярных масс атомов облегчает определение структуры химических соединений, поскольку достаточно изменить одну переменную и тогда все элементы матрицы, содержащей кинетические параметры, использующие ее, пересчитываются автоматически.
В третьей главе приведены результаты экспериментального исследования.
В разделе 3.1 описано изучение бинарных комплексов N-фосфонометилглицина с медью(II) методами потенциометрии и электронной спектроскопии, а также определение влияния аминокислоты (валина) на процесс комплексообразования.
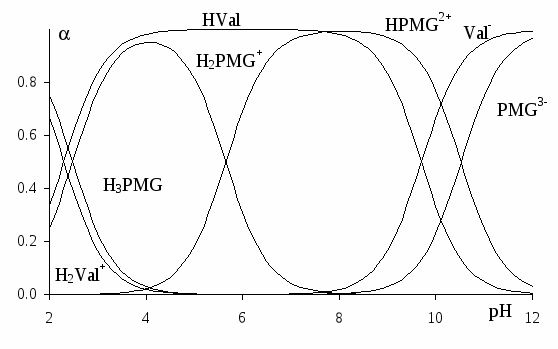
По значениям констант депротонирования лигандов в условиях исследования процессов комплексообразования (температура, ионная сила), определенных нами методом рН метрии, были рассчитаны диаграммы распределения, представленные на рисунке 1.
Рисунок 1. Диаграмма распределения различных форм N-фосфономе-тилглицина и валина.
В системе Cu2+-H3PMG константы устойчивости комплексов убывают в ряду , что в первом случае соответствует переходу от тридентатного связывания с образованием двух пятичленных хелатных колец к бидентатному с восьмичленным циклом, а во втором – объясняется стерическими затруднениями при образовании связи с двукратно протонированной фосфоновой группой.
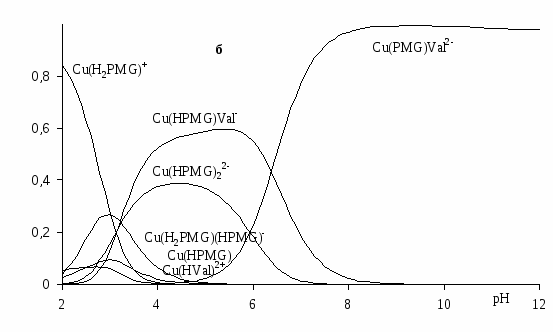
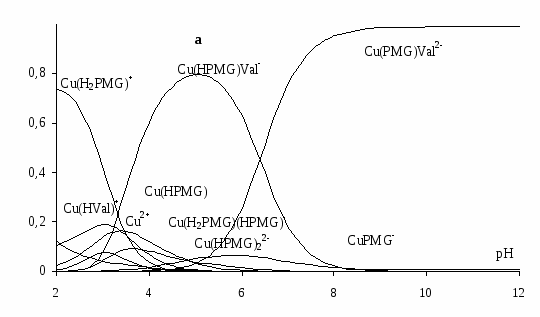
Для тройных систем Cu2+-H3PMG-HVal нами были получены значения констант устойчивости разнолигандных комплексов Cu(PMG)Val2- (lgβ1110 = 19.81(4)) и Cu(HPMG)Val- (lgβ1111 = 26.02(6)) и рассчитаны диаграммы распределения иона металла (рисунок 2). Образованию комплексов Cu(H2PMG)(HVal)+, Cu(HPMG)(HVal), Cu(HPMG)Val, Cu(PMG)Val2, по всей видимости, препятствует большая устойчивость при низких значениях рН бис-комплексов с формами HPMG2- и H2PMG-, способными образовывать хелатные комплексы.
Большую устойчивость комплекса Cu(PMG)Val2 по сравнению с Cu(PMG) можно объяснить вхождением в координационную сферу иона металла меньшего по объему по сравнению с PMG3- хелатообразующего валинат-иона, также занимающего два места в экваториальной плоскости комплекса. По сравнению с Cu(Val)2 тройной комплекс устойчив за счет тридентатного характера связывания глифосат-аниона.
Рисунок. 2. Диаграммы распределения металла для растворов с соотношениями сCu: сPMG : сVal = 1:1:1 (а) и 1:2:2 (б) (сCu=0.0015 моль/л, 0.1 М KCl).
В электронных спектрах в системе Cu2+-H3PMG при увеличении рН и соотношения сPMG: сCu возрастает оптическая плотность, максимум полосы поглощения смещается в длинноволновую область не превышая значения 14500 см-1, что означает присутствие не более одного атома азота в экваториальной плоскости комплекса, то есть в комплексе Cu(PMG) одна из донорных групп не принимает участия в связывании и один из лигандов координирован бидентатно. Об этом также свидетельствует его константа устойчивости, которая намного ниже ожидаемой при одинаковой координации обоих лигандов.
Добавление в систему валина смещает сигнал в длинноволновую область и при рН > 8 максимум полосы поглощения имеет значение свыше 14500 см-1, что подтверждает нахождение в экваториальной плоскости комплекса двух донорных атомов азота.
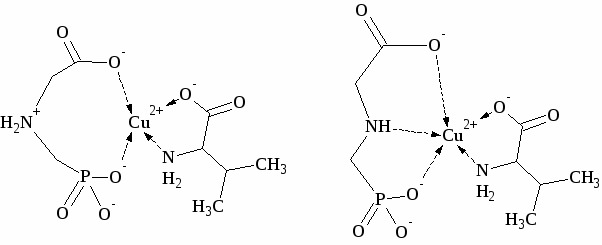
Значения констант устойчивости, полученные в ходе компьютерной обработки оптических спектров, соответствуют данным рН метрического титрования, что свидетельствует о корректности выбранной схемы равновесий. Нами предложены следующие способы координации в разнолигандных комплексах:
Cu(HPMG)Val Cu(PMG)Val2–
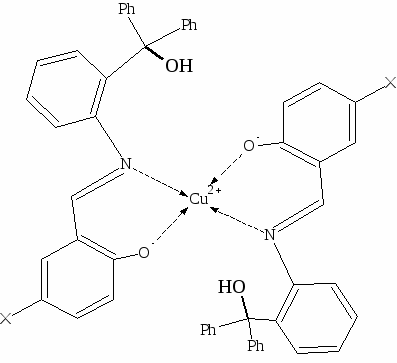
В разделе 3.2 описано исследование строения комплексов Cu(II) с 2-[2-гидроксифенил]-4,4-дифенил-1,2-дигидро-4Н-3,1-бензоксазином (I) и 2-[2-гидрокси-5-нитрофенил]-4,4-дифенил-1,2-дигидро-4Н-3,1-бензоксазином (II) методами ЭПР и электронной спектроскопии.
По данным ИК спектров установлено, что в реакции комплексообразования участвует именно азометиновая форма лигандов. Данные ЭПР (наличие дополнительной сверхтонкой структуры от двух ядер азота) позволяют предположить следующее строение координационного центра:
(Х = H (I); NO2 (II)).
Разложение электронного спектра на Гауссовы составляющие с помощью программы ГАЭС позволяет выделить четыре компоненты, параметры которых приведены в таблице 2, соответствующие d-d переходам.
Приравнивая, полученные в рамках МУП, выражения для энергии переходов между d-орбиталями со значениями ν0 из таблицы 2, получаем системы уравнений для четырех возможных вариантов расположения энергетических уровней:
1) ;
2) ;
3) ;
4) .
Таблица 2.
Параметры полос поглощения отдельных электронных переходов в комплексах меди(II) c соединениями I и II.
№ перехода
, дм3∙моль-1∙см-1
ν0, см-1
δ½, см-1
f, 10-4
I
1
20
14047
1910
10.57
2
39
15422
1078
11.63
3
29
17111
1000
8.023
4
27
19033
1133
8.463
II
1
12
14122
2100
6.972
2
39
15820
1284
13.85
3
23
17928
1036
6.592
4
18
19581
1022
5.089
Значения параметров МУП найдены нами решением полученных систем уравнений и приведены в таблице 3.
Анализ рассчитанных значений параметров МУП позволяет считать вариант (2) более предпочтительным, так как для него выполняется ряд соотношений: > (где =, ), поскольку атом азота образует более прочные ковалентные связи; ≈ 3-5 для всех донорных атомов и , характерно для координационных связей меди(II) с N- и O-содержащими донорными группами.
Таблица 3.
Параметры МУП комплексных соединений, рассчитанные по электронным спектрам.
Вариант
Параметры
Cu(II) + I
Cu(II) + II
(1)
(2)
(3)
(4)
(1)
(2)
(3)
(4)
7100
7100
7100
7100
7100
7100
7100
7100
6947
8322
10011
11933
7022
8720
10828
12481
1979.8
3011
3317
5719
1628
2901
3656
5722
1018.8
2050
5122
6564
801
2074.5
5536
6776
2824.3
4543
5810
7251
2681.5
4804
6385
7625
Так как энергия -орбитали может быть меньше энергии -орбитали лишь в случае отсутствия координации в аксиальных положениях, то можно считать, что данные электронной спектроскопии свидетельствуют о неучастии в координации атомов кислорода трифенилкарбинола в растворе и подтверждают предложенную выше структуру.
Таким образом, данные электронных спектров подтверждают структуру комплекса, предложенную выше.
Раздел 3.3 посвящен определению структуры комплекса меди(II) состава Cu(НGala)24H2O методом ИК спектроскопии.
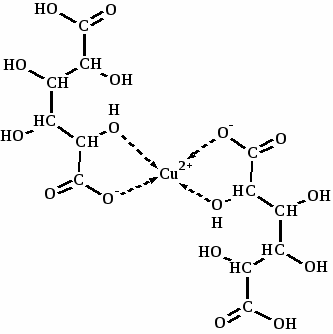
Произведенный нами эмпирический анализ и сравнение ИК спектров галактаровой кислоты (ГК) и галактарата меди(II) показал, что при комплексобразовании происходит разрыв водородных связей свободной кислоты, и взаимодействие спиртовых групп (νОНспирт) ГК с ионом металла, причем только одна из карбоксильных групп ГК связывается с ионом меди(II), а другая – остается связанной водородной связью с карбоксильной группой ГК молекулы соседнего комплекса.
Расщепление полосы поглощения, принадлежащей валентным колебаниям карбонильной группы ГК, в спектре комплекса на две полосы поглощения 1618 и 1385 см-1, соответствующие антисимметричным и симметричным валентным колебанием депротонированной карбоксильной группы (νasCOO־ и νsCOO־, соответственно) ГК. Значение ΔνCOO־ равное 233 см-1 и присутствие в ИК спектре галактарата меди полосы средней интенсивности в области 1729 см-1 свидетельствует о монодентатной координации карбоксильной группы с ионом меди(II).
Понижение частот валентных колебаний связей С-О спиртовых групп (νС-Оспирт) в спектре комплекса на ~20 см-1 свидетельствует о взаимодействии спиртовых групп ГК с ионом меди(II), что приводит к изменению системы водородных связей.
На основании вышеизложенного нами предложена следующая структура соединения:
,
исходя из которой, было проведено сравнение рассчитанных и экспериментальных данных (таблица 4).
Используемая нами методика пофрагментного расчета частот и форм нормальных колебаний сложных молекул предполагает предварительный расчет отдельных фрагментов участвующих в комплексообразовании, в частности лиганда, с уточнением исходных значений силовых постоянных в ходе расчета.
Таблица 4.
Экспериментальные и рассчитанные значения частот полос поглощения H2Gala и Cu(HGala)2∙4H2O (см-1).
H2Gala
Cu(HGala)2∙4H2O
Отнесение
Эксперимент
Расчет
Эксперимент
Расчет
3422пл, 3280ш
3570, 3455
3577, 3477пл, 3304, 3160пл
3570, 3400
νOHспирт
2968, 2921, 2870
2962, 2855
2969, 2923, 2857
2962, 2855
νCH
2656, 2560
3577, 3477
2656, 2559пл
-
νOHкарб
1729
1729
1729
-
νC=O
-
-
1619
1619
νasCOO¯
1455
1460
1452
1459
δCCH
1422
1412
1422пл
1424
δCОНспирт + δCОНкарб
1375
1376
1365пл
1376
δCCH
-
-
1385
1375
νsCOO¯
1310пл, 1296, 1261пл
1310, 1300, 1257
1310, 1298, 1262
1309, 1298, 1255
δCCH + δCОНспирт
1240, 1212,
1240, 1211
1241, 1211
1240, 1211
νC-С,
1123, 1062
1117, 1052пл, 1047
νC-Oспирт
966
988
τCСОНкарб
919
920
-
τCООН
862, 830, 801, 720пл, 700, 668, 633, 510, 465, 376, 283, 249, 242пл, 208, 179 пл, 139, 116, 74
879, 845, 802, 720пл, 698, 667, 634, 509, 467, 401, 373пл, 281, 236ш, 208, 179, 140, 119пл, 76
Скелетные колебания (δCCС + τОССС + τОССО + τСССС + δОСО и т.п.)
-
-
554, 442
607, 410
νCu-O
-
-
330, 152, 125,
334, 155, 128
δ(Cu-лиганд)
Хорошее соответствие результатов расчета экспериментальным данным подтверждает предложенную нами выше структуру координационного окружения иона металла.
Выводы
Разработана методика определения строения и свойств комплексных соединений меди(II) путем совместного применении методов потенциометрического титрования и обработки электронных спектров, показана возможность ее использования для сложных систем, содержащих как бинарные, так и разнолигандные комплексные соединения.
При исследовании систем медь(II) – N-фосфонометилглицин – валин методами потенциометрического титрования и электронной спектроскопии определены значения констант устойчивости разнолигандных комплексов: Cu(PMG)Val2– и Cu(HPMG)Val–. Обнаружено, что образованию соединений Cu(H2PMG)(HVal)+ и Cu(HPMG)(HVal) препятствует большая устойчивость при низких рН бискомплексов с HPMG2 и H2PMG, способными образовывать хелатные комплексы, в отличие от нейтральной формы валина. Большая устойчивость комплекса Cu(PMG)Val2– по отношению к Cu(PMG)24– может быть объяснена вхождением в координационную сферу иона металла хелатообразующего валинат-иона, занимающего два места в экваториальной плоскости комплекса.Тройной комплекс устойчив за счет тридентатного характера связывания глифосат-аниона.
По данным электронных спектров в комплексе CuPMG24 одна из донорных групп не принимает участие в связывании, а один из лигандов координирован бидентатно. В системе медь(II) N-фосфонометилглицин аминокислота возможно образование разнолигандных комплексов, имеющих высокую устойчивость, что необходим учитывать при моделировании процессов, протекающих в биологических системах с участием иона металла и глифосата.
Установлено, что в комплексообразовании меди(II) с 2-[2-гидроксифенил]-4,4-дифенил-1,2-дигидро-4Н-3,1-бензоксазином и 2-[2-гидрокси-5-нитрофенил]-4,4-дифенил-1,2-дигидро-4Н-3,1-бензоксазином участвуют азометиновые формы лигандов, при этом образуются соединения CuL2 с координацией по фенольной и азометиновой группам обоих лигандов. Методом разложения электронных спектров на Гауссовы составляющие определены энергии d-d переходов, проведен расчет параметров взаимодействия в рамках модели углового перекрывания и установлен порядок расположения орбиталей центрального атома по энергиям: .
На основании эмпирического отнесения полос поглощения в ИК спектре соединения Cu(HGala)2·4H2O определено строение координационного узла. Пофрагментным расчетом частот и форм нормальных колебаний для галактаровой кислоты и комплексного соединения с медью(II) подтверждено участие α-гидроксильной и карбоксильной групп галактаровой кислоты в координации иона меди(II), определены силовые постоянные связей металл-лиганд. Показано, что расчет колебательного спектра исследуемых соединений для фрагмента молекулы может заменить расчет полной структуры молекулы.
Результаты диссертационной работы изложены в следующих публикациях:
Болотин С.Н., Заплатина Н.П., Скляр А.А., Панюшкин В.Т. Компьютерный анализ спектров ЭПР сложных равновесных систем // Мат. IV международной научно-практической конференции «Компьютерные технологии в науке, производстве, социальных и экономических процессах». Новочеркасск: ЮРГТУ, 2003. Ч. 3 С. 13.
Болотин С.Н., Скляр А.А., Панюшкин В.Т. Компьютерный анализ спектров ЭПР жидких растворов при наличии сложных равновесий // Тезисы докладов VII Международного семинара по магнитному резонансу (спектроскопия, томография и экология). Ростов-на-Дону, 2004. С. 132-133.
Болотин С.Н., Скляр А.А., Трудникова Н.М. Математическое моделирование химических равновесий по данным оптической спектроскопии // Мат. IV международной науч.-практ. конференции «Моделирование. Теория, методы и средства». Новочеркасск: ЮРГТУ, 2004. Ч. 2. С. 47-48.
Болотин С.Н., Панюшкин В.Т., Николаенко И.А., Скляр А.А. Комплексообразование меди(II) с L-гистидином в водном растворе по данным спектров ЭПР // Журнал неорганической химии. 2004. Т. 49. №. 11. С. 1838-1842.
Скляр А.А., Болотин С.Н., Трудникова Н.С. Колечко Д.В. Программа обработки спектральных данных комплексов переходных металлов // Сборник тезисов докладов «Информационно-вычислительные технологии в решении фундаментальных научных проблем и прикладных задач химии, биологии, фармацевтики и медицины (ИВТН-2004)». М.: Открытые системы, 2004. С. 34.
Скляр А.А., Болотин С.Н., Апенышева Т.Е., Пушкарева К.С., Буков Н.Н. Определение энергий взаимодействия металл - лиганд комплексов меди(II) с производными дигидробензаксазина методом анализа электронных спектров поглощения // Сборник тезисов докладов «Информационно-вычислительные технологии в решении фундаментальных научных проблем и прикладных задач химии, биологии, фармацевтики и медицины (ИВТН-2005)». – М.: Открытые системы, 2005. С. 58.
Скляр А.А., Апенышева Т.Е., Болотин С.Н., Колоколов Ф.А., Пушкарева К.С., Буков Н.Н. Геометрия комплексного соединения меди(II) с 2-[2-гидрокси-5-нитрофенил]-4,4-дифенил-1,2-дигидро-4Н-3,1-бензоксазином в растворе хлороформа // Тезисы докладов XXII Международной Чугаевской конференции по координационной химии 2005. С. 495-496.
Панкова О.С., Трудникова Н.М., Скляр А.А., Болотин С.Н. Спектрофотометрическое исследование разнолигандных комплексов меди(II) c серином, валином и аспарагиновой кислотой // Тезисы докладов XV Российской студенческой научной конференции «проблемы теоретической и экспериментальной химии». Екатеринбург 2005. С. 170.
Пащевская Н.В., Болотин С.Н. Скляр А.А., Трудникова Н.М., Буков Н.Н., Панюшкин В.Т. Исследование комплексообразования в системе медь(II) N-фосфонометилглицин валин. // Журнал неорганической химии. 2005. Т. 50. № 12. С. 2107 – 2112.
Скляр А.А., Болотин С.Н., Панюшкин В.Т. Программа для расчета спектральных характеристик и содержания комплексных соединений в растворе по данным ЭПР и электронных спектров. Свидетельство об официальной регистрации программы для ЭВМ №2005610034.
Скляр А.А., Болотин С.Н.. Программа гауссиан анализа электронных спектров (ГАЭС). Свидетельство об официальной регистрации программы для ЭВМ №2005611573.
Paschevskaya N.V., Bolotin S.N., Sklyar A.A., Trudnikova N.M., Bukov N.N., Panyushkin V.T. Binary and ternary complexes of copper(II) with N-phosphonomethylglycine and valine // Journal of Molecular Liquids. 2006. V. 126. N 1-3, P. 89-94.
Апенышева Т.Е., Буков Н.Н., Скляр А.А., Болотин С.Н., Пушкарева К.С. Строение комплексных соединений меди(II) с производными дигидробензоксазина в растворе хлороформа // Координационная химия. 2006. Т. 32. №6. С. 350 – 353.
Скляр А.А., Колоколов Ф.А., Болотин С.Н. Программа для расчета частот и форм нормальных колебаний сложных молекул. Свидетельство об официальной регистрации программы для ЭВМ №2006610413.

Нравится материал? Поддержи автора!
Ещё документы из категории география:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ