Ненасыщенные альдегиды и кетоны
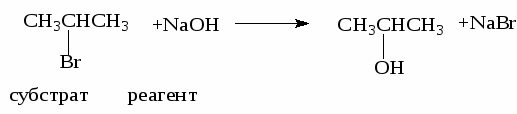
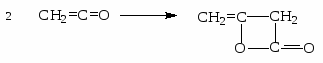
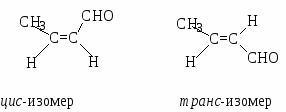
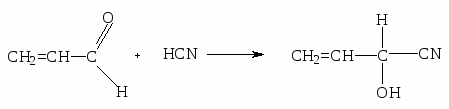
 Ненасыщенные альдегиды и кетоны
Ненасыщенные альдегиды и кетоны
Ненасыщенные альдегиды и кетоны, в зависимости от взаимного расположения двойной и карбонильной групп в молекуле, могут быть поделены на три группы: с сопряженными (CH=CH2-COCH3 - метилвинилкетон, бутен-1-3-он; CH2=CHCHO - акролеин, пропеналь), кумулированными (кетены CH2=C=O) и изолированными (CH2=CHCH2CH2CH2COCH3) связями. Из них наибольший интерес представляют соединения с сопряженными связями, особенно - акролеин и кротоновый альдегид
Для некоторых ненасыщенных альдегидов и кетонов сохранились эмпирические (акролеин) или рациональные (метилвинилкетон) названия. По номенклатуре IUPAC положение двойной связи и карбонильной группы указывают цифрами.
Важнейшими представителями ненасыщенных альдегидов являются акролеин CH2=CH-CHO и кротоновый альдегид CH3-CH=CH-CHO.
Существует несколько способов получения акролеина:
Альдольная конденсация формальдегида с ацетальдегидом
CH2=O + CH3-CHO CH2OH-CH2-CHO
оксипропионовый альдегид
Оксипропионовый альдегид далее подвергается дегидратации:
CH2OH-CH2-CHO CH2=CH-CHO + H2O
Прямое каталитическое окисление пропилена
CH2=CH-CH3 + O2 CH2=CH-CHO + H2O
Дегидратация глицерина
CH2OH-CHOH-CH2OH CH2OH-CH=CHOH CH2OH-CH2-CH=O CH2=CH-CHO
Акролеин используется для получения пластмасс, отличающихся большой твердостью. При конденсации акролеина с пентаэритритом получают полимеры, по внешнему виду напоминающие стекло. Акролеин используют в качестве исходного вещества для синтеза глицерина.
Кротоновый альдегид получают кротоновой конденсацией ацетальдегида (см. Лекция №24). Применяется для получения масляного альдегида, бутанола, масляной кислоты, а также малеинового ангидрида.
Химические свойства
Акролеину, кротоновому альдегиду и другим непредельным соединениям с сопряженной двойной и карбонильными связями присущи реакции, свойственные алкенам и альдегидам. Взаимное влияние двойной связи и карбонильной группы находит отражение в некоторых особенностях, например:
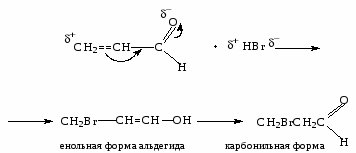
1. Порядок присоединения HBr не соответствует правилу Марковникова
2. Синильная кислота присоединяется к акролеину по карбонильной группе:
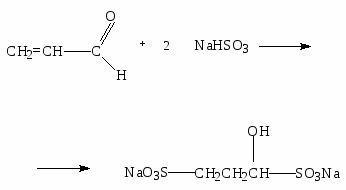
3. Гидросульфит натрия присоединяется не только по карбонильной группе, но и по двойной связи:
Метилвинилкетон - простейший представитель ненасыщенных кетонов. Существует в виде двух изомеров:
Метилвинилкетон получают преимущественно двумя способами:
Гидратация винилацетилена.
HCC-CH=CH2 + H2O CH3COCH=CH2
Конденсация формальдегида с ацетоном:
H2C=O + CH3COCH3 HOCH2CH2COCH3 CH2=CHCOCH3
Метилвинилкетон проявляет свойства как кетона, так и алкенов. Легко полимеризуется в прозрачную бесцветную стекловидную массу, используемую в производстве пластмасс.
Кетенами называются соединения, содержащие группу >C=C=O. По строению они напоминают непредельные кетоны. Простейший кетен CH2=C=O может быть получен из бромангидрида бромуксусной кислоты под действием цинковой пыли:
CH2BrCOBr + Zn CH2=C=O + ZnBr2
В промышленности кетен получают пиролизом ацетона
CH3COCH3 CH2=C=O + CH4
и дегидратацией уксусной кислоты в присутствии катализаторов кислотного типа:
CH3COOH CH2=C=O + H2O
CH3COOH + H+ CH3COO+H2 CH3C+=O CH2=C=O + H+
Кетены чрезвычайно легко реагируют с водой:
CH2=C=O + H2O CH3COOH
карбоновыми кислотами:
CH2=C=O + CH3COOH (CH3CO)2O.
Спиртами:
CH2=C=O + CH3CH2OH CH3COOCH2CH3.
Аминами:
CH2=C=O + CH3NH2 CH3CONHCH3 + H2O.
В промышленности из кетена получают уксусную кислоту, уксусный ангидрид, этилацетат, дикетен и другие вещества, являющиеся полупродуктами в производстве красителей и лекарственных веществ.
Кетен легко полимеризуется с образованием дикетена:
.
Дикетен реагирует с водой, спиртами, аминами:
CH2=COCH2CO + H2O CH3COCH2COOH.
Ароматические альдегиды и кетоны
Ароматические альдегиды и кетоны характеризуются наличием карбонильной группы, связанной с углеродом бензольного ядра или боковой цепи. Альдегиды с карбонильной группой первого типа называются по соответствующим ароматическим кислотам, а с карбонильной группой в боковой цепи – как арилзамещенные альдегиды жирного ряда.
Кетоны бывают чисто ароматические (дифенилкетон или бензофенон) и жирноароматическими (метилфенилкетон или ацетофенон).
Способы получения ароматических альдегидов
Многие ароматические альдегиды могут быть получены способам, описанными для альдегидов жирного ряда (Лекция№23): окисление первичных спиртов, сухая перегонка кальциевых солей ароматической и муравьиной кислот, синтезы с участием реактивов Гриньяра и др.
Окисление ароматических углеводородов.
Важный способ синтеза ароматических альдегидов (в частности, бензальдегида) – окисление углеводородов кислородом воздуха на катализаторе (V2O5, MnO2):
C6H5-CH3 C6H5-CHO
Способ имеет как лабораторное, так и промышленное значение.
Формилирование ароматических углеводородов.
Для ароматического ряда известны реакции прямого введения альдегидной группы, не имеющие аналогий в жирном ряду (реакция Гаттермана-Коха):
C6H5CH3 + HCl+CO CH3-C6H4-CHO
Реакция катализируется хлоридами меди и алюминия. Предполагается, что в качестве промежуточного продукта образуется хлористый формил HCOCl, не существующий в свободном виде. Бензол в эту реакцию вступает очень плохо, его гомологи дают хорошие выходы (50-60%).
Гидролиз гем-дигалогенпроизводных.
Существует способ получения бензальдегида через хлористый бензилиден C6H5CHCl2:
C6H5CH3 + Cl2 C6H5CHCl2 + H2O C6H5CHO + 2 HCl
толуол хлористый бензилиден бензальдегид
Гидролиз проводится в присутствии катализатора (Fe).
Способы получения ароматических кетонов
Для получения ароматических кетонов применимы многие методы получения кетонов жирного ряда (окисление вторичных спиртов, перегонка кальциевых солей ароматической и какой-либо другой кислоты, кроме муравьиной - см. Лекцию №23).
Реакция Фриделя-Крафтса. В качестве исходных веществ могут использоваться ароматические углеводороды, эфиры фенолов:
C6H6 + Cl-CO-C6H5 C6H5-CO-C6H5 + HCl
хлористый бензоил бензофенон
Реакция катализируется хлористым алюминием.
Химические свойства ароматических альдегидов
Ароматические альдегиды вступают в большинство реакций, свойственных альдегидам жирного ряда. Специфическими реакциями ароматических альдегидов являются следующие:
Реакция Канниццаро.
В присутствии водного или спиртового раствора щелочи (50%) ароматические альдегиды могут диспропорционировать, образуя соответствующий спирт и соль кислоты (реакция Канниццаро):
2 C6H5CHO + KOH C6H5COOK + C6H5CH2OH
бензальдегид бензоат калия бензиловый спирт
Большинство альдегидов жирного ряда в условиях реакции Канниццаро подвергаются осмолению, однако, если в альдегиде отсутствует атом водорода в -положении, то реакция протекает вполне гладко. Механизм реакции следующий:
Бензоиновая конденсация. Под действием цианид-иона две молекулы ароматического альдегида могут конденсироваться с образованием -оксикетона. Поскольку простейшее соединение, образующееся при конденсации бензальдегида, называется бензоином, эта последовательность реакций получила название бензоиновой конденсации:
Реакционная способность ароматических альдегидов и кетонов зависит от заместителей в ароматическом ядре. Так, наличие электроноакцепторных групп (NO2-) повышает реакционную способность по карбонильной группе. Большое значение имеет также пространственный фактор: заместитель (трет-С4H9-, SO3H-) в орто-положении ароматического ядра снижает реакционную способность.
Большинство ароматических кетонов реагируют с гидроксиламином и производными гидразина по обычной схеме:
(Ar)2C=O + NH2OH (Ar)2C=NOH + H2O
кетоксим
(Ar)2C=O + NH2-NH-C6H5 (Ar)2C=N-NH-C6H5 + H2O
фенилгидразон
Из всех азотистых производных кетонов наибольший интерес представляют оксимы. Оксимы чисто ароматических несимметричных кетонов существуют в виде двух геометрических изомерных форм, син- и анти-:
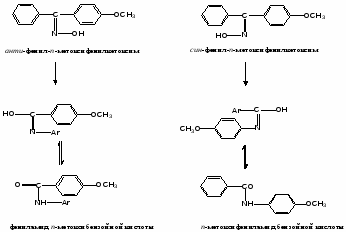
Из всех азотистых производных кетонов наибольший интерес представляют оксимы. Оксимы чисто ароматических несимметричных кетонов существуют в виде двух геометрических изомерных форм, син- и анти-. Син-формой принято считать изомер, содержащий меньший радикал в цис-положении с гидроксильной группой оксима. Более стойкой является анти-форма. Она получается из син-формы под действием кислот. Аналогичное явление известно и для оксимов ароматических альдегидов:
Оксимы жирноароматических кетонов обычно существуют в виде одной более стойкой формы. Важным свойством оксимов является их способность подвергаться перегруппировке Бекмана: под действием ангидридов и хлорангидридов кислот два изомерных оксима дают два изомерных амида:
перегруппировка Бекмана используется для получения - и -аминокислот.
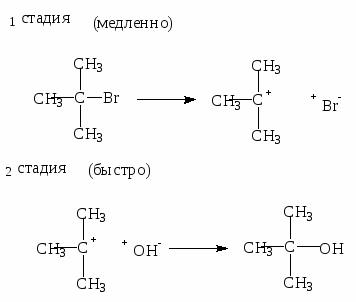
Реакция замещения галогена на ОН-группу протекает по механизму нуклеофильного замещения SN. В зависимости от строения субстрата замещение протекает по SN1 (мономолекулярное замещение):
(
C
H
3
)
3
C
O
H
+ HX
(
C
H
3
)
3
C
O
H
H
-
H
2
O
(
C
H
3
)
3
C
O
H
H
(
C
H
3
)
3
C
O
H
H
X
-
(
C
H
3
)
3
C
X
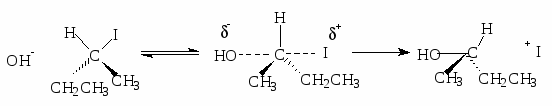
или SN2 (бимолекулярное):
C
H
3
C
H
2
O
H
+ HBr
C
H
H
C
H
3
O
H
B
r
-
C
C
H
3
H
H
O
H
B
r
C
H
3
C
H
2
B
r
+
H
2
O
-
+
Атакующий агент – анионы (SH -, OН -, I -, Br -, С l -, F -, RO -, CH3COO -, ONO2-) или молекула (ROH, HOH, NH3, RNH2). По увеличению реакционной способности анионы располагаются в следующий ряд:
HS -, RS - > I - > Br - > RO - > Cl - > CH3COO - > ONO2-
Анионы более сильные нуклеофилы, чем сопряженные кислоты:
OH - > HOH, RS - > RSH, RO - > ROH, Cl - >HCl
Нуклеофил – атом (или частица), который может отдать пару электронов любому элементу, кроме водорода. Механизм бимолекулярного нуклеофильного замещения (SN2) включает образование промежуточного комплекса.
Представленная реакция является реакцией замещения, так как нуклеофил (ОН -) вытесняет уходящую группу (I-).
Механизм мономолекулярного нуклеофильного замещения (SN1) состоит из двух стадий:
Реакции замещения по механизму SN1 в тех случаях, когда образуется стабильный катион. Первичные галогеналканы реагируют по механизму SN2 , а третичные - по механизму SN1.

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ