Плотность жидкости при нормальной температуре кипения
 Плотность жидкости при нормальной температуре кипения
Плотность жидкости при нормальной температуре кипения
Аддитивный метод Шредера
При изучении свойств органических жидкостей Шредером было сформулировано правило, в соответствии с которым при прогнозировании мольного объема чистой жидкости при нормальной температуре кипения следует сосчитать число атомов углерода, водорода, кислорода и азота в молекуле, добавить по единице на каждую двойную связь и сумму умножить на семь. При этом получаем мольный объем жидкости в см3/моль. Правило Шредера дает удивительно хорошие результаты для нормальных жидкостей - погрешность, как правило, не превышает 3-4% тон. Плотности сильно ассоциированных жидкостей прогнозируются с меньшей точностью. В дальнейшем аддитивный метод Шредера модифицировался самим автором и другими учеными. В табл. 6.5 приведены значения групповых вкладов в последней редакции Шредера и Ле Ба.
Таблица 6.5
Аддитивные составляющие для расчета молярных объемов Vb
органических веществ
Тип атома, группы, связи
Составляющая, см3/моль
Шредер
Ле Ба
Углерод
7
14,8
Водород
7
3,7
Кислород (за исключением приведенных ниже случаев):
7
7,4
в метиловых сложных и простых эфирах
–
9,1
в этиловых сложных и простых эфирах
–
9,9
в высших сложных и простых эфирах
–
11,0
в кислотах
–
12,0
Тип атома, группы, связи
Составляющая, см3/моль
Шредер
Ле Ба
соединенный с S, P, N
–
8,3
Азот:
7
–
с двойной связью
–
15,6
в первичных аминах
–
10,5
во вторичных аминах
–
12,0
Бром
31,5
27
Хлор
24,5
24,6
Фтор
10,5
8,7
Иод
38,5
37
Сера
21
25,6
Кольцо:
–
трехчленное
-7
-6,0
четырехчленное
-7
-8,5
пятичленное
-7
-11,5
шестичленное
-7
-15,0
нафталиновое
-7
-30,0
антраценовое
-7
-47,5
Двойная связь между атомами углерода
7
–
Тройная связь между атомами углерода
14
–
Неаддитивный метод Тина и Каллуса
Величина мольного объема жидкости при нормальной температуре кипения представлена в качестве функции критического объема:
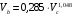 ,(6.13)
,(6.13)
где 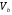 и
и 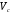 выражены в см3/моль.
выражены в см3/моль.
Это простое соотношение хорошо прогнозирует 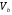 для органических чистых жидкостей, погрешность не превышает 3% отн. при условии, что значения критического объема определены надежно.
для органических чистых жидкостей, погрешность не превышает 3% отн. при условии, что значения критического объема определены надежно.
Рассмотренные выше методы Шредера и Тина-Каллуса не распространяются на всю область насыщенных состояний жидкости. Они приложимы к одной точке в этой области - нормальной температуре кипения. Прогнозирование плотности насыщенной жидкости при любой температуре ниже  может быть выполнено на основе некоторых уравнений состояния вещества, так, например, уравнения Бенедикта-Уэбба-Рубина для углеводородов. Однако целесообразнее использовать для этого специальные эмпирические корреляции, которые относительно просты и в большинстве случаев более точны.
может быть выполнено на основе некоторых уравнений состояния вещества, так, например, уравнения Бенедикта-Уэбба-Рубина для углеводородов. Однако целесообразнее использовать для этого специальные эмпирические корреляции, которые относительно просты и в большинстве случаев более точны.
Практически все корреляционные методы основаны на принципе соответственных состояний и требуют знания плотности насыщенной жидкости хотя бы при одной температуре. Поскольку даже такой минимум информации не всегда доступен, приходится прибегать к оценкам критической плотности вещества по его критическому объему. При отсутствии экспериментальных данных вычисление плотности может быть основано на коэффициенте сжимаемости жидкости при давлении насыщения, что рационально выполнять с использованием таблиц Ли-Кеслера (разд. 4). Ниже рассмотрены оба подхода.
Метод Ганна-Ямады
Метод предназначен для прогнозирования молярного объема 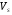 и плотности неполярных или слабополярных жидкостей
и плотности неполярных или слабополярных жидкостей 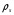 только на линии насыщения. Он основан на принципе соответственных состояний. Для прогнозирования необходимо как минимум знать ацентрический фактор и критические температуру и давление. Предложенная авторами корреляция имеет вид
только на линии насыщения. Он основан на принципе соответственных состояний. Для прогнозирования необходимо как минимум знать ацентрический фактор и критические температуру и давление. Предложенная авторами корреляция имеет вид
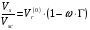 ,(6.14)
,(6.14)
где 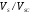 - безразмерный параметр,
- безразмерный параметр, 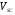 - масштабирующий параметр,
- масштабирующий параметр, 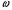 - ацентрический фактор.
- ацентрический фактор. 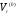 и
и 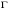 являются функциями приведенной температуры. Для расчета
являются функциями приведенной температуры. Для расчета 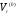 рекомендованы корреляции двух видов:
рекомендованы корреляции двух видов:
при 
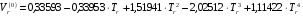 ;(6.15)
;(6.15)
при 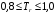
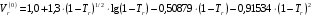 .(6.16)
.(6.16)
Расчет значения 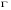 производится по одному уравнению для любой температуры в диапазоне
производится по одному уравнению для любой температуры в диапазоне 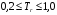 :
:
 .(6.17)
.(6.17)
При расчете масштабирующего параметра рекомендованы следующие подходы.
Если известен молярный объем насыщенной жидкости 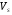 или ее плотность при приведенной температуре
или ее плотность при приведенной температуре 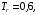 то расчет
то расчет 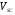 построен на основе этих сведений:
построен на основе этих сведений:
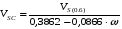 .(6.18)
.(6.18)
Если экспериментальные данные для 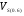 отсутствуют, то расчет масштабирующего параметра выполняется по уравнению
отсутствуют, то расчет масштабирующего параметра выполняется по уравнению
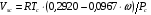 .(6.19)
.(6.19)
В большинстве случаев масштабирующий параметр близок по значению к критическому объему 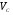 .
.
При наличии экспериментальных сведений о плотности интересующей насыщенной жидкости при некоторой температуре 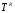 масштабирующий параметр
масштабирующий параметр 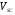 может быть исключен из расчета, и задача сводится к решению уравнения
может быть исключен из расчета, и задача сводится к решению уравнения
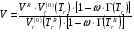 ,(6.20)
,(6.20)
где 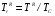 , а их участие в уравнении следует понимать как температурный уровень, при котором вычисляются
, а их участие в уравнении следует понимать как температурный уровень, при котором вычисляются 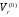 и
и  , а не как сомножители.
, а не как сомножители.
Метод Ганна-Ямады считается наиболее точным из имеющихся в настоящее время методов прогнозирования плотности насыщенной жидкости при Tr < 0,99. Несмотря на то, что он рекомендован авторами для неполярных или слабо полярных веществ, результативность его зачастую оказывается достаточной и в приложении к полярным жидкостям.
Пример 6.4
Методом Ганна-Ямады рассчитать плотность жидкого изобутилбензола, находящегося на линии насыщения в диапазоне 298-650 К. Критические параметры и ацентрический фактор вещества приведены выше.
Решение
Молярный объем вещества 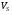 при избранной температуре вычисляется по уравнению (6.14).
при избранной температуре вычисляется по уравнению (6.14).
Поскольку экспериментальные данные для 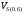 отсутствуют, то расчет масштабирующего параметра производим по уравнению (6.19):
отсутствуют, то расчет масштабирующего параметра производим по уравнению (6.19):
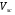
 82,05·650·(0,2920-0,0967·0,378)/31 = 439 см3/моль.
82,05·650·(0,2920-0,0967·0,378)/31 = 439 см3/моль.
Результаты расчета плотности приведены в табл.6.6 и на рис. 6.9. Для 298 К имеем:
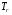 = 298/650 = 0,458;
= 298/650 = 0,458;
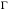 = 0,29607 – 0,09045·0,458 –0,04842·0,4582 = 0,244;
= 0,29607 – 0,09045·0,458 –0,04842·0,4582 = 0,244;
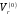 = 0,33593–0,33953·0,458+1,51941·0,4582+1,11422·0,4584 = 0,354;
= 0,33593–0,33953·0,458+1,51941·0,4582+1,11422·0,4584 = 0,354;
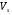 = 0,354·(1–0,378·0,244)·439 = 140,9 см3/моль;
= 0,354·(1–0,378·0,244)·439 = 140,9 см3/моль;
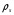 = 134,222/140,9 = 0,952 г/см3 .
= 134,222/140,9 = 0,952 г/см3 .
Метод Йена и Вудса
Метод предназначен для прогнозирования плотностей жидкостей при любых давлениях. В приложении к плотности насыщенной жидкости метод заключается в следующем. Приведенная плотность жидкости, находящейся на линии насыщения, коррелирована с приведенной температурой:
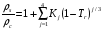 ,(6.21)
,(6.21)
где 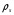 - мольная плотность насыщенной жидкости,
- мольная плотность насыщенной жидкости, 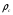 - критическая плотность вещества,
- критическая плотность вещества, 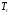 - приведенная температура.
- приведенная температура.
Коэффициенты 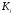 являются функциями критического коэффициента сжимаемости и вычисляются по уравнениям
являются функциями критического коэффициента сжимаемости и вычисляются по уравнениям
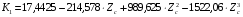 ;(6.22)
;(6.22)
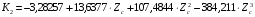 при
при 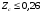 ;(6.23)
;(6.23)
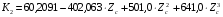 при
при 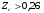 ;(6.24)
;(6.24)
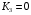 ;(6.25)
;(6.25)
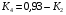 .(6.26)
.(6.26)
Пример 6.5
Методом Йена и Вудса рассчитать плотность жидкого изобутилбензола, находящегося на линии насыщения в диапазоне 298-650 К. Критический коэффициент сжимаемости изобутилбензола равен 0,28, критический объем составляет 480 см3/моль.
Решение
Вычисляем значения коэффициентов Kj:
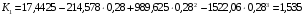 ;
;
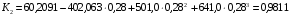 ;
;
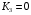 ;
;
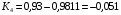 .
.
2. Критическая плотность изобутилбензола:
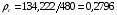 г/см3 .
г/см3 .
3. Рассчитываем плотность жидкого изобутилбензола, находящегося на линии насыщения. Для 298 К имеем
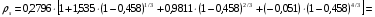 =0,8056 г/см3.
=0,8056 г/см3.
Фрагмент результатов расчета при других температурах приведен в табл. 6.6., на рис. 6.9. дается сопоставление их с полученными методом Ганна-Ямады и другими методами.
Метод Чью-Праусница
Метод предназначен для прогнозирования плотности жидкости при любых давлениях. В приложении к жидкому состоянию на линии насыщения метод заключается в следующем. Отношение критической плотности c к плотности насыщенной жидкости s коррелировано с приведенной температурой и ацентрическим фактором:
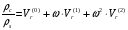 .
.
Для расчета 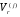 предложены следующие эмпирические уравнения:
предложены следующие эмпирические уравнения:
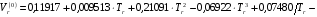
 ;(6.27)
;(6.27)
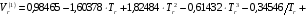
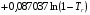 ;(6.28)
;(6.28)
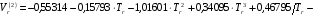
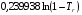 (6.29)
(6.29)
Пример 6.6
Методом Чью и Праусница рассчитать плотность жидкого изобутилбензола, находящегося на линии насыщения, в диапазоне 298-650 К. Критический объем составляет 480 см3/моль.
Решение
1. Вычисляем значения функций 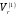 . Для 298 К имеем
. Для 298 К имеем
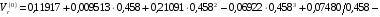
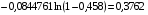 ;
;
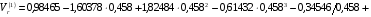
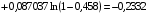 ;
;
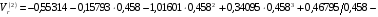
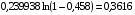 .
.
2. Вычисляем критическую плотность
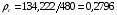 г/см3.
г/см3.
3. Рассчитываем плотность изобутилбензола при 298 К:
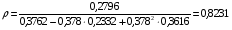
 г/см3.
г/см3.
Результаты расчета плотности насыщенной жидкости при других температурах приведены в табл. 6.6. и сопоставлены на рис. 6.9. с данными, полученными методами Ганна-Ямады и Йена-Вудса.
Таблица 6.6
Плотность жидкого изобутилбензола (г/см3) на линии насыщения,
вычисленная методами Ганна-Ямады ( ), Йена-Вудса (
), Йена-Вудса (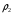 )
)
и Чью-Праусница (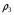 )
)
Т, К
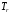
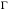
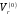
V
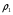
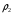
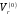
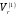
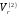
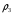
323
0,497
0,239
0,362
144,5
0,929
0,789
0,3760
-0,1921
0,2659
0,8189
373
0,574
0,228
0,380
152,3
0,882
0,753
0,3834
-0,1271
0,1062
0,7976
473
0,728
0,205
0,426
172,4
0,779
0,671
0,4238
-0,0408
-0,1195
0,7145
573
0,882
0,179
0,512
209,7
0,640
0,556
0,5091
-0,0094
-0,2057
0,5872
648
0,997
0,158
0,817
337,4
0,398
0,348
0,8333
-0,2592
0,4746
0,3481
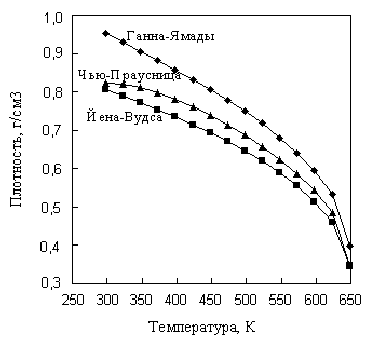
Р и с. 6.9. Зависимость плотности изобутилбензола
от температуры
Из сопоставления следует, что все рассмотренные методы единообразно передают характер изменения плотности изобутилбензола с изменением температуры, наибольшее различие в оценках составляет 18% отн. и относится к 298 К. Причем метод Йена-Вудса дает меньшие значения плотности во всем диапазоне температур. Опыт нашей работы показывает, что из рассмотренных методов предпочтение следует отдавать методам Ганна-Ямады, Чью-Праусница и методу, основанному на коэффициентах сжимаемости, которые вычислены по таблицам Ли-Кеслера или аналитическому уравнению состояния Бенедикта-Уэбба-Рубина.
Плотность ненасыщенной жидкости
При прогнозировании плотности ненасыщенной жидкости в основном используются следующие подходы.
1. В качестве опорного значения плотности принимается плотность насыщенной жидкости при рассматриваемой температуре; вычисляется вклад в плотность, обусловленный изменением давления от уровня давления насыщенного пара до заданного, и рассчитывается плотность жидкости под давлением.
2. По таблицам Ли-Кеслера или по уравнению состояния вещества вычисляется коэффициент сжимаемости при заданных температуре и давлении, после чего вычисляется молярный объем вещества и его плотность.

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ