Рвотные и противорвотные средства
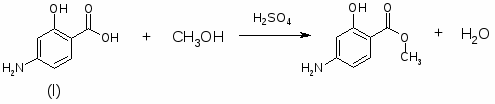
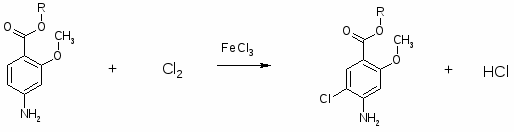

 Министерство образования и науки Украины
Министерство образования и науки Украины
УКРАИНСКИЙ ГОСУДАРСТВЕННЫЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ
КУРСОВАЯ РАБОТА
НА ТЕМУ:
РВОТНЫЕ И ПРОТИВОРВОТНЫЕ СРЕДСТВА
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ 3
1. ОБЩИЕ ПОЛОЖЕНИЯ 6
2. ИСТОРИЯ ВОЗНИКНОВЕНИЯ РВОТНЫХ И ПРОТИВОРВОТНЫХ ПРЕПАРАТОВ 12
3. МЕХАНИЗМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ 16
3.1. РВОТНЫЕ СРЕДСТВА 17
3.2. ПРОТИВОРВОТНЫЕ СРЕДСТВА 19
3.3. НЕЙРОЛЕПТИКИ 21
3.4. АНТИХОЛИНЕРГИЧЕСКИЕ (ХОЛИНОБЛОКИРУЮЩИЕ, ХОЛИНОЛИТИЧЕСКИЕ) СРЕДСТВА 22
3.5.ПРОТИВОГИСТАМИННЫЕ СРЕДСТВА 23
4. КЛАССИФИКАЦИЯ ПРЕПАРАТОВ 25
5. ТАБЛИЦА ПРЕПАРАТОВ 26
6. МЕТОДЫ ПОЛУЧЕНИЯ И АНАЛИЗА 31
6.1. Получение и анализ метоклопрамида 31
6.2. Получение и анализ бромоприда и диметпрамида 35
6.3. Получение и анализ ондансетрона 38
СЛОВАРЬ ТЕРМИНОВ 40
ЛИТЕРАТУРА 42
ВВЕДЕНИЕ
Рвота является одним из самых частых клинических симптомов, встречающихся в повседневной практике врачей разных специальностей, особенно бригад скорой и неотложной помощи. В некоторых случаях – при острых отравлениях, пищевой токсикоинфекции, синдроме острого живота и т.д. – причина рвота ясна и тактика ведения больных хорошо разработана. Но в определённых ситуациях этиология и патогенез рвоты остаются весьма трудной дифференциально-диагностической проблемой. Случай такой труднообъяснимой рвоты в англоязычной литературе получили название “unexplained vomiting” (“необъяснимая рвота”). [1].
Рвоту подразделяют на физиологическую и патологическую. Первая форма представляет собой, по сути, защитный физиологический механизм, благодаря которому организм избавляется от неудобоваримых физических и химических веществ, попавших в желудочно-кишечный тракт. Патологическая рвота не преследует этой цели, может вызываться самыми различными причинами и приводит к появлению вторичных клинических нарушений.
Патологическая рвота может быть осознанным и произвольным актом.
Рвота – сложно - рефлекторный акт, приводящий к извержению содержимого желудка (иногда вместе с содержимым кишечника) наружу через рот (реже и через нос).
При анализе психогенной рвоты имеют в виду, что и у здоровых лиц реакция на неприятные пищевые или на стрессовые раздражители нередко сопровождается рвотой и что склонность людей к рвоте весьма индивидуальна. Известно, что женщины более подвержены рвоте, чем мужчины, дети – в большей степени, чем взрослые.
Рвота часто является защитным актом, направленным на освобождение желудка от попавших в него раздражающих токсических веществ. В таких случаях это физиологический процесс, для ускорения которого может понадобиться применение специальных лекарственных (рвотных) веществ.
Рвота контролируется специальными структурами продолговатого мозга: рвотным центром и так называемой хеморецепторной пусковой зоной. Рвота развивается при возбуждении рвотного центра, что может произойти путем непосредственного воздействия на него токсических или лекарственных веществ, рефлекторного его возбуждения с центростремительных путей, а также при поступлении в него импульсов от хеморецепторов пусковой зоны. Хеморецептивная зона благодаря своей локализации способна принимать раздражения как через кровь (т.к. расположена перед гематоэнцефалическим барьером), так и через спинномозговую жидкость (благодаря близости с пространством желудочка).
Раздражение рецепторов пищеварительного канала передаётся через структуры через спинномозговую жидкость к ядрам одиночного пути (Nucleus tractus solitarii) продолговатого мозга, хотя часть волокон достигает непосредственно хеморецептивной зоны. 2].
Эта зона особенно чувствительна к действию химических веществ и рвотное, так же как и противорвотное, действие многих лекарственных веществ реализуется путем первичного возбуждения или торможения этой зоны. Из лекарственных веществ непосредственное центральное действие на пусковую зону оказывают морфин и другие наркотические анальгетики, апоморфин, противоопухолевые препараты и др.
Основное применение в качестве лекарственного рвотного средства имеет апоморфин.
Акту рвоты предшествуют тошнота и ряд сопровождающих ее эффектов, в том числе усиление саливации и бронхиальной секреции. Эти эффекты наблюдаются также при применении рвотных средств в малых дозах, причем некоторые из них используются в качестве отхаркивающих средств.
Противорвотное действие могут оказывать вещества, влияющие на разные звенья нервной регуляции.
Если рвота вызвана местным раздражением желудка, то после удаления раздражающих веществ в случае необходимости могут быть применены обволакивающие и вяжущие средства. Уменьшение возбудимости рецепторов желудка и подавления тошноты и рвоты может быть достигнуто назначением местных анестетиков.
Для снятия возбуждения рвотного центра ранее основное применение имели седативные и снотворные средства. Существенные успехи в получении специфичных, высокоэффективных противорвотных средств центрального действия связаны с развитием работ по изучению холинолитических, противогистаминных, нейролептических препаратов.
Противорвотное действие различных нейротропных препаратов в значительной степени связано с их влиянием на нейромедиаторные системы рвотного центра и хеморецепторной пусковой зоны. Хеморецепторная зона содержит дофаминовые рецепторы, в разных ядрах рвотного центра имеются холинергичекие, гистаминовые и серотониновые 5-НТ3-рецепторы.
В последнее время важную роль в развитии рвоты и механизме действия противорвотных средств придают серотониновым (5-НТ3) рецепторам.
Холинолетические препараты нашли наибольшее применение в профилактике и лечении морской и воздушной болезни.
Для этих же целей широко применяют противогистаминные препараты: димедрол, дипразин и др. В механизме действия этих препаратов определенную роль играют также их седативный эффект и холинолетический компонент.
Эффективными противорвотными средствами являются нейролептические препараты группы фенотиазина и бутирофенона, действующие на дофаминергические системы. Их действие связано главным образом с тормозящим влиянием на хеморецепторную зону. Высокой противорвотной активностью в ряду производных фенотиазина обладают этаперазин, метеразан, трифтазин и др., в ряду бутерофенов - галоперидол и др.
К производным фенотиазина, обладающим сильным и более избирательным действием, чем другие нейролептики, и не вызывающим поэтому побочных эффектов, связанных с общей нейролептической активностью, относится препарат тиэтилперазин.
К противорвотным препаратам, действие которых связанно преимущественно с влиянием на серотониновые (5-НТ3) рецепторы, относят ондансетрон, трописетрон.
Метопрокламид и его аналоги влияют на серотониновые (5-НТ3) рецепторы, одновременно блокируя дофаминовые (D2) рецепторы.
В связи с комплексностью нейрохимической организацией рвотного акта наиболее выраженный противорвотный эффект может наблюдается при комбинированном применении веществ, влияющих на разные медиаторные системы. 3].
1. ОБЩИЕ ПОЛОЖЕНИЯ
При раздражении слизистой оболочки зева, пищевода и желудка большое значение имеют рефлексы защитного характера. В результате этих рефлексов возникает рвота. Рвота способствует удалению из желудка токсических продуктов, препятствуя их дальнейшему поступлению в кишки и всасыванию в кровь. 4].
Рвота наблюдается у многих видов млекопитающих, за исключением грызунов, у которых отсутствует рвотный центр. Рвоту не наблюдают также у некоторых травоядных.
Рвотные средства (emetica) применяют для удаления сильно раздражающих веществ, которые попали в желудок при отравлении. По существу она представляет собой защитный механизм, обеспечивающий удаление раздражающего и токсического вещества из верхних отделов желудочно-кишечного тракта 5].
Слизистые рта, желудка и кишечника снабжены рецепторами, обладающими высокой чувствительностью к раздражителям, поступающим с пищей и питьём. С этих рецепторов возникают рефлексы, обеспечивающие секреторную и двигательную реакцию на пищу, а так же защитные реакции при попадании через рот вредных или «отвергаемых», веществ, как их называл И.П. Павлов.
Исследованиями И.П. Павлова, произведёнными по созданному им методу хронических фистул, доказана чрезвычайная избирательность реакций этих рецепторов. Благодаря этому, состав слюны, характер секреции желудочного, поджелудочного и кишечного соков строго зависят от химического состава пищевых раздражителей и от характера механического воздействия на слизистые оболочки 4.
Рвотный центр может возбуждаться либо непосредственно (через кровь, например, при воспалительных явлениях в центральной нервной системе, интоксикации, острой анемии мозга и т. п.), или рефлекторно через окончания чувствительных нервов задней стенки глотки, корня языка, носоглотки, желудка, верхних отделов кишок, печени, почек, брюшины и др. Причиной рвоты могут быть и психические раздражения, которые вызывают чувство отвращения. На основе безусловных рвотных рефлексов может быть вызвана условно-рефлекторная рвота на алкоголь при лечении алкоголиков.
Акт рвоты находится под контролем центра рвоты, локализованного в продолговатом мозге рядом с другими центрами, регулирующими функции органов и систем организма, так же вовлекающимися в процесс рвоты и определяющими сопутствующие физиологические изменения в продромальном периоде и во время рвоты. Она возникает при активации центра рвоты самыми разнообразными стимулами. Это могут быть вызывающие отвращение зрительные, обонятельные или вкусовые ощущения. Раздражение вестибулярного аппарата и интероцепторов различной локализации так же может быть причиной рвоты [5].
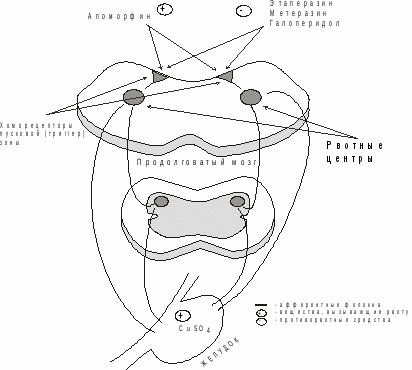
Уставлено, что с центром рвоты связана специальная зона, получившая название пусковой зоны (trigger zone), которая очень чувствительна к действию химических веществ, чуждых для организма. Расположена она на дне IV желудочка (рис.1).
Рвота наступает при возбуждении рвотного центра, а также при поступлении в него импульсов от хеморецепторов триггерной зоны 6].
Различают центральный и рефлекторный механизм возбуждения рвотного центра. Отсюда и деление рвотных средств на две группы – центрального (прямого) и рефлекторного (периферического) действия. Из лекарственных веществ непосредственное центральное действие на пусковую зону оказывают морфин и другие наркотические анальгетики, апоморфин, противоопухолевые препараты и др. Периферическое действие оказывают вещества, раздражающие рецепторы слизистой оболочки желудка, такие как меди, сульфат, цинка сульфат и др. Сердечные гликозиды (при передозировке) могут вызвать рвоту, действуя непосредственно на пусковую зону продолговатого мозга, а так же рефлекторным путём. Вещества, которые действуют центрально или непосредственно на рвотный центр, следует вводить парентерально, а вещества, которые действуют рефлекторно – внутрь [5].
Рвотный центр координирует акт рвоты на основании поступления сигналов из различных источников:
хеморецепторов триггерной зоны (ХРТЗ), очень чувствительной к воздействию лекарственных и других химических веществ;
вестибулярной системы;
с периферических отделов, например, при растяжении или раздражении кишечника, инфаркте миокарда, из корковых центров.
Рвотный центр содержит много мускариновых холинэргических рецепторов, H1- рецепторов гистамина и серотониновых 5-HT3- рецепторов. В ХТЗ преобладают дофаминовые рецепторы 7].
В настоящее время ХРТЗ представляет собой скорее физиологическую или фармакологическую структуру, чем морфологическую единицу. Многочисленные агенты, в том числе морфин, апоморфин, алкилирующие средства и гликозиды наперстянки, стимулируют ХРТЗ, а фенотиазины и некоторые антигистаминные средства угнетают их. Однако следует сказать, что ХРТЗ являются только промежуточным пунктом на пути сенсорной чувствительности и в отсутствии стимуляции рвотного центра не способна вызвать рвоту, в то время как непосредственное электрическое или химическое раздражение рвотного центра может провоцировать рвоту. Рвоте обычно предшествует чувство тошноты и повышенная секреция слюны, бронхиального секрета и пота. Мышцы, принимающие участие в акте кашля, участвуют и в акте рвоты, а центры блуждающего нерва, рвотный и кашлевой тесно связаны функционально. Рвота – акт, частично управляемый, она может быть вызвана насильственно, произвольно и у детей легче, чем у взрослых 8].
Рвотный акт может наступить при механическом раздражении слизистой оболочки зева. Механическое раздражение зева поэтому является наиболее простым способом взывания рвоты. Рвота наблюдается при непосредственном возбуждении рвотного центра или связанной с ним частей мозга, например при опухолях мозга, воспалении мозговых оболочек и других инфекционных заболеваниях.
Показанием к применению рвотных средств центрального действия является необходимость вызвать быструю рвоту при невозможности удалить ядовитое вещество промыванием желудка (у покушавшихся на самоубийство, психически больных, при потере сознания и нарушении глотания и т. п.).
Однако следует подчеркнуть, что применение рвотных средств не обеспечивает полного удаления попавшего в желудок яда, так как спазматические сокращения отдельных частей желудка создают условия для удержания части яда в складках слизистой оболочки.
Противопоказаниями к применению рвотных средств являются заболевания сердца, гипертензия, туберкулез легких с кровотечениями, воспалительные процессы органов пищеварительной системы, тяжелые случаи угнетения нервной системы с поражением рвотного центра, выраженные формы истощения, ожоги пищевода и желудка вследствие действия крепких кислот и щелочей, беременность (опасность аборта в результате энергичных сокращений мышц живота), грыжа (опасность ущемления). Из-за значительного нарушения во время рвоты сердечной деятельности, артериального давления и дыхания рвотные средства очень тяжело переносят лица с заболеваниями сердечно-сосудистой системы, а также лица старческого возраста.
Следует подчеркнуть, что применение рвотных средств не обеспечивает полного удаления попавшего в желудок яда, так как спазматические сокращения отдельных частей желудка создают условия для удержания части яда в складках слизистой оболочки [5].
Однако в ряде случаев рвота является сопутствующим процессом, ухудшающим состояние организма. Нередко рвота развивается в результате общего токсикоза, обусловленного поступлением в организм (не только через желудок, но и парентеральным путём) токсических продуктом, в том числе лекарственных средств. Рвота может быть обусловлена различными заболеваниями, оперативными вмешательствами, эмоциональным возбуждением и т.п. Лучевая терапия также обычно осложняется рвотой. Нередко рвота наступает в результате перевозбуждения лабиринтного аппарата (например, при морской и воздушной болезни). В этих и других случаях часто необходимо применение средств, успокаивающих рвоту.
Если рвотные средства в настоящее время применяются редко, то борьба с рвотой, изнуряющей и обезвоживающей организм (назначение противорвотных средств), необходима довольно часто [7].
Механизм рвотного акта обязательно должен учитываться при выборе противорвотных средств в каждом конкретном случае. Противорвотные средства, как и рвотные, можно разделить на две группы: центрального и рефлекторного действия [8].
Противорвотное действие могут оказать вещества, влияющие на разные звенья нервной регуляции. Например, если причина рвоты связана с непосредственным раздражением рвотного центра, следует применять средства, оказывающие успокаивающее и угнетающее влияние на центральную нервную систему (седативные, снотворные, антихолинергические, противогистаминные и особенно нейролептики).
Противорвотное действие нейролептиков группы фенотиазина (аминазин и др.) и группы бутерофенона, связано, главным образом, с тормозящим влиянием их на хеморецепторную пусковую зону в продолговатом мозге.
При рвоте рефлекторного характера, причиной которой является раздражение чувствительных нервов в слизистой оболочке желудка или кишок, применяют местноанестезирующие и обволакивающие средства. При спазме кишок, желчных и почечных проходов, мочевых путей, сопровождающихся рвотой, применяют спазмолитики.
Показаниями к назначению препаратов этой группы, в частности этаперазина, служит рвота беременных, рвота, связанная с заболеваниями желудка или вызванная лекарственными веществами. Препарат оказывает выраженное расслабляющее действие на мышцы, хорошо успокаивает икоту. При рвоте, связанной с вестибулярными нарушениями, этаперазин и ему подобные вещества малоэффективны. Поэтому при морской или воздушной болезни обычно назначают скополамин (м-антихолинергическое средство), который обладает прямым угнетающим влиянием на рвотный центр в продолговатом мозге. Скополамин входит в состав таблеток «Аэрон», применяемых против укачивания и при болезни Меньера.
Кроме указанных средств, противорвотным действием при нарушениях функции вестибулярного аппарата обладают препараты ментола (валидол), применяемые внутрь. При рвоте, вызванной раздражением слизистой оболочки желудка, показано промывание желудка, анестезия его слизистой оболочки холодом (глотать кусочки льда), ментол, мятная вода или местноанестезирующие средства (анестезин, новокаин). При спазме органов брюшной полости (пилороспазм, желчная и кишечная колика) и мочевых путей показаны спазмолитики (атропин, папаверин, ношпа), амилнитрит (вдыхание 2—3 капель). При застойных явлениях в желудке эффективен прием 2—3 капель раствора йода на рюмку воды. При периодических сокращениях «голодного» желудка показан раствор хлористоводородной кислоты.
В связи с комплексностью нейрохимической организации рвотного акта наиболее выраженный противорвотный эффект может наблюдаться при комбинированном применении веществ, влияющих на разные медиаторные системы [5].
2. ИСТОРИЯ ВОЗНИКНОВЕНИЯ РВОТНЫХ И ПРОТИВОРВОТНЫХ ПРЕПАРАТОВ
Раньше в качестве рвотного средства применяли корень ипекакуаны, или рвотный корень, действующим веществом которого является алкалоид эметин. После приёма внутрь корня ипекакуаны рвота наступает не сразу, а лишь после довольно длительного периода времени, в течение которого происходит суммация импульсов, поступающих с чувствительных нервных окончаний к рвотному центру. В 1817году из корня ипекакуаны был выделен алкалоид эметин.
В 1890 году был синтезирован анестезин. Годом раньше русский ученый В. К. Анреп открыл местноанестезирующие свойства алкалоида кокаина. В 1905 году был осуществлён синтез новокаина. Эти события положили начало широкому применению лекарственных средств для местной анестезии. Анестезин весьма активен при местном применении. До сих пор его применяют в виде присыпок, мазей, микстур (меновазин и др.) при кожном зуде, невралгии, миалгиях, ссадинах, трещинах, ожогах, при боли в области желудка, иногда назначают внутрь при рвоте, при морской и воздушной болезни.
Приоритет в открытии и изучении механизма действия рвотных средств принадлежит Н. Н. Токареву в лаборатории И. П. Павлова, который в 1895 г. первый исследовал рвотное действие алкалоида эметина и установил рефлекторный характер его действия. Было доказано, что эметин вызывает рвоту лишь при введении его через рот. Введение его ректально или подкожно неэффективно.
В 1918 году был расшифрован механизм действия атропина. Стало очевидно, что для эндогенного ацетилхолина должны существовать в организме “места связывания” - рецепторы, для которых ацетилхолин является естественным лигандом. Таким образом, сформировались первые представления о холинорецепторах.
Специальной группой антихолинергических препаратов являются средства, оказывающие преимущественное влияние на центральные холинреактивные системы. Блокатором центральных холинорецепторов в определенной степени является атропин, однако значительно более специфическое блокирующее влияние на эти рецепторы оказывают, созданные начиная с 40 - 50-х годов, синтетические “центральные холинолитики”.
В 1919 году Кеннон обнаружил “шокоподобное” действие гистамина при его внутреннем введении животным. Интерес к гистамину еще больше повысился, когда в 1927 году его обнаружили в легких и других тканях животных. Так в 1917 - 1929 годах было обнаружено, что гистамин высвобождается из клеток организма при ожогах. При внутрикожном введении растворов гистамина обнаружилось повышение проницаемости сосудов, отек тканей. Гистамин стал рассматриваться, как один из “медиаторов” воспаления и аллергии. Т.о., стали назревать идеи о целесообразности создания фармакологических средств, влияющие на гистаминергические процессы, в первую очередь противогистаминных препаратов. Реализовать эту идею удалось в 1935-1937 годах. В 1945-1946 годах были созданы фенотиазиновые противогистаминные препараты: этизана, дипразина и др. В 50-е годы стали широко применять димедрол.
Крупным фундаментальным достижением 50-х годов выявилось открытие медиаторной роли серотонина.
В конце прошлого века физиологи обнаружили, что при образовании кровяных сгустков из них выделяется вещество, вызывающее сужение кровеносных сосудов, и дали ему название вазотонин. В 40-х годах ХХ столетия было высказано предположение, что это вещество играет роль в патогенезе артериальной гепертензии и началось его подробное изучение. В 1948 году оно было выделено в кристаллическом виде и названо серотонином. Синтез серотонина был осуществлён в 1951 году.
При изучении эндогенных серотонинергических процессов было выявлено три вида серотониновых рецепторов.
В 1952 году была обнаружена специфическая эффективность хлорпропазина (аминазина) и резерпина для лечения психических больных.
В 1957г. были открыты впервые антидепрессанты (ипрониазид, имипрамид). Затем обнаружили транквилизирующие свойства мепробамата и производных бензодиазепина.
В 1966г. научная группа ВОЗ предложила для психотропных препаратов первую классификацию:
- нейролептики, они же “антипсихотические средства”, ранее обозначавшиеся как “большие транквилизаторы”;
- анксиолитические средства, ранее обозначавшиеся “большие транквилизаторы”;
- антидепрессанты, иногда их называют также “психические энергизаторы”;
- психостимуляторы;
- психодислептики, называемые также “психозомиметические вещества”.
Новая группа психотропных препаратов - “ноотропов”, первым представителем которых был пирацетам, появилась в начале 70-х годов.
Раздел фармакологии, занимающийся изучением этих веществ, получил название “психофармакология”, а препараты указанных видов действия стали называться психотропными.
В 1967г. Конгресс психиатров в Цюрихе предложил разделить эти препараты на две группы:
а) нейролептические вещества, применяемые преимущественно при тяжелых нарушениях деятельности ЦНС (психозах);
б) транквилизирующие вещества, применяемые при менее выраженных нарушениях функций ЦНС, главным образом при неврозах.
Нейролептические вещества первоначально назывались ”нейроплегики”. Транквилизаторы обозначались также как “атарактики”, “антифобические средства” и др.
В 1989 году были синтезированы блокаторы серотониновых 5-нт3 – рецепторов препараты ондансетрон (латран), трописетрон и другие. Через эти рецепторы, плотно локализованные в триерных зонах рвотного центра мозга, реализуются тошнота и рвота, обусловленные поступлением в организм химических соединений, особенно противоопухолевых препаратов.
Большой интерес вызвали синтезированные в последнее время (1989) препараты ондансетрон (латрин), трописетрон и др. Через эти рецепторы, плотно локализованные в тригерных зонах рвотного центра мозга, реализуется тошнота и рвота, обусловленные поступлением в организм химических соединений, особенно противоопухолевых препаратов. Ондансетрон и трописетрон, их аналоги нашли широкое применение для профилактики и терапии этих осложнений при химио- и лучевой терапии онкологических заболеваний.
Под психотропными подразумеваются лекарственные средства, применяемые специально для лечения психических заболеваний.
Первые современные психотропные препараты были созданы в начале 50-х годов XX века. До этого основными препаратами, используемые для этой цели, были снотворные и седативные средства, инсулин, кофеин.
Хронологическая таблица.
Год
1895 г
(Н.Н.Токарев.) -
Первые исследования рвотного действия алкалоида эметина и установление рефлекторного характера его действия
1876 г
Выделение из продуктов гниения белков гистамина
1890 г
1905 г
Осуществлен синтез новокаина
1918 г
Расшифрован механизм действия атропина
1919 г
(Кеннон.)
Обнаружено “шокоподобное” действие гистамина при его внутривенном введении животным
1927 г
Обнаружение гистамина в легких и других тканях животных
1917-1929 годах
Выявлено, что гистамин высвобождается из клеток организма при ожогах
1935-1937 годах
1945-1946 годах
Созданы фенотиазиновые противогистаминные препараты: дипразин, этизан и др.
1948 годах
Выделен в кристаллическом виде серотонин
1951 годах
Синтез серотонина
1952 годах
Обнаружена специфическая эффективность аминазина для лечения психических больных
1957 годах
1966 годах
Научной группой ВОЗ была предложена для психотропных препаратов первая классификация
1989 годах
3. МЕХАНИЗМ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ
В процессе рвоты принимают участие дыхательная мускулатура, мышцы брюшного процесса и пищевой канал. Вначале наблюдается антиперистальтика тонкой кишки, и её содержимое частично забрасывается в желудок. Затем возникает спазм привратника и препилорической части желудка с одновременным расслаблением дна желудка и пищевода, вход в желудок открывается. В момент рвоты происходит глубокий вдох, создаётся отрицательное давление в грудной полости, присасывающее действие способствует переходу содержимого желудка в пищевод. Одновременно резко сокращается диафрагма и брюшной пресс, что приводит к повышению внутрижелудочного давления, и в момент выдоха содержимое желудка выбрасывается через пищевод и полость рта наружу.
Важным моментом в рвотном акте является то, что в начальной фазе его наблюдается усиление отделения слюны, секреции бронхиальных желез, расслабление мускулатуры бронхов, что облегчает отделение мокроты. Эти эффекты наблюдаются также при применении рвотных средств в малых дозах, что даёт возможность некоторые из них использовать в качестве отхаркивающих средств.
Перед рвотой происходит учащение, а затем замедление дыхания, изменение ритма сокращений сердца, наблюдается потоотделение, усиление секреции слюнных желез, слизистых желез пищевода и зева, а также слизистых желез дыхательных путей.
Во время рвоты кратковременно повышается артериальное давление, после чего наступает быстрое его снижение и как следствие – слабость мышц.
Рвоте обычно предшествует период nausea (морская болезнь, тошнота).
Происхождение тошноты, место возникновения чувствительных импульсов и пути их проведения до конца не изучены. Причиной тошноты могут быть раздражение лабиринтов, болевое раздражение внутренних органов, отрицательные эмоции.
У человека тошнота обычно сопровождается бледностью, холодным потом, усиленной секрецией желез полости рта, желудка, бронхов, слезотечением, неправильным дыханием, снижением артериального давления, слабостью мышц, угнетением произвольных движений.
Важнейшим результатом взаимодействия лекарственного вещества с определенной тканью является физико-химическое взаимодействие молекулы лекарственного вещества со специфическими, с родственными молекулами биологической системы клетки этой ткани. Такая специфическая биомолекула (или ее часть) называется циторецептором. Специфичность циторецептора определяется структурной комплиментарностью его с данным лекарственным веществом. В результате комплексирования изменяется конформация биомолекулы. Это влечет за собой изменение ее функции в клетке, а затем и изменение функции самой клетки (первичная, или стартовая, фармакологическая реакция). Изменение функции отдельных клеток приводит к изменению функции органа или системы.
Данный механизм лежит в основе действия лекарственного препарата на организм человека в общем, однако, если рассматривать непосредственно влияние определенных групп лекарственных средств на те или иные органы, то возникает ряд характерных особенностей. Поэтому при освещении фармакодинамических свойств лекарственных веществ фиксируется внимание не столько на общих моментах, сколько на особенностях, характеризующих механизм действия каждой группы лекарственных веществ.
1.3.1. РВОТНЫЕ СРЕДСТВА
Рвотные средства применяют для удаления сильно раздражающих веществ, которые попали в желудок, и для опорожнения желудка при отравлении.
Однако в ряде случаев рвота является симптомом заболевания, ухудшающим состояние организма.
Рвота представляет собой сложный координированный процесс, ведущий к освобождению желудка от его содержимого. В этом процессе принимают участие дыхательная мускулатура, мышцы брюшного пресса и пищевой канал. В начале наблюдается антиперистатика тонкой кишки, и ее содержимое частично забрасывается в желудок. Затем возникает спазм привратника и препилорической части желудка с одновременным расслаблением дна желудка пищевода, вход в желудок открывается. В момент рвоты происходит глубокий вдох, создается отрицательное давление в грудной полости, присасывающие действие способствует переходу содержимого желудка в пищевод. Одновременно резко сокращается диафрагма и брюшной пресс, что приводит к повышению внутрижелудочного давления, и в момент выхода содержимое желудка выбрасывается через пищевод и полость рта наружу.
Важным моментом в рвотном акте является то, что в начальной фазе его наблюдается усиление отделения слюны, секреции бронхиальных желез, расслабление мускулатуры бронхов, что облегчает отделение мокроты.
Перед рвотой происходит учащение, а затем замедление дыхания, изменение ритма сокращений сердца, наблюдается потоотделение, усиление секреции слюнных желез, слизистых желез пищевода и зева, а также слизистых желез дыхательных путей.
Во время рвоты кратковременно повышается артериальное давление, после чего наступает быстрое его снижение и как следствие - слабость мышц.
Рвоте обычно предшествует период nausea (морская болезнь, тошнота). Происхождение тошноты, место возникновения чувствительных импульсов и пути их проведения до конца не изучены. Причиной тошноты могут быть раздражение лабиринтов, болевое раздражение внутренних органов, отрицательные эмоции.
У человека тошнота обычно сопровождается бледностью, холодным потом, усиленной секрецией желез полости рта, желудка, бронхов, слезотечением, неправильным дыханием, снижением артериального давления, слабостью мышц, угнетение произвольного движения.
Координация рвотного акта осуществляется при помощи парного рвотного центра, находящегося в продолговатом мозге, в основном, в боковой части сетчатого образования, в солитарном пучке и его ядре. Рвотный центр расположен в продолговатом мозге рядом с кашлевым центром и центром блуждающего нерва.
Нервные волокна, несущие возбуждение к рвотному центру, проходят главным образом в составе блуждающего нерва.
Рвотный центр в продолговатом мозге имеет хеморецепторную пусковую (триггерную) зону, которая очень чувствительна к действию химических веществ, чуждой для организма. Рвота наступает при возбуждении рвотного центра, а также при поступлении в него импульсов от хеморецепторов триггерной зоны.
Рвотный центр может возбуждаться либо непосредственно (через кровь, например, при воспалительных явлениях в ЦНС и т.п.), или рефлекторно через окончания чувствительных нервов задней стенки глотки, корня языка, носоглотки, желудка, верхних отделов кишок, печени, почек, брюшины и др. Причиной рвоты могут быть и психические раздражения, которые вызывают чувство отвращения. На основе безусловных рвотных рефлекторов может быть вызвана условно-рефлекторная рвота на алкоголь при лечении алкоголиков.
Рвотный акт может наступить при механическом раздражении слизистой оболочки зева. Механическое раздражение зева поэтому является наиболее простым способом вызывания рвоты. Рвота наблюдается при непосредственном возбуждении рвотного центра или связанных с ним частей мозга, например при опухолях мозга, воспалении мозговых оболочек и других инфекционных заболеваниях.
Различают центральный и рефлекторный механизм возбуждения рвотного центра. Отсюда и деление рвотных средств на две группы - центрального и рефлекторного действия. Вещества, которые действуют центрально или непосредственно на рвотный центр (апоморфин), следует вводить парентерально, а вещества, которые действуют рефлекторно, - внутрь.
К препаратам рвотных средств центрального действия относится, прежде всего, апоморфина гидрохлорид. Практически он является единственным применяемым в настоящее время рвотным средством. Средняя доза апоморфина вызывает обычно многократную рвоту после очень короткой стадии тошноты. Большие дозы апоморфина действуют противорвотно, что объясняется угнетением сетчатого образования. Рвотное действие его может быть использовано и при хроническом алкоголизме. Для этого с помощью апоморфина вырабатывают отрицательный условный рефлекс на алкоголь.
Среди рвотных средств рефлекторного действия можно отметить соли тяжелых металлов - цинка и меди сульфат. Меди и цинка сульфат наиболее быстро вызывают рвоту рефлекторного характера. Однако практическое применение их ограничено, так как они действуют раздражающе на слизистую желудка и могут вызвать общетоксичекое действие.
2.3.2. ПРОТИВОРВОТНЫЕ СРЕДСТВА
Если рвотные средства в настоящее время применяются редко, то борьба с рвотой, изнуряющей и обезвоживающей организм, необходимо довольно часто.
Механизм рвотного акта обязательно должен учитываться при выборе противорвотных средств в каждом конкретном случае. Противорвотные средства, как и рвотные, можно разделить на две группы: центрального и рефлекторного действия.
Если причина рвоты связана с непосредственным раздражением рвотного центра, следует применять средства, оказывающие успокаивающее и угнетающее влияние на ЦНС (седативные, снотворные, антихолинергические, противогистаминные и особенно нейролептики).
Противорвотное действие нейролептиков группы фенотиазина (аминазин) связано, главным образом, с тормозящим влиянием их на хеморецепторную пусковую зону в продолговатом мозге.
При рвоте рефлекторного характера, причиной которой является раздражение чувствительных нервов слизистой оболочки желудка или кишок, применяют местноанастезирующие средства. При спазме кишок, желчных и почечных ходов, мочевых путей, сопровождающихся рвотой, применяют спазмолитики.
Среди наиболее известных в настоящее время противорвотных средств следует отметить этапиразин, который в 10 раз активнее, чем аминазин. Этапиразин является активным нейролептическим средством. Механизм его действия связан со способностью угнетать рецепторы триггер-зоны продолговатого мозга.
Показаниями к назначению препаратов этой группы, в частности этапиразина, служит рвота беременных, рвота, связанная с заболеванием желудка или вызванная лекарственными веществами. Препарат оказывает выраженное расслабляющее действие на мышцы, хорошо успокаивает икоту.
При рвоте, связанной с вестибулярными нарушениями, этаперазин и ему подобные вещества малоэффективны. Поэтому при морской или воздушной болезни обычно назначают скополамин (м-антихолинергическое средство), который обладает прямым угнетающим влиянием на рвотный центр в продолговатом мозге. Скополамин входит в состав таблеток “Аэрон”, применяемых против укачивания и при болезни Меньера.
Кроме указанных средств, противорвотным действием при нарушениях функции вестибулярного аппарата обладают препараты ментола (валидол), применяемых внутрь. При рвоте, вызванной раздражением слизистой оболочки желудка, показано промывание желудка, анестезия его слизистой оболочки холодом (глотать кусочки льда), ментол, мятная вода или местноанестезирующие средства (анестезин). При спазме органов брюшной полости (пилороспазм, желчная и кишечная колика) и мочевых путей показаны спазмолитики (папаверин).
Таблица 1. Лекарственные средства, эффективные при рвоте и тошноте
№ п/п
ТОЧКА ПРИЛОЖЕНИЯ ДЕЙСТВИЯ
1.
Холинолитики, скополамин и некоторые средства, относящиеся к блокаторам Н1-рецепторов гистамина [циклизин, дименгидринат (димедрол), дифенгидрамин, меклозин, мепирамин, прометазин]
Рвотный центр
2.
Антагонисты дофамина, домперидон, метоклопрамид, галоперидол
ХТЗ и кишечник
3.
Фетотиазины, хлорпромазин (аминазин), прохлорперазин, триэтилперазин
Рвотный центр и ХТЗ
4.
Другие лекарственные средства (при рвоте, обусловленной цитотоксическим действием): кортикостероиды (дексаметазон, метилпреднизалон), набилон (каннабиноиды), бензодиазепины (диазепам, лоразепам)
Рвотный центр и ХТЗ
3.
4.3.3. НЕЙРОЛЕПТИКИ
Действие производных фенотиазина является весьма сложным. Они повышают порог возбудимости не только чувствительных, и двигательных элементов подкорковой области и коры большого мозга. Классическим представителем производных фенотиазина является аминазин.
Аминазин, как и другие производные фенотиезана, растворяется в воде, хорошо всасывается и легко проникает через гематоэнцефалический барьер. В мозге производные фенотиазина в большом количестве накапливаются в зрительном бугре, подбугорной области, в среднем мозге и значительно меньше - в коре большого мозга.
Снижая возбудимость рецепторов триггер-зоны рвотного центра, заложенного на дне четвертого желудка, производные фенотиазина обладают противорвотным действием. Они способны подавлять икоту. Однако при рвоте, связанной с раздражением рецепторов вестибулярного аппарата и слизистой оболочки пищевого канала, ни аминазин, ни другие производные фенотиазина не эффективны.
Вовлечение в реакцию центров подбугорной области, а также других близко расположенных структур сопровождается снижением центрального влияния на секреторную деятельность надпочечных и других эндокринных желез, что приводит, в частности, к уменьшению секреции адреналина и кортикостероидов. Обмен веществ и температура тела снижается. В механизме гипотермии, с одной стороны, играет роль снижения тонуса симпатических сосудодвигательных центров, расширение периферических сосудов и увеличение теплоотдачи, а с другой - снижение теплопродукции в связи со снижением обмена веществ.
На биохимическом уровне производные фенотиазина угнетают процессы аэробного окисления в нейронах. Тормозят НАД- и НАДФ- зависимые дегидрогиназы, аденозинтрифосфатазу, цитохромоксидазу и фосфодиэстеразу, что приводит к накоплению глюкозы и гликогена и способствует процессам регенерации и восстановления структуры нервных клеток. Параллельно с уменьшением энергетического обмена под действием производных фенотиазина снижает обмен фосфолипидов и белков мозга, а вместе с торможением активности аденозинтрифосфатазы уменьшается трансмембранный перенос метаболитов.
В ряду лекарственных препаратов группы бутерофена, оказывающих выраженное депремирующее действие на эмоциональную и двигательную сферы ЦНС, особый интерес представляет галопередол.
Механизм депремирующего действия изучен не достаточно. Подобно аминазину, галоперидол обладает адренолитическим действием на синаптические образования центральной и периферической нервной системы, купирует невротические и реактивные состояния, рвоту различного происхождения, оказывает выраженное противосудорожное действие.
По строению и фармакодинамическим свойствам к группе фенотиазина близко примыкают производные тиоксантена, в частности хлорпротиксен.
В отличие от аминазина хлорпротиксен устраняет состояние депрессии, чувство боли и ощущение страха. Поэтому он часто применяется при психозе, сопровождающемся агрессивностью, психомоторным возбуждением. Оказывает сильное противорвотное действие.
5.
6.3.4. АНТИХОЛИНЕРГИЧЕСКИЕ (ХОЛИНОБЛОКИРУЮЩИЕ, ХОЛИНОЛИТИЧЕСКИЕ) СРЕДСТВА
Антихолинергическими средствами, или холиноблокаторами, называют вещества, блокирующие холинорецепторы, предшествуя воздействие с ними ацетилхолина. В результате блокады холинорецепторов нарушается передача импульсов с холинергических нейронов на иннервируемые ими клетки. Вещества, которые блокируют м- и н-холинорецепторы, обладают недостаточной избирательностью действия, малоактивны, поэтому применяются весьма ограниченно. Более широко используются холиноблокаторы, избирательно блокирующие только м- и н-холинорецепторы.
м-Холиноблокаторы. Эта группа включает природные вещества, а именно алкалоиды - гиосциамина, его рецемат атропин, скополамин, выделяемые из красавки, белены и дурмана. Общим свойствами веществ является избирательно блокировать м-холинорецептороы. Это свойство обусловлено сходством строения м-холиноблокаторов с ацетилхолином. В основе действия м-холиноблокаторов лежит их конкурентный антагонизм с ацетилхолином в некоторых холинэргических синапсах. В результате м-холиноблокаторы затрудняют или делают невозможной передачу импульсов с парасимпатических постганглионарных волокон на клетки исполнительных органов (сердца, гладкомышечных органов, желез внешней секреции), а также импульсов поступающих к потовым железам по симпатическим холинэргическим нервам.
Скополамин обладает более сильным, чем у атропина, угнетающим влиянием на ЦНС, особенно на ядра вестибулярного нерва. Поэтому его применяют при паркинсонизме, вестибулярных нарушениях, при купировании эпилептического статуса.
Предполагают, что эти препараты реагируют также с соответствующими компонентами клеточной мембраны, делая их непроницаемыми для гистамина, а гладкомышечные волокна - нечувствительными к нему.
7.
8.3.5.ПРОТИВОГИСТАМИННЫЕ СРЕДСТВА
Механизм действия противогистаминных средств основан на их конкурентном антагонизме (химической или биологической конкуренции) с гистамином с последующей блокадой гистаминореактивных биохимических систем (гистаминовых рецепторов). Они вытесняют гистамин из участков цитоплазмы, с которыми он связывается. В этих случаях лечебное действие обеспечивается их центральным антихолинергическим, седативным и противорвотным свойствами. В связи с этим все противогистаминные средства можно разделить на 2 группы: 1) средства, угнетающие ЦНС, для которых характерен седативный и снотворный эффект - “ночные” противогистаминные средства (димедрол, производные фенотиазина); 2) средства, стимулирующие ЦНС - “дневные” противогистаминные средства (перновин, диазолин).
Данные последних лет показывают, что существует два типа гистаминовых рецепторов. Возбуждение гистамином рецепторов Г1(Н1) вызывает сокращение гладкомышечных органов, в том числе кишок и бронхов. Эти рецепторы блокируются димедролом, дипразином и др.
Возбуждение гистамином рецепторов Г2 (Н2) стимулирует секрецию хлористоводородной кислоты слизистой оболочкой желудка, вызывает тахикардию у морских свинок и тормозит сокращение матки крысы. Эти рецепторы избирательно блокируются новыми синтетическими производными гистамина - циметидином и метиамидом. Блокаторы гистаминовых Н2-рецепторов лишены отрицательного действия.
Противогистаминные средства применяют в основном, с целью симптоматической терапии. Они показаны при заболеваниях, в патогенезе которых имеется аллергический компонент (крапивница, сенная лихорадка, аллергические осложнения лекарственной терапии) и патологические реакции организма на переливание крови и кровезамещающих жидкостей.
Кроме того, противогистаминные средства показаны: при бессоннице (димедрол и производные фенотиазина) и при лучевой болезни, эти средства эффективны при паркинсонизме, хорее, рвоте беременных, при вестибулярных расстройствах (болезнь Меньера), при морской и воздушной болезни. м-Холиноблокаторы применяют с целью профилактики бронхоспазма, при язвенной болезни желудка и двенадцатиперстной кишки, при кишечной, почечной и печеночной колике, при болезни Паркинсона, для расширения зрачка и профилактике укачивания.
4. КЛАССИФИКАЦИЯ ПРЕПАРАТОВ
Лекарственные средства, вызывающие рвоту, классифицируют в зависимости от локализации точек приложения их действия. По такому принципу они делятся на:
Средства центрального действия, стимулирующие ХРТЗ (апоморфин и др.).
Средства периферического действия (горчица, сульфат меди, рвотный камень и др.). Препараты вызывают рвоту рефлекторно в результате раздражения слизистой оболочки желудка. После перерезки блуждающего нерва рвота не возникает.
Средства как центрального так и периферического действия (ипекуана и др.).
Некоторые авторы делят рвотные и противорвотные препараты только на две группы:
препараты центрального и периферического действия [8].
Ещё в одном источнике предлагается следующая классификация лекарственных средств, эффективных при рвоте и тошноте [7]:
5. ТАБЛИЦА ПРЕПАРАТОВ
№
п/п
Структурная формула
Название и синонимы
Систематическое название
Методы получения
Анализ
Разное
1.
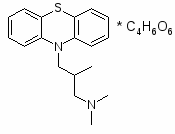
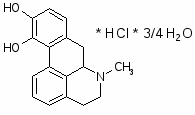
Апоморфин
6-methyl-5,6,6a,7-tetrahydro-4H-dibenzo[de,g]quinoline-10,11-diol
[10]
9],
10]
Впервые синтезирован в 1869 году
2.
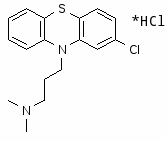
Аминазин (Largactil, Megaphen, Thorazine)
Гидрохлорид 2-хлор-10-(3-диметиламинопро
пил)-фенотиазина
11], 12]
13]
Впервые синтезирован во Франции. Первое сообщение о нём появилось в 1952 году.
3.
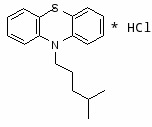
Алимемазин терален, alimezine, nedeltran, temaril.
10-(3-Диметиламино-2-метилпропил)-фенотиазина гидротартрат
4.
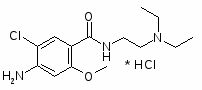
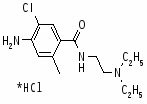
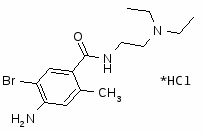
Бромоприд. Биморал, Ablex, Digesan, Modulan, Viadil, и др.
4-амино-5-бром-N-(2-N,N-диэтиламиноэтил)-2-метоксибензамид.
14]
5.
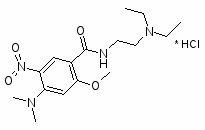
Димепрамид
5-нитро-4-диметиламино-2-метокси-N-(2-диэтиламиноэтил)-бензомида гидрохлорид.
6.
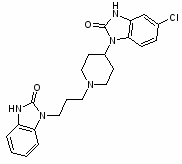
Домперидон мотилиум, домперон, cilroton, peridal.
5-хлор-1(1-(3-(2-оксо-1-бензимидазолинил)пропил)-4-пиперидил)-2-бензимидазолинон
7.
Метоклопрамид апо-метоклоп, гастросил, клометол, метпрамид.
4-амино-5-хлор-N-(2-диэтиламиноэтил)-2-метоксибензамида гидрохлорид.
15]
16], 17]
8.
CuSO4 * 5H2O
Меди сульфат
9.
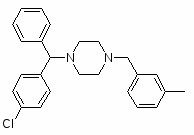
Меклозин, бонин
1 - ((4 - хлорфенил) фенилметил) 4 - ((3 - метилфенил)метил)
пиперазин
10.
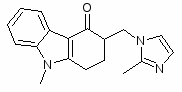
Ондансетрон зофран, латран.
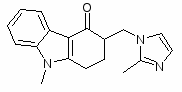
4Н-Карбазол-4-он, 1, 2, 3, 9 – тетрагидро – 9 - метил-3-(2-метил-1Н-имидазол-1-ил) метил
11.
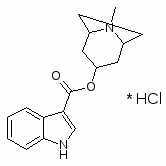
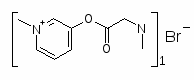
Пиридостигмина бромид, калимин 60 Н, калимин форте
3 - ((диметиламино) карбонил) окси) – 1 -метилпиридиния бромид
12.
13.
Скополамин, scopolaminum hydrobromicum, hyoscini hydrobromidum.
9-methyl-3-oxa-9-azatricyclo[3.3.1.02,4]non-7-yl 3-hydroxy-2-phenylpropanoate
18]
19]
Впервые синтезирован в 1988 году Э. Шмидтом.
Дигидрохлорид 2-трифторметил-10--(4-метилперазинил-1)-пропил-фентиазина
15.
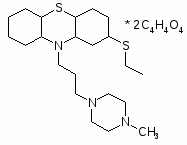
Тиэтилперазин торекан, торестен, трестен.
2-Этилтио-10-(3-(1-метилпиперазинил-4)-пропил)-фенотиазина дималеат
16.
Трописетрон навобан, тропиндол.
{(1αН, 5αН)-8-метил-8-азабицикло-(3,2,1)-окт-3α-иловый эфир} 1Н-индол-3-карбоновой кислоты гидрохлорид
17.
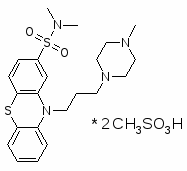
Тиопроперазин мажептил, cephalin, thioperazine, vontil.
2-Диметилсульфамидо-10-(3-(1-метилпиперазинил-4)-пропил)-фенотиазин
20.
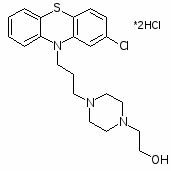
Флуфеназин, миренил
4-(3-(2-(трифторметил)-10Н-фенотиазин-10-ил)пропил)-1-пиперазинилэтанол
22.
Этаперазин, chlorpiprazin, fentazin, perphenazine, trilafon.
2-Хлор-10-{3-(1-(β-оксиэтил)-пиперазинил-4)-пропил}-фенатиазина дигидрохлорид
6. МЕТОДЫ ПОЛУЧЕНИЯ И АНАЛИЗА
9.
10.6.1. Получение и анализ метоклопрамида
4-амино-5-хлор-N-[2-(диэтиламино)этил]-2-метоксибензамида гидрохлорид
Метоклопрамид является специфическим блокатором дофаминовых (D2) рецепторов, а также серотониновых (5-HT3) рецепторов.
Препарат оказывает противорвотное действие, успокаивает икоту, и, кроме того, оказывает регулирующее влияние на функции желудочно-кишечного тракта: тонус и двигательная активность органов пищеварения усиливаются, а секреция желудка не меняется.
Применяют в качестве противорвотного средства при тошноте, рвоте, связанных с наркозом, лучевой терапией, побочным действием лекарств (препаратов наперстянки, цитостатиков, антибиотиков и др.), при рвоте беременных, при нарушениях диеты и др. На рвоту вестибулярного генеза метоклопрамид не действует.
Описание. Белый или почти белый кристаллический порошок без запаха или почти без запаха.
Растворимость. Очень легко растворим в воде; легко растворим в этаноле (~750 г/л) ИР; умеренно растворим в хлороформе Р; практически нерастворим в эфире Р.
Хранение. Метоклопрамида гидрохлорид следует хранить в хорошо укупоренной таре, предохраняющей от действия света.
ТРЕБОВАНИЯ
Общее требование. Метоклопрамида гидрохлорид содержит не менее 98,0 и не более 101,0% C14H22ClN3O2*HCl в пересчёте на безводное вещество.
Подлинность. Можно применять либо испытания А и Г, либо испытания Б, В и Г.
А. Проводят испытание в инфракрасной области спектра. Инфракрасный спектр соответствует спектру, полученному со стандартным образцом метоклопрамида гидрохлорида СО, или спектру сравнения метоклопрамида гидрохлорида.
Б. Спектр поглощения раствора испытуемого вещества в HCl (0,01 моль/л) ТР с концентрацией 20 мкг/мл при наблюдении между 230 и 350 нм даёт максимумы при длинах волн около 273 и 309 нм; поглощения в кювете с толщиной слоя 1 см при этих длинах волн составляют соответственно 0,79 и 0,69.
В. Растворяют 0,05 г испытуемого вещества в 5 мл воды и добавляют 5 мл 4-диметиламинобензальдегида ИР5; появляется жёлто-оранжевое окрашивание.
Г. Раствор испытуемого вещества с концентрацией 20 мг/мл даёт характерную для хлоридов реакцию.
Прозрачность и окраска раствора. Раствор 1,0 г испытуемого вещества в 10 мл свободной от диоксида углерода воде Р прозрачен и окрашен не более интенсивно, чем стандартный окрашенный раствор ЖлЗ.
Сульфатная зола. Не более 1,0 мг/г.
Вода. Проводят определение методом Карла Фишера, используя около 0,5 г испытуемого вещества; содержание воды не менее 45 и не более 55 мг/г.
PH раствора. PH раствора испытуемого вещества в свободной от диоксида углерода воде Р с концентрацией 0,10 г/мл составляет 4,5-6,5.
Посторонние примеси. Проводят испытание, используя в качестве сорбента силикагель Р4, а в качестве подвижной фазы смесь 95 объёмов 1-бутанола Р и 5 объёмов аммиака (~260 г/л) ИР. Наносят на пластинку отдельно по 5 мкл каждого из двух растворов в метаноле Р, содержащих (А) 50 мг испытуемого вещества в 1 мл и (Б) 0,50 мг испытуемого вещества в 1 мл. После извлечения пластинки из хроматографической камеры дают ей высохнуть на воздухе и оценивают хроматограмму в ультрафиолетовом свете (254 нм). Любое пятно, которое даёт раствор А, кроме основного пятна, не должно быть более интенсивным, чем пятно, которое даёт раствор Б.
Количественное определение. Растворяют около 0,3 г испытуемого вещества (точная навеска) в 80 мл уксусного ангидрида Р, добавляют 10 мл раствора ацетата ртути в уксусной кислоте ИР и титруют хлорной кислотой (0,1 моль/л) ТР, определяя конечное значение потенциометрическим методом. Каждый миллилитр хлорной кислоты (0,1 моль/л) ТР соответствует 33,63 мг C14H22ClN3O2*HCl.
ПОЛУЧЕНИЕ
1.Соединение формулы 2-MeO-4-H2N-5-ClC6H2CONHCH2CH2NEt2, обладающее противорвотным действием, получают хлорированием соединений формулы 2-MeO-4-H2NC6H3COOR (R=алкил) в положение 5, ацилированием реакционноспособными производными соединений формулы HOOC(CH2)nCOOH (n=0-2) и обработкой образующихся соединений формулы R1HNOC(CH2)COHNR2 [R1=2-Cl-4-(ROOC)-5-MeOC6H2] амином формулы H2NCH2CH2NEt2.
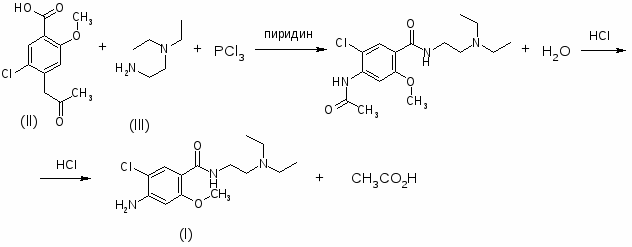
2. 2-Метокси-4-амино-5-хлор-N-(2-диэтиламиноэтил)-бензамид (I) получают реакцией 2-метокси-4-ацетиламино-5-хлорбензойной кислоты (II), H2NCH2CHNEt2 (III) и PCl3 в соотношении 1:1:0,63 при 60-90° в присутствии пиридина, полученный 2-метокси-4-ацетиламино-5-хлор-N-(2-диэтиламиноэтил)-бензамид извлекают толуолом и гидролизуют при кипячении с HCl (кислотой).
Пример. 20 г III в 350 мл абсолютного пиридина охлаждают до ~ 10°C, при 0° приливают 11,83 г PCl3, перемешивают при ~10°, прибавляют 35 г безводной II, перемешивают при нагревании до ~80°C и ~4 ч при 80-90°, отгоняют в вакууме пиридин, прибавляют 150 мл воды и продолжают отгонку остатка пиридина, прибавляют 70 мл воды и 200 мл толуола, при охлаждении подщелачивают 20%-ным NaOH до pH 9,5-10,0, разделяют слои, водный слой извлекают небольшим количеством толуола, органический слой и экстракт соединяют, промывают небольшим количеством воды, извлекают смесью 70 мл концентрированной HCl и 140 мл воды, солянокислый экстракт нагревают 1 ч при ~100°, обесцвечивают активированным углем при нагревании 10-15 мин при 100-102°, охлаждают до ~20°, устанавливают на pH 6,5-6,8, фильтруют, разбавляют водой, при охлаждении подщелачивают на фенолфталеин 20%-ным NaOH, осадок промывают, сушат, кристаллизуют из толуола, получают I, выход ~88%, tпл. 147-8°.
АНАЛИЗ
1. Фотометрический метод определения метоклопрамида (I) основан на описанной ранее реакции его с о-аминофенолом (II) или его N-замещёнными (N-бензил-, N-салицилил- или N,N-диметил-) производными и KIO3. К 15 мл глицинового буферного раствора (pH 1,7) прибавляют 1мл 0,05%-ного раствора (II) в спирте или в разбавленной HCl (pH 1,5), 1 мл 0,003 М раствора KIO3, вносят пробу раствора (I), разбавляют водой до 25 мл и измеряют ОП при 520 нм. Раствор I готовят, растворяя по 200 мг его в 0,5 мл спирта или 0,5 HCl и разбавляя водой до объёма 100 мл. По 5 мл приготовленных растворов разбавляют водой до 50 мл. Растворы подчиняются закону Бера в интервале концентраций I 250-1000 мкг в 25 мл. Метод пригоден для определения I в лекарственных формах.
2. Быстрое и простое определение метоклопрамида в плазме осуществляют методом ВЭЖХ после депротеинизации исследуемых проб при помощи MeCN, содержащего прокаинамид (внутренний стандарт). Анализ производят на Кл (25 см * 4,6 мм), содержащей Ультрасфер Si (5 мкм), в потоке 65%-ного водного раствора MeCN, содержащего 5 ммоль/л (NH4)H2PO4, (pH 7,0) при расходе ПФ 1 мл/мин и флуориметрическом детектировании (312/360 нм). ПрО равен 0,89 нг/мл, открываемость 99,6%.
3. Метоклопрамид [I, N-(диэтиламиноэтил)-2-метокси-4-амино-5-хлорбензамид] идентифицируют, определяя его спектры поглощения в ИК- и УФ-области [ (макс.) 278 и 308 м], реакцией диазотирования или реакцией осаждения с йодвисмутовым раствором, БХ в системе C4H9OH+CH3COOH+вода 100:5:30 (Rf пятна 0,55) или электрофорезом в 2н HCOOH (проявитель – в реактив Эрлиха). Количественное определение I, содержащего в своей молекуле алифатическую цепь и NH2-группу в ароматическом кольце, основано на ацетилировании I (CH3CO) и алкалиметрическом титровании ацетилпроизводного I в безводном растворителе.
4. Методика нитрометрического микроопределения ди-ХГ 2-метокси-5-хлорпрокаинамида (I примперан) в таблетках и инъекционных растворах с индикатором Na-солью N-нитрозодифениламиноазобензол-м (или п-)-сульфокислоты. 20 мг I смешивают с 5 мл 1н HCl, добавляют 5 мл воды, 0,2 г KBr и 1 каплю индикатора, затем титруют 0,01М раствором NaNO2 до перехода окраски раствора из фиолетовой в жёлтую (1 мл 0,01М раствора NaNO2 соответствует 0,00373 г I). Полученные результаты соответствуют данным потенциометрического анализа. Приведены результаты определения I в различных готовых лекарственных формах.
11.
12.6.2. Получение и анализ бромоприда и диметпрамида
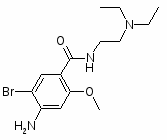
4-амино-5-бром-N-(2-N,N-диэтиламиноэтил)-2-метоксибензамид
Бромоприд по структуре и действию близок к метоклопрамиду. Химически отличается лишь наличием атома брома вместо хлора в положении 5 бензольного ядра.
По показаниям к применению также близок к метоклопрамиду.
Назначают главным образом при тошноте и рвоте, связанных с расстройствами желудочно-кишечного тракта (понижение тонуса желудка и кишечника, отрыжка, метеоризм и т.д.).
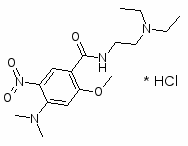
5-нитро-4-диметиламино-2-метокси-N-(2-диэтиламиноэтил)-бензамида гидрохлорид
Диметпрамид также по структуре и механизму действия близок к метоклопрамиду.
Применяют для предупреждения и купирования тошноты и рвоты в послеоперационном периоде, при лучевом лечении и химиотерапии онкологических больных и др.
Получение
1.Предложены обладающие успокаивающим действием соединения формулы 2-RO-4-R-5-RC6H2COR (I).
Пример. Смесь 40,2 г I (R=Me, R=NH2, R=Cl, R=OH) (Iа), 300 мл NEt3 и 23,2 г Et2NCH2CH2NH2 кипятят 8 ч, упаривают, добавляют 300 мл 10%-ного раствора NaOH, получают 54,5 г I [R=Me, R=NH2, R=Cl, R=Et2NCH2CH2NH (A)], выход 91%, т.пл. 145-7°; из маточного раствора после подкисления выделяют 2,5 г Iа, т.пл. 202-5°.
Аналогично получают I (R=Me, R=NH2, R=Br, R=A) с выходом 93,2%, т.пл. 134-6°.
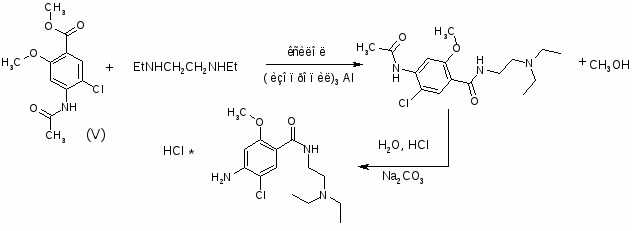
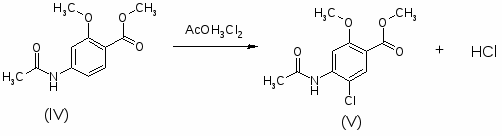
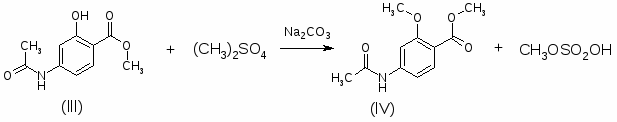
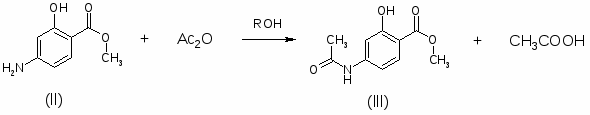
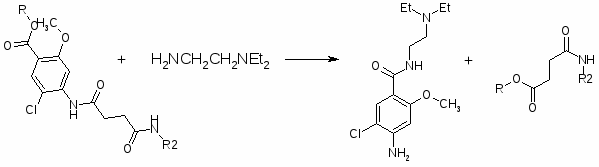
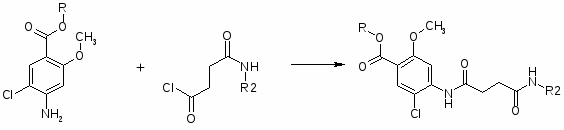
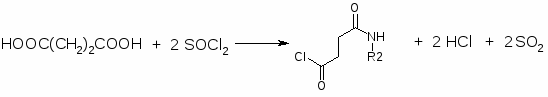
2. Соединения общей формулы 1-ZO-4-X-5-YC6H2CONH-(CH2)nNRR (R и R – C2H5; Z – CH3; X – NH2, N(CH3)2; Y – Cl, Br, NO2; n=2) получают исходя из п-аминосалициловой кислоты (I). I последовательно эстерифицируют, ацилируют по NH2-группе, алкилируют по OH-группе, вводят заместитель Y в 5-положение, обрабатывают H2N(CH2)NRR и гидролизуют. 883 г I и 970 г 93% -ной H2SO4 кипятят с 1875 г абсолютного MeOH 5-6 часов, охлаждают до 30°, выливают при перемешивании в раствор 975 г Na2CO3 в 12,5 л воды, отфильтровывают осадок, сушат при 60°С, получают МЭ I (II), выход 86%, т.пл. 119°. 361 г II ацилируют в 725 мл абсолютного спирта 225 г Ac2O при температуре >50°, разбавляют 7,5 л воды, перемешивают 1,5 часа, сушат при 55-60°, получают метил-п-ацетиламиносалицилат (III), выход 94%, т.пл. 152-3°. 427 г III растворяют при ~48° и перемешивают, в 1500 мл ацетона быстро прибавляют 276 г Na2CO3 и 277 г Me2SO4, нагревают до кипения, кипятят 15 часов, отгоняют 1200 мл ацетона, охлаждают до 50°, разбавляют 2500 мл воды, отфильтровывают осадок, сушат при 55-60°, получают метил-2-метокси-4-ацетил-аминобензоат (IV), выход 78%, т.пл.127°. 348 г IV в 1800 мл AcOH нагревают до 30°, пропускают Cl2 при 15-20° до привеса на 112 г, выливают в 19 л воды, выдерживают 1 час, центрифугируют, отмывают осадок от Cl¯, сушат при 60°, получают метил-2-метокси-4-ацетиламино-5-хлор-бензоат (V), выход 86%, т.пл. 153°. К 345 г V, 670 мл ксилола и 156 г EtNHCH2CH2NHEt прибавляют 67 г (изо-Pr)3Al, осторожно нагревая до кипения и отгоняя дистиллят через колонку (высота 30 см), после отгонки MeOH и части ксилола (4 часа) охлаждают, прибавляют 1600 мл воды и 400 мл концентрированной HCl, фильтруют, отделяют водный слой, прибавляют 600 мл 30%-ной Na2CO3, отфильтровывают N-(диэтиламиноэтил)-2-метокси-4-ацетиламино-5-хлорбензамид, кипятят с 1340 мл концентрированной HCl и 2200 мл воды 1,5 часа и ещё 10 мин с 2-3 г активированного угля, фильтруют, из фильтрата действием Na2CO3 выделяют N-(диэтиламиноэтил)-2-метокси-4-амино-5-хлорбензамид, выход 65%, т.пл. 144°, т.пл. ди-ХГ 136-7°.
13.
14.6.3. Получение и анализ ондансетрона
4H-Карбазол-4-он,1,2,3,9-тетрагидро-9-метил-3-[(2-метил-1H-имидазол-1-ил) метил]
Использование известных антиэметиков, таких, как антагонисты допамина (метоклопрамид), кортикостероиды, лоразепам и их комбинации, оказывает определённое противорвотное действие, но вызывает ряд побочных явлений, в том числе экстрапирамидные рсстройства, характерные для метоклопрамида. Создание новых противоопухолевых препаратов из группы антагонистов рецепторов серотонина третьего типа (5HT3) было результатом направленного поиска активных антиэметиков для больных, получающих цитостатическую терапию.
Тошнота и рвота, возникающие в процессе цитостатической терапии, связаны с выбросом серотонина (5HT) из энтерохромаффиноподобных клеток слизистой оболочки тонкого кишечника. 5HT вызывает рвотный рефлекс и ощущение тошноты через активацию афферентных волокон блуждающего нерва. Это в свою очередь вызывает освобождение серотонина в area postrema, расположенной в области дна IV желудочка головного мозга. Эта богатая рецепторами серотонина формация подвержена и прямому воздействию цитостатиков, поступающих сюда с кровью. Эффект препаратов из группы антагонистов рецепторов 5HT3 по предупреждению тошноты и рвоты, вызываемых цитостатиками и облучением, связан с блокадой этих рецепторов на уровне нейронов как периферической, так и центральной нервной системы.
Клиническое применение получили три препарата группы антагонистов 5HT3 – зофран (ондансетрон), навобан (трописетрон) и китрил (гранисетрон). Использование этих антиэметиков существенно расширило возможности применения высокоэметогенных цитостатиков, в первую очередь производных платины, позволив предупредить или значительно уменьшить тошноту и рвоту у 70-80% больных.
Несмотря на близкий механизм действия, различные препараты группы антагонистов рецепторов 5HT3 (зофран, навобан, китрил) отличается по своим фармакокинетическим характеристикам и в связи с этим по оптимальному режиму их применения.
Препарат зофран (ондансетрон) фирмы “Glaxo” в настоящее время широко используется как антиэметогенный компонент противоопухолевой химиотерапии. В ряде рандомизированных многоцентровых исследований на репрезентативных группах больных была убедительно показана как значительно большая, чем у метоклопрамида, эффективность препарата, так и его лучшая переносимость, в частности полное отсутствие серьёзных побочных действий, таких, как нередкие при применении метоклопрамида экстрапирамидные расстройства. Так, по сводным данным литературы, эффективность зофрана по купированию рвоты составляет 65-86%, а метоклопрамида – 41-64%. Экстрапирамидные расстройства наблюдались у 18-19% больных, применявших метоклопрамид, и не отмечены при использовании зофрана.
В нашей стране зофран зарегистрирован в конце 1992г. В настоящее время он уже применяется в ряде клиник при проведении противоопухолевой химиотерапии.
СЛОВАРЬ ТЕРМИНОВ
Блуждающий
нерв –
десятая пара черепных нервов у позвоночных животных и человека. Иннервирует органы головы, шеи, грудной и брюшной полостей. Участвуют в регуляции рефлекторных актов.
Болезнь Меньера –
болезненное состояние, обусловленное действием но организм экзогенных токсинов (например, микробных) или вредных веществ эндогенного происхождения (например, при токсикозе беременных.
Булимия –
неутолимый голод, сопровождающийся слабостью, болью в подложечной области; наблюдается при эндокринных и некоторых других заболеваниях.
Ваготомия –
пересечение блуждающих нервов.
Гематоэнцефали-
ческий барьер –
комплексный физиологический механизм, находится в ЦНС на границе между кровью и нервной тканью.
Гипертензия –
повышение гидростатического давления в сосудах, полых органах или полостях организма.
Интероцепторы –
чувствительные нервные окончания, воспринимающие раздражения из внутренней среды организма, рассеяны во внутренних органах и кровеносных сосудах.
Медиаторы –
химические вещества, молекулы которых способны реагировать со специфическими рецепторами клеточной мембраны и изменять её проницаемость для определённых ионов, вызывая возникновения потенциала действия.
Перистальтика –
волнообразное сокращение стенок полых трубчатых органов (кишок, желудка и др.), способствующие продвижению их содержимого к выходным отверстиям.
Пилорической
части –
трубчатые железы в слизистой оболочке желудка, расположенные в области перехода желудка в двенадцатиперстную кишку.
Продромальный период –
стадия предвестников болезни – появление её не специфических признаков.
Секреция –
образование и выделение железистыми клетками особых продуктов – секретов, необходимых для жизнедеятельности организма.
Спазмолитики –
лекарственные вещества, снимающие спазмы гладкой мускулатуры внутренних органов и др.
Хеморецепторы –
чувствительные нервные окончания, воспринимающие химические раздражения.
Цитостатики –
лекарственные вещества, блокирующие деление клеток, подавляющие реакции иммунитета.
Экстрапирамидная система –
совокупность структур, расположенных в больших полушариях и стволе головного мозга, участвующих в управлении движениями, регуляции мышечного тонуса, эмоциональных проявлениях (смех, плач).
Этиология –
учение о причинах болезни.
ЛИТЕРАТУРА
1. Машковский М. Д. Лекарственные средства: В 2-х томах. М.: Медицина 1997.
2. Машковский М. Д. Лекарства века. – М.: ООО “Издательство Новая Волна” 1998. – 320 с.
3. Популярная медицинская энциклопедия. Глав. Ред. Ф. Н. Петров, А. Ф. Серенко. М., “Сов. Энциклопедия”, 1968.
4. Аничков С.В., Беленький П.Н. Учебник фармакологии,— МЕДГИЗ Ленинградское отделение, 1955г.
5. Батрак Г.Е. Фармакология, Киев, "Вища школа",1980, с. 320
6. Фармакология, Харкевич Д.А.— Москва «Медицина», 1981г., стр.246-249
7. Клиническая фармакология, т.2, Лоуренс Д.Р., Бенитт П.Н.— Москва «Медицина», 1993г.,стр.496-505
8. Фармакология, Кудрин А.Н.— Москва «Медицина»,1991г.
9. Новый колориметрический метод определения хлоргидрата апоморфина в инъекционных растворе. Тончева п., Клоушева А., "Фармация", 1962, 12, №4, с.10-14
10. Новый спектрофотометрический микрометод определения апоморфина. Clenrum Desigan “Z. Analyt. Chem.”, 1969, 248, №3-4, 179-180
11. Рубцов М.В., Байчиков А.Г. Синтетические химико-фармацевтические препараты, Москва, Медицина,1971, 328 с.
12. Способ выделения аминазина. Ярыгина Т.И., Москаленко Р.И., Яковлева Л.Ф., Савельева Г.И., Кудымов Г.И., Шмаков Н.М. [Перм. фармац. ин-т]. Авт. св. СССР, кл. С07д 93/14, №487890
13. Государственная Фармакопея: Х издание, Москва, Медицина, 1968, 1040 с.
14. Способ получения производных бензамидов Мори Хироси, Сибута Татэо. [Тейкоку дзоки Сейяку к.к.], япон. пат. кл. 16С624, (С07с 103/82), №49-7150
15. Способ получения -(- диэтиламиноэтил)-2-метокси-4-амино-5-хлорбензамида. Лернер О.М., Рачинский Ф.Ю., Авт. Св.СССР, кл.12о.16, (С07с), №249367
16. Халецкий А.М. «Фармацевтическая химия», Ленинград, Медицина, 1966, 764с.
17. Флуоресцентные свойства метоклопромида и его определение в готовых лекарственных формах. Balyens W., Moerloose P. “Analyst”, 1978, 103, №1225, 359-367
18. Метод получения скополамина из травы индийского татула. А.Н. Бабец, «Фармация», 1963, 8, №6, с.23-34
19. Количественный микроанализ производных тропана с помощью йодмонохлорида на основе полийодной реакции. Супрун П.П. «Фармация респ. межвед. сб.», 1975, вып.2, 63-66

Нравится материал? Поддержи автора!
Ещё документы из категории медицина, здоровье:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ