Зависящие от времени процессы в ядерном магнитном резонансе
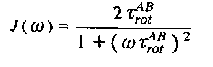
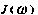
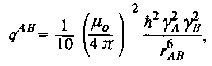
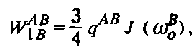
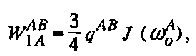
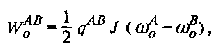
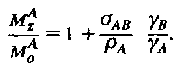
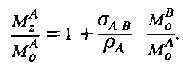
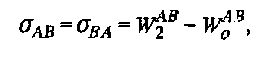
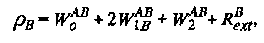
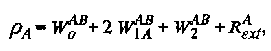
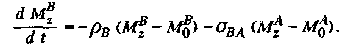
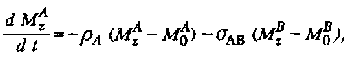
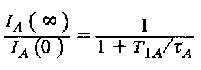
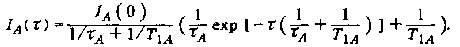
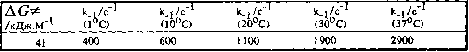
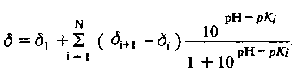
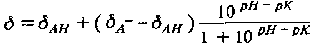
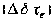
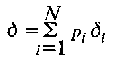
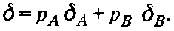
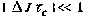
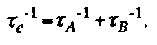
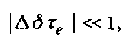
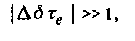
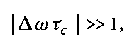
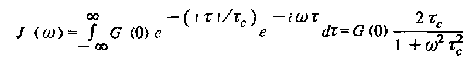
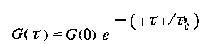
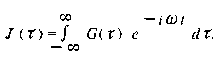
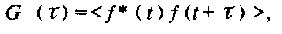

Реферат
на тему:
«Зависящие от времени процессы в ЯМР»
Введение
Процессы спиновой релаксации за счет модуляции во времени различных взаимодействий – характерный, но далеко не единственный пример явлений, которые могут быть изучены методом ЯМР. Эти процессы в шкале времени ЯМР часто характеризуются либо очень малыми, либо очень большими временами. Понятие шкалы времени основано на простой концепции, которая находит применение во многих областях. Если речь идет о медленном процессе, то предполагается, что он может быть описан последовательно, на каждом из этапов. При рассмотрении быстрого процесса предполагается, что наблюдаем за неким усредненным поведением системы. Здесь необходимо сразу же пояснить, что понятие медленных и быстрых процессов вводится лишь тогда, когда приводится шкала времени, в которой проводится рассмотрение.
Простейший путь состоит в том, чтобы задать предельные значения времен, и в этом случае все физические явления описывать как быстрые или медленные по сравнению с этими значениями. Очевидно, что времена, задающие масштаб, зависят также и от того, какие физические процессы описываются в данном приближении. При этом существует не одна временная шкала ЯМР, а множество различных шкал в зависимости от типа рассматриваемых взаимодействий. С теоретической точки зрения наиболее сложной для обсуждения является промежуточная область, в которой не реализуются при предельных случаях: быстрых и медленных процессов. Независимо от используемой шкалы ЯМР физические процессы, связанные с различными движениями, обладают своей собственной шкалой времени, которая может быть описана временами корреляции или характеристическими частотами. В табл. представлены типичные интервалы частот для основных молекулярных движений: от очень медленных – с характеристическими временами от нескольких минут до нескольких часов до очень быстрых – в пикосекундной области.
Существуют разнообразные резонансные методы, позволяющие регистрировать процессы, протекающие с характерными временами до 10 нc. Только такие сверхбыстрые процессы, как торсионные и вибрационные движения атомов, не поддаются прямому наблюдению с помощью методов ЯМР. Кроме того существуют макроскопические движения: потоки жидкостей и мышечные сокращения. Эти процессы играют второстепенную роль в спектроскопии in-vitro, ориентированной на биохимические проблемы, однако в ЯМР-томографии и в in-vivo-спектроскопии роль таких процессов достаточно велика. Таким образом, характерные времена процессов, регистрируемых с помощью ЯМР, попадают в широкую область, охватывающую несколько порядков на временной шкале, при этом каждый из ЯМР-экспериментов характеризуется определенной временной областью, которая соответствует исследуемым процессам.
1. Временная корреляция и спектральная плотность
Молекулярные движения в жидкостях, например, вращения боковых цепей, не описываются определенными частотами на больших временных интервалах: мгновенная скорость вращения может варьироваться от одной боковой цепи к другой и от молекулы к молекуле, а за счет соударений с молекулами растворителя скорость вращения может изменяться как по величине, так и по направлению. Это означает, что молекулярные движения обладают широким спектром частот, который также присущ флуктуирующим магнитным полям, возникающим в результате движения атомов и молекул и ответственным за релаксационные процессы в спиновой системе.
Так как в растворе большое число одинаковых молекул находится в состояниях, характеризуемых разнообразными движениями, то при вычислении тех или иных величин проводят усреднение по ансамблю молекул, а также по большому промежутку времени. Поведение во времени какой-либо случайной величины f(Я), например, флуктуирующего магнитного поля, обычно описывают с помощью корреляционной функции
где угловые скобки означают усреднение по ансамблю, а черта – усреднение по времени. Усреднение по всем значениям времени t применимо при описании стационарного состояния, для которого с точки зрения статистики не имеет значения, относительно какого момента времени определена корреляционная функция. Для случайных процессов таких, например, как движение молекул в состоянии термодинамического равновесия, корреляционная функция максимальна для ф = 0 и убывает во времени. Для больших ф она должна стремиться к нулю, так как по определению для случайных процессов корреляции должны уменьшаться при условии, что наблюдение за системой ведется в течение достаточно длительного времени. Ширина корреляционной функции обычно описывается параметром, называемым временем корреляции Tc. Эта величина характеризует определенный вид движения и является мерой того, на каком временном интервале значения случайной величины еще можно рассматривать как коррелированные отлична от нуля.
Фурье - образ корреляционной функций Gi ф) называют спектральной плотностью J:
Точное значение времени корреляции и само определение этого параметра зависит от соответствующей корреляционной функции G, вид которой определяется конкретным физическим процессом. Во многих случаях корреляционную функцию можно достаточно хорошо описать экспонентой
Соответствующая спектральная плотность J, которую можно получить фурье - преобразованием этой корреляционной функции, имеет лоренцеву форму:
Для случая диффузии время корреляции обычно легко поддается интерпретации. Это среднее время между двумя соударениями данной молекулы с другими молекулами. Полуширина лоренцевой функции, как видно из, равна 1 /Tc. Таким образом, уменьшение времени корреляции, очевидно, расширяет спектральную область, на которой спектральная плотность отлична от нуля. Площадь под лоренцевой кривой постоянна и не зависит от времени корреляции.
Время корреляции Tc служит характерным параметром для проведения сравнений в шкале времени ЯМР, о которой речь шла ранее. Сама шкала времени определяется максимальной величиной взаимодействия Д. Процесс, характеризуемый временем корреляции Tc, является медленным, если
и соответственно быстрым, если Ао) Тс
2. Химический обмен
Химический обмен – один из наиболее наглядных примеров динамических процессов. Сущность этого явления ясна из интуитивных соображений. Под химическим обменом в общем случае понимают процессы, в которых спин ядра в процессе релаксации может находиться в состояниях, характеризуемых различным химическим окружением, что соответствует различным параметрам ЯМР. В основе изменения окружения ядерного спина может лежать внутримолекулярный процесс, такой, например, как изменение конформации, или же межмолекулярный процесс. Здесь можно рассматривать исследуемое ядро в новой ковалентной структуре или же, наоборот, включать в рассмотрение межмолекулярные взаимодействия тех молекул, которые содержат данное ядро, и таким образом учитывать изменение окружения данного ядра. В простейшем случае имеется только два различных состояния, которые отличаются по химическому сдвигу д. Время корреляции Tc здесь представлено временами жизни Ta и Tb в состояниях AwB соотвественно, а величина Д О) непосредственно определяется разностью химических сдвигов Д д = дВ – дА, измеренной в единицах частоты. В этом случае медленный обмен определяется неравенством
а быстрый обмен -
где
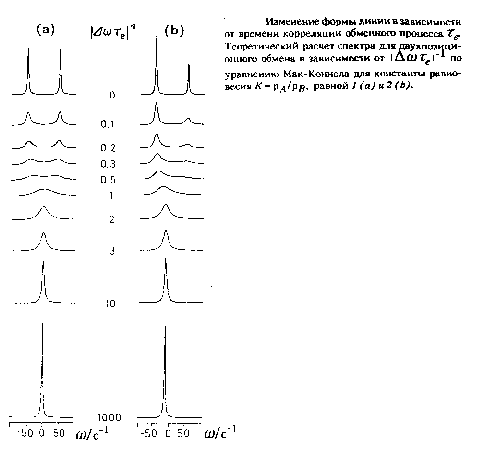
Соответствующие спектры ЯМР могут быть достаточно хорошо описаны обобщенными уравнениями Блоха, полученными в работе Мак-Коннела. Оба предельных случая: быстрого и медленного обмена, можно объяснить без привлечения серьезных расчетов, а чисто из интуитивных соображений путем предельных переходов Xe ~*0 и соответственно Xe ~* °°. В первом случае можно наблюдать лишь одну линию, так как ядро участвует в бесконечно быстром обмене между двумя состояниями с различным химическим окружением. Во втором случае можно наблюдать две резонансные линии с химическими сдвигами Oa и Ob, интенсивности которых прямо пропорциональны относительным заселенностям рл и рв, т.е. в данном случае обмен вообще отсутствует. Усреднение положений резонансных линий при быстром обмене приводит к химическому сдвигу
Для описания поведения в промежуточной области такое простое соотношение отсутствует, однако можно вычислить в явном виде положение сигнала ЯМР как функцию времени корреляции обменного процесса Te. Условия медленного обмена приводят к уширению обеих линий, а при ускорении обмена – к слиянию их в одну уширенную линию при выполнении условия I Aoxe \ ~ 1. При дальнейшем возрастании скорости обмена линия будет сужаться до тех пор, пока ее ширина не станет равной ширине линии в отсутствие обмена.
Аналогичный процесс усреднения происходит и в случае других взаимодействий. Если окружения, соответствующие двум состояниям Л и В, различаются только константами косвенного спин-спинового взаимодействия Ja и Jb, то наблюдается мультиплет с усредненной константой J' =pAJA+pBJBjs, oTex пор, пока для величины Al = JА – Jгв выполняется неравенство
Так как константы взаимодействия J, как правило, не коррелируют с разностью химических сдвигов, то в ряде случаев на основе этих констант должна быть установлена шкала времени, отличная от шкалы химических сдвигов. При наличии в спиновой системе взаимодействия, например косвенного спин-спинового, химический обмен не поддается описанию с помощью простых уравнений Мак-Коннела. Однако принципиально возможно описание поведения такой системы с привлечением квантово-механических подходов.
Какую биохимическую информацию можно извлечь из изучения процессов, связанных с химическим обменом? В области быстрого обмена в принципе можно рассчитать населенности отдельных состояний при условии наличия некоторой дополнительной информации. При этом наиболее важной является информация о числе состояний, участвующих в быстром обмене, так как это число присутствует в расчетной формуле в качестве параметра.
Для описания быстрого обмена между N состояниями следует обобщить уравнение на случай N состояний:
с учетом того, что в уравнении необходимо экспериментально определить значения <5 и в случае, когда населенность второго партнера будет существенно большей. В общем случае в расчет следует включить еще сведения о функциональной зависимости. Если найдено, что в реальном случае спектр ЯМР позволяет наблюдать случай быстрого обмена, то отсюда непосредственно следует, что время корреляции процесса обмена Xe меньше чем 1/1 Ад I.
В случае медленного обмена спектр будет более информативным. Наименьшее число различных состояний можно вычислить из числа резонансных линий, а соответствующие значения населенностей можно непосредственно получить из величины интеграла для каждой резонансной линии. Это позволяет зафиксировать с помощью ЯМР различные состояния, которые ранее удавалось зафиксировать только косвенно, например, с привлечением кинетических методов. Кроме того, здесь можно получить ограничение на значение времени корреляции обмена Xe: это значение должно быть больше чем 1 / I Д ь I. В промежуточной области вблизи– 1 обмен вызывает существенные изменения формы линии. Это позволяет путем построения теоретического спектра достаточно точно определять значения времени корреляции обменных процессов Tx в различных состояниях X. В области умеренно медленного обмена между экспериментально наблюдаемыми значениями времени поперечной релаксации Тц1, времени релаксации Tix в отсутствие обмена вместе с уравнением дает модифицированное уравнение Хендерсона-Хассельбалха
Если измерить зависимость химического сдвига от рН и описать эту зависимость с помощью уравнения, подбирая рК, то непосредственно из ЯМР-экспериментов удается получить значения р / С для индивидуальных групп. Это особенно важно, если речь идет, например, о спектрах 1H протеинов, поскольку данный метод достаточно точно позволяет определить значения рК каждого заряженного остатка.
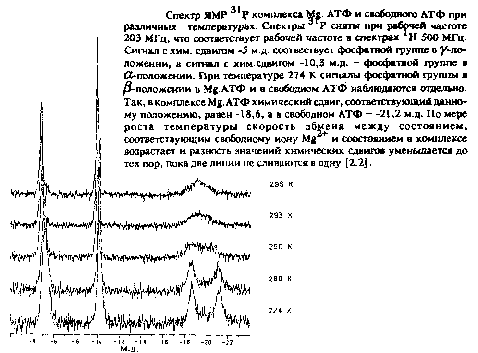
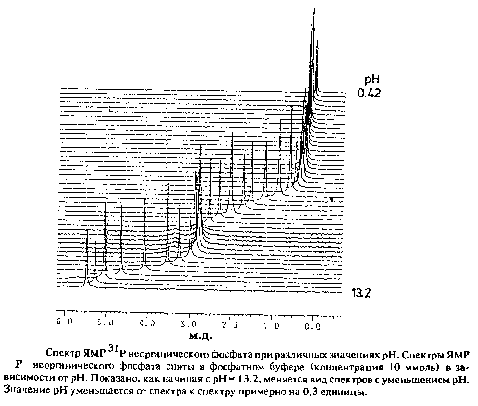
Неорганический фосфат принимает участие во многих ферментативных реакциях, поскольку он либо переносится на субстрат, либо расщепляется. Кроме того, неорганический фосфат принимает на себя функцию буфера. Для фосфатной группы существуют кроме двух различных протонированных форм в равновесии еще и следующие формы: Н3РО4, H2PO4», HPO42», PO43». При измерении спектров ЯМР 1P для различных значений рН мы всякий раз наблюдаем один сигнал, химический сдвиг которого изменяется в зависимости от концентрации ионов гидроксония. Такой вид спектра полностью соответствует случаю быстрого обмена.
Если по одной из осей отложить значение химического сдвига, а по другой рН, то можно построить кривую титрования, состоящую из четырех интервалов. Отсюда следует, что вещество, участвующее в данном процессе быстрого обмена, существует по крайней мере в четырех различных формах, которые характеризуются значениями химических сдвигов Oi, д2, O3 и д4, что полностью соответствует предположениям о четырех состояниях протонирования неорганического фосфата, полученным из химического подхода.
В данном случае функциональная зависимость является несколько более сложной, чем описываемая уравнением, так как здесь для описания равновесия необходимо использовать более одного значения рК. Используя закон действующих масс, можно расширить уравнение на N значений pKj Если кооперативные эффекты отсутствуют, то для N значений рК; можно просто записать сумму
Если значения с K1 существенно отличаются друг от друга, как это имеет место на рис. 2.8, то вблизи каждого из значений с Ki можно достаточно точно построить значения химических сдвигов, используя простое уравнение. Этот метод применяется достаточно часто, если необходимо построить какой-либо из участков кривой титрования.
4. Образование комплексов с диамагнитными лигандами
Комплексообразование молекул с диамагнитными лигандами подчиняется тем же правилам, что и процесс протонирования, зависящий от значения рН. Однако скорости обмена часто настолько малы, что условие быстрого обмена не выполняется. Интересными с точки зрения биологических приложений являются комплексы с ионами металлов, которые играют роль катализаторов в большинстве ферментативных превращений. Особенно часто встречаются комплексы двухвалентных металлов таких, как магний и кальций. Основным веществом в биологических реакциях является адено-зин 5 трифосфат, образующий в физиологических условиях комплекс с ионом Mg.
Устойчивость Mg.ATO-KOMiDieKca зависит от температуры. В больших магнитных полях переход от медленного к быстрому обмену происходит примерно при 25°С. При низких температурах можно отдельно наблюдать сигналы от Mg.ATO и свободного АТФ. При повышении температуры наблюдается усредненная резонансная линия, положение которой зависит от концентрации реагентов.
Анализ формы линии позволяет достаточно точно найти значение скорости обмена и энергии активации, которые определяются используемой буферной системой. В отличие от этого комплекса время жизни комплекса с кальцием настолько мало, что при самых сильных магнитных полях выше точки замерзания воды реализуется случай почти быстрого обмена.
Таблица 2.5. Значения энергий активации и скоростей обмена в комплексе М.АТФ
Скорость обмена k_ j -1 /Tfi и энергии активации Д Cj^ сильно зависят от значения рН раствора и от типа ионов, содержащихся в этом растворе. Приведенные в табл. значения вычислены из спектров, показанных на рис. 2.9.
Во многих реакциях ферментативного превращения Mg БФЦ сам является субстратом, поэтому ферментативная активность, прежде всего, определяется концентрацией свободного Mg.ATO. Это значение концентрации можно непосредственно определить по спектрам ЯМР из интенсивности соответствующих резонансных линий при понижении температуры. При более высоких температурах можно косвенно судить о концентрациях по химическому сдвигу, если известна константа связывания АТФ с магнием в данных экспериментальных условиях.
5. Перенос поляризации с насыщением
В области медленного обмена используется метод, основанный на переносе поляризации с насыщением. С помощью этого метода часто удается провести более точное и однозначное определение времен корреляции обменных процессов по сравнению с данными, получаемыми из анализа формы линии. Кроме того, метод переноса поляризации с насыщением позволяет получить дополнительную информацию о том, действительно ли две наблюдаемые в спектре резонансные линии соответствуют двум состояниям, между которыми осуществляется обмен. Реализация этого метода достаточно проста. С помощью импульса длительностью ф, воздействующего селективно, т.е. на определенной частоте, проводится насыщение линии В и измерение обычного спектра ЯМР. Этот эксперимент является примером использования метода селективного насыщения для подавления пика растворителя.
Пусть в момент времени ф положение спина, резонансная линия которого подлежит насыщению, изменится и осуществится переход из положения В в положение А. В этом случае интенсивность резонансной линии, соответствующей положению А, уменьшится. Эффективность этого метода, с одной стороны, определяется длительностью интервала ф, в течение которого осуществляется обмен, и скоростью обмена в системе 1/ ХА. С другой стороны, эффект уменьшается по мере установления равновесного распределения Больцмана, которое характеризуется временем продольной релаксации Ti А. Формально интенсивность Ia резонансной линии А в зависимости от времени ф, в течение которого проводится насыщение резонансной линии В, описывается следующим выражением:
Для времени насыщения при условии, что оно существенно больше значения Т}А, устанавливается состояние равновесия и отношение интенсивностей линий при наличии или отсутствии насыщения дается формулой
Существует еще одна возможность пометить спин В. Эта возможность может быть реализована посредством инверсии намагниченности, соответствующей спину В, селективным 180°-ным импульсом. При этом эффект воздействия на состояние спина ядра А может быть обнаружен с помощью неселективного детектирующего импульса, который подается на спиновую систему спустя время ф. В этом эксперименте с ростом ф прежде всего уменьшается интенсивность сигнала от ядра А до значения, соответствующего минимальному, а затем возрастает вновь до величины, соответствующей значению для невозмущенной системы.
Источниками погрешностей, которые могут вызывать неверную интерпретацию результатов, является ограниченная селективность инвертирующих и насыщающих импульсов, которые могут искажать соседние линии, а также вызывать ядерный эффект Оверхаузера, неявным образом влияющий на интенсивность резонансных линий, в частности, на сигнал А.
6. Ядерный эффект Оверхаузера
Изменение интенсивности сигнала в спектрах ЯМР за счет насыщения соответствующих резонансных состояний спина электрона впервые было обнаружено А.В. Оверхаузером. Впоследствии это явление было названо эффектом Оверхаузера. Перенос принципов этого эксперимента на систему двух спинов, связанных между собой диполь-дипольным взаимодействием, является основой для определения пространственной структуры методом ЯМР. Эффект Оверхаузера и ядерный эффект Оверхаузера основаны на изменении поляризации, наблюдающейся в связанной системе при условии изменения населенности одной или нескольких подсистем. Так как диполь-дипольное взаимодействие, определяющее изменение населенностей, зависит от расстояния между взаимодействующими спинами, то величина ЯЭО также зависит от расстояния между ними. Эта зависимость позволяет определить соответствующие межатомные расстояния.
Экспериментальные методы, с помощью которых наблюдается ЯЭО, подобны методам, используемым для определения скоростей обмена в случаях переноса поляризации с насыщением или инвероного переноса поляризации. В данном контексте эти методы известны, как TOE и переходный ЯЭО. Кроме того ЯЭО измеряется в двумерных ЯМР-экспериментах, которые могут быть использованы для определения скоростей химического обмена.
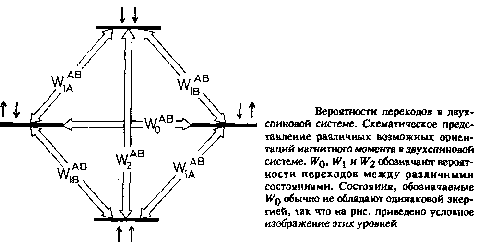
Простейшей системой, позволяющей достаточно наглядно продемонстрировать ЯЭО, является молекула, в которую входят два спина А и В, связанные диполь-дипольным взаимодействием, причем Ia = Ib – 1/2. Если провести усреднение по большому числу таких молекул, то каждой молекуле можно поставить в соответствие 4 возможных состояния, характеризуемых определенными населенностями, т.е. установить, с какой вероятностью населено каждое из состояний. В состоянии термодинамического равновесия имеет место распределение Больцмана. Если нужно изменить населенности, облучая спиновую систему на частоте, соответствующей резонансной частоте ws спина В, то вследствие диполь-дипольного взаимодействия произойдет изменение населенностей всех спиновых состояний. При условии, что облучение проводится в течение длительного времени, в системе установится новое стационарное состояние. Возникающие при этом релаксационные процессы можно в зависимости от изменения суммарного квантового числа m ядер А и В обозначить как нульквантовые, одноквантовые и двухквантовые.
Изменения населенностей приводят также к изменению ж-компоненты
Ma намагниченности спина А, величину которой к моменту времени t можно определить с помощью 90°-ного импульса. После фурье-преобразования найдем изменение интенсивности соответствующей резонансной линии на частоте wA.
Эти изменения намагниченности во времени можно описать с помощью дифференциальных уравнений
В этих уравнениях рА и рв обозначают скорости спин-решеточной релаксации ядер А и В, Oab – скорость релаксации, описывающая обмен между ядрами А и В, M0 – намагниченность в состоянии термодинамического равновесия. Скорости релаксации определяются следующим образом:
где W0, W\ и Wi – вероятности нуль-, одно- и двухквантовых переходов, а RaQ обозначает дополнительные каналы релаксации для спинов А и В.
Ядерный эффект Оверхаузера измеряется отношением интенсивности сигнала S после возбуждения к интенсивности сигнала S0 в отсутствие возбуждения или отношениемMzM0, поскольку интенсивность сигнала пропорциональна величине ж-компоненты намагниченности. Если в течение времени X, которое существенно больше времени продольной релаксации системы, на систему воздействует РЧ импульс на частоте, то это приведет к тому, что в стационарном состоянии MZB, dMz /dtn dMz Idt в и обратятся в нуль. Простым преобразованием и подстановкой для оценки ЯЭО в стационарном состоянии получим
Так как равновесная намагниченность пропорциональна гиромагнитному отношению у, то можно переписать в виде
Вероятности переходов для продольной релаксации даются следующими формулами:
Если движение, влияющее на релаксационные процессы, изотропно, как, например, вращательная диффузия, то коэффициент Qab, который пропорционален интенсивности взаимодействия, имеет вид
где мп – магнитная проницаемость вакуума, гав – расстояние между спинами A Ь В.
Соответствующая функция спектральной плотности .. есть
Если подставить эту функцию в выражение для с и получим максимальное усиление сигнала в 2,988 раза, если проведем насыщение по протону, непосредственно связанному с углеродом. Это увеличение чувствительности является дополнительным, поскольку при измерении спектров ЯМР 13C обычно используется широкополосная развязка. Правда, необходимо помнить, что ЯЭО не всегда приводит к увеличению интенсивности. Ядра 15N и 29Si имеют отрицательное гиромагнитное отношение, и ЯЭО приводит к уменьшению сигнала.
Если внешняя релаксация отлична от нуля, то стационарный ЯЭО зависит от расстояния между спинами, и его можно использовать для определения этого расстояния.
Однако для количественного определения расстояний необходимо дополнительное рассмотрение эффекта с учетом внешней релаксации.
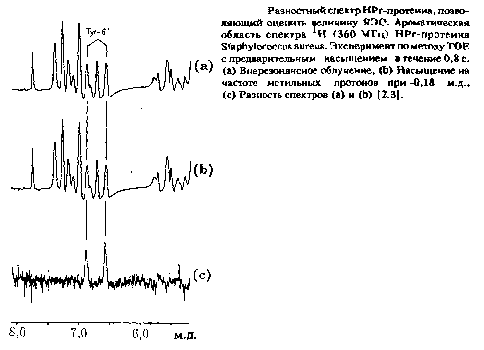
Межатомные расстояния можно определить более точно, если проследить за временной зависимостью ЯЭО. На рис. 2.12 показано влияние переноса поляризации с насыщением между метильной группой и ароматическим кольцом в HPr протеине, который является компонентой фосфоенолпируватзависимой системы фосфотрансферазы. Влияние насыщающего импульса, который подается на частоте 0) в, можно лучше всего оценить количественно, если кроме спектра в режиме предварительного насыщения на частоте Шв снять также исходный спектр в режиме предварительного насыщения на частоте Шв, т.е. спектр, в котором резонансная линия на частоте Шв отсутствует. Разностный спектр позволяет селективно оценить эффект Оверхаузера. Величина наблюдаемых эффектов часто может составлять несколько процентов, т.е. относительно мала. Для получения хорошего значения отношения сигнал/шум необходимо провести большое число накоплений. Небольшие нестабильности в работе прибора могут вносить искажения в разностную картину, и часто именно этим объясняется необходимость построения циклического эксперимента, причем попероменно проводится, например, 16 экспериментов в режимах on-resonance и off-resonance, а соответствующие спады свободной индукции накапливаются отдельно. С помощью этого метода можно наблюдать на современном спектрометре ЯЭО величиной в несколько процентов. Если построить зависимость величины
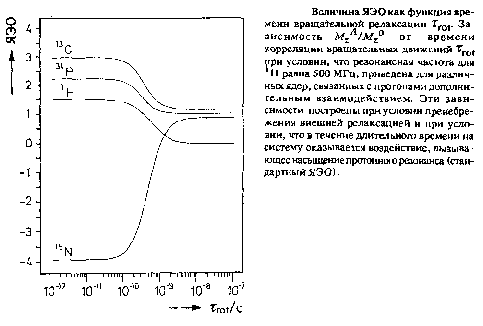
ЯЭО от длительности насыщающего импульса или длительности интерва-ламежду 180°-ным и 90°-ным импульсами, то первоначальное возрастание определится межатомным расстоянием Tab между рассматриваемыми спинами. Определение расстояний: с помощью эффекта Оверхаузера является существенным элементом алгоритма установления структуры биологических макромолекул с помощью ЯМР.
7. Использование стабильных изотопов в качестве меток
Введение радиоактивных изотопов в качестве меток – один из стандартных методов, используемых в биохимии для установления путей протекания реакций. В ЯМР он также является основным экспериментальным методом, однако при условии, что используются стабильные изотопы. Если ход химических реакций известен точно, то этот метод может быть использован в качестве вспомогательного для проведения отнесения сигналов в спектрах. Если, например, в определенном положении протон замещается на дейтерий, то отсутствие соответствующей линии в спектре является точным доказательством того, что именно этот протон занимает данное, определенное положение. Для того чтобы иметь возможность проследить за ходом протекания реакций, необходимо заменить изотоп, регистрируемый обычно в спектрах ЯМР, на другой изотоп, и затем проследить за изменением интенсивности соответствующей линии в спектре ЯМР.
Типичным примером такого рода замещения является замена 14N на 15N, 12C на 13C и 1H на 2H. Это изотопное замещение наиболее интересно при проведении исследований методом ЯМР in-vivo. Трудности возникают только для ядер 31P, для которых отсутствуют стабильные изотопы, при использовании которых можно было бы провести изотопное замещение обычными методами. Здесь ситуацию можно существенно упростить, проведя маркировку по всей группе. Можно проследить за поведением фосфатной группы в процессе реакции, если провести маркировку по изотопам кислорода 17O или 18O, естественное содержание которых весьма невелико.
Проведение изотопного замещения по 17O, спин которого равен 5/2, приводит к расщеплению сигнала фосфора в секстет. Наличие квадрупольного момента у кислорода уменьшает время релаксации ядерного спина 7O. Спин-спиновое взаимодействие с ядром 31P позволяет получить представление об эффективных механизмах, дающих дополнительный вклад в релаксацию. Если с атомом фосфора связаны больше одного атома 17O, то линия приобретает сложную мультиплетную структуру, так что интенсивность сигнала уменьшается, и его уже трудно отличить от фона. Иная картина наблюдается для изотопа 18O. Этот изотоп, как и изотоп 16O, наиболее распространенный в природе, обладает нулевым спином и не вызывает появления дополнительной структуры в наблюдаемой спектральной линии. Правда, замена атома 16O в фосфатной группе на атом О приводит к небольшому высокопольному сдвигу резонансной линии на 0,025 м.д., причем этот сдвиг пропорционален числу связанных с атомом фосфора тяжелых изотопов. При этом можно наблюдать сигнал ЯМР 31P от фосфатной группы отдельно, что позволяет установить число атомов 1 О.
Изотопный обмен 18O может быть использован для более полного изучения реакций ферментативных превращений. При катализе большая группа ферментов расщепляет фосфаты, ответственные за энергозапас, и таким образом осуществляется перенос фосфатной группы или на другой субстрат или на окружающую воду. При ферментативном гидролизе нуклеозидтрифосфата, ответственного за энергозапас клетки, в качестве промежуточного продукта возникает такое состояние фосфатной группы, при котором связь с ангидридом фосфорной кислоты уже расщеплена, однако фосфатный остаток P1 – еще связан с нукле-озиддифосфатом и присоединен к ферменту Е. Формально эту реакцию можно представить в виде следующего уравнения:
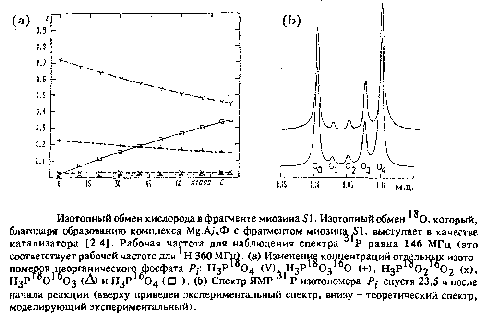
В принципе, все этапы реакции в являются обратимыми, хотя скорость протекания этих процессов зависит от активационной энтальпии Д G*^, т.е. от особенностей ферментативного катализа. Для многих ферментов этап повторяется многократно, прежде чем, наконец, фосфатная группа попадет в воду. Если провести полное замещение по концевой фосфатной группе в НТФ по изотопу 18O, то при протекании реакции в обычной воде всякий раз при прохождении первого этапа реакции атом16O встраивается в фосфатную группу. Если же обратный процесс невозможен до тех пор, пока в реакционную смесь не попадет Pi, то в смеси присутствует только вещество следующего состава: Р160180з. В другом предельном случае, т.е. при условии, что первый этап реакции будет многократно повторяться, прежде чем в реакционную смесь попадет Pi, в смеси можно обнаружить свободный P16и4· Использование соответствующих теоретических моделей позволяет найти зависящее от времени распределение меток. Согласование свободных параметров дает возможность предположить, что существует конечное число обратных реакций с высвобождением Pi и значением константы скорости к-г для связывания Pi в комплекс Е.НДФ. На рис. 2.13 приведен пример такого моделирования для миозинового фрагмента Si. Правда, здесь проведено рассмотрение не для меченой АТФ, а для изотопомеченого неорганического фосфата. Здесь наблюдается обратная реакция в присутствии комплекса Sl. Mg.AДΦ. В этой системе первый этап повторяется примерно 40 раз, прежде чем высвобождается фосфат. Первые эксперименты по изучению механизма ферментативного изотопного обмена в фосфатной группе проходили с привлечением масс-спектрометрии, поскольку этот метод является весьма чувствительным для определения изотопного состава в малых молекулах. Преимуществом ЯМР является то, что при определении изотопного состава можно проводить измерения непрерывно, без дериватизации, хотя при работе с низкими концентрациями метод масс-спектрометрии, конечно, более эффективен.

Нравится материал? Поддержи автора!
Ещё документы из категории физика:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ