Конспект урока по Химии "Гидроксиды металлов"
Гидроксиды металлов
Г
 ИДРОКСИДЫ Ме
ИДРОКСИДЫ Ме

О
 СНОВАНИЯ
СНОВАНИЯ
АМФОТЕРНЫЕ
КИСЛОТЫ
-
РАСТВОРИМЫЕ ИЛИ ЩЕЛОЧИ
НЕРАСТВОРИМЫЕ
Основания – сложные вещества, состоящие из атомов металла и гидроксогруппы.
Основания – это гидроксиды металлов с валентностью I – II реже III.
Общая формула ![]()
Амфотерные гидроксиды – это гидроксиды металлов с валентностью II – IV, проявляющие слабые кислотные свойства.
Кислоты – гидроксиды металлов с валентностью IV – VII, проявляющие кислотные свойства (номенклатура, свойства как у всех кислот)
Классификация оснований
по кислотности – однокислотные (содержат одну гидроксильную группу), многокислотные (содержат несколько гидроксильных групп)
по растворимости в воде – растворимые или щелочи и нерастворимые.
Номенклатура оснований и амфотерных гидроксидов: гидроксид + русское название металла + (валентность металла)
Физические свойства:
все неорганические основания – твердые вещества,
большинство оснований белого цвета, однако, есть окрашенные, например Cu(OH)2 – голубого, CuOH – желтого, Fe(OH)3 – красно-бурого цвета.
По отношению к воде растворимые и нерастворимые (выпишите растворимые и нерастворимые основания по таблице).
Химические свойства
Химические свойства щелочей.
растворяются в воде
действуют на индикаторы
взаимодействуют с кислотными оксидами:
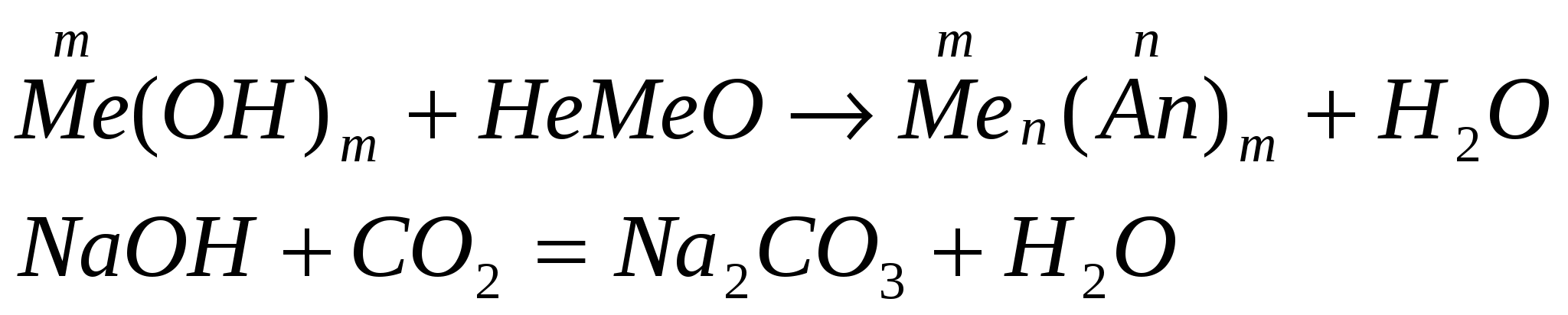
взаимодействуют с кислотами (реакция нейтрализации)
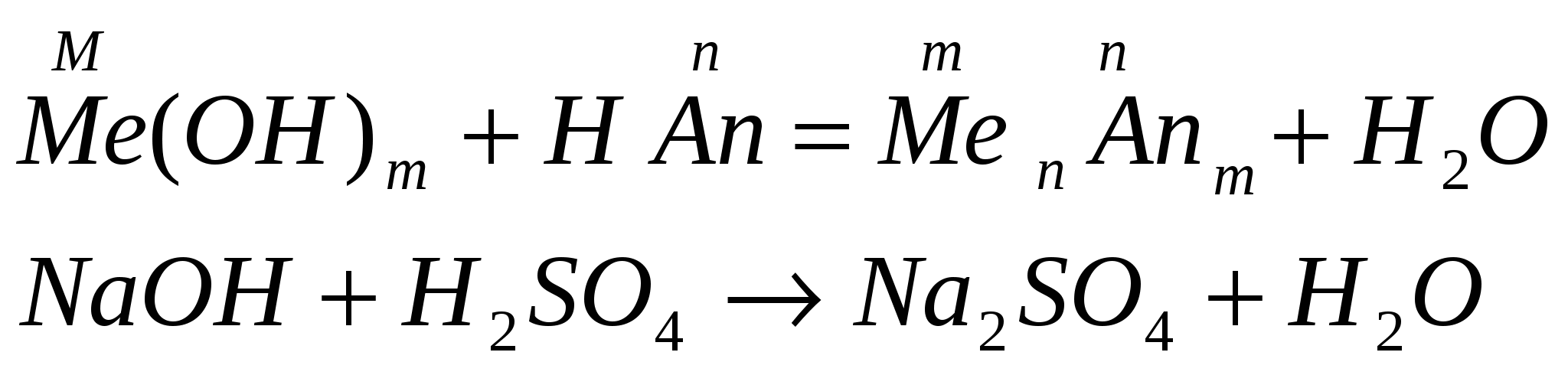
взаимодействуют с солями, если выпадает осадок
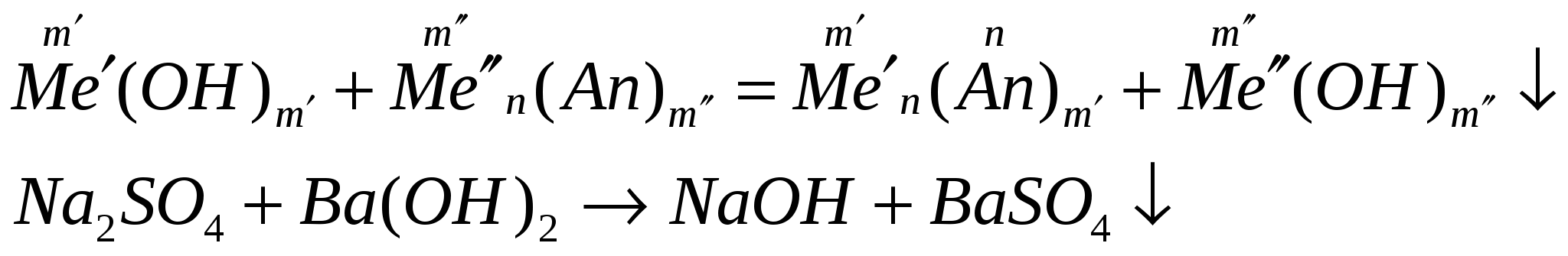
взаимодействуют с амфотерными оксидами
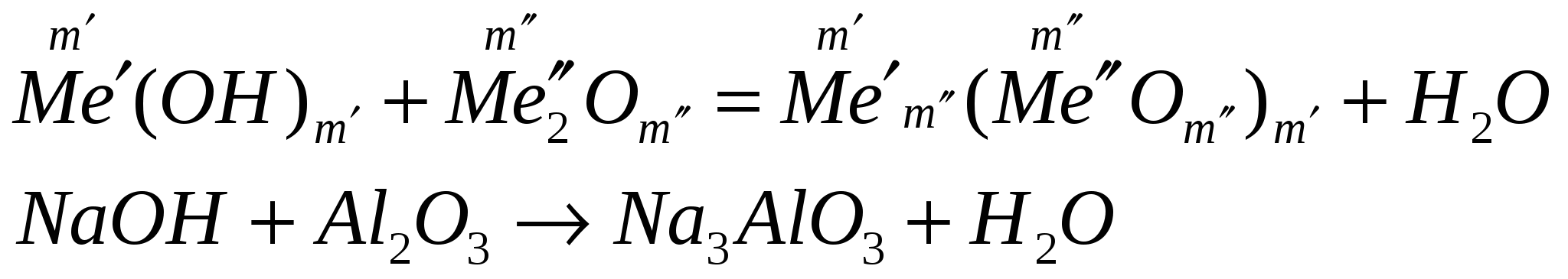
взаимодействуют с амфотерными гидроксидами.
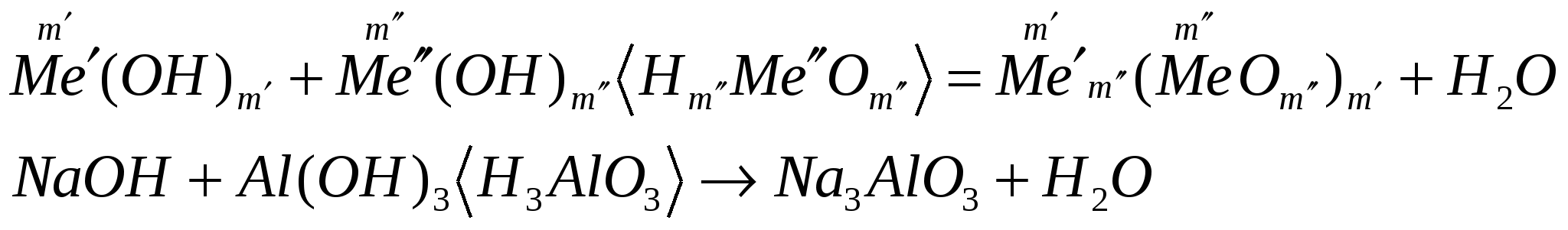
Химические свойства нерастворимых оснований
взаимодействуют с кислотами
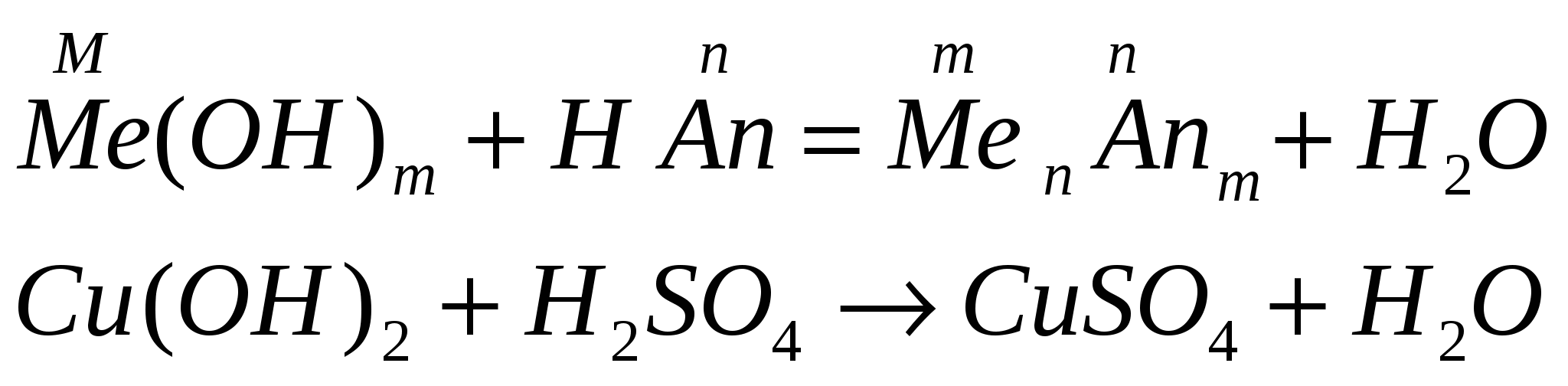
разлагаются при нагревании
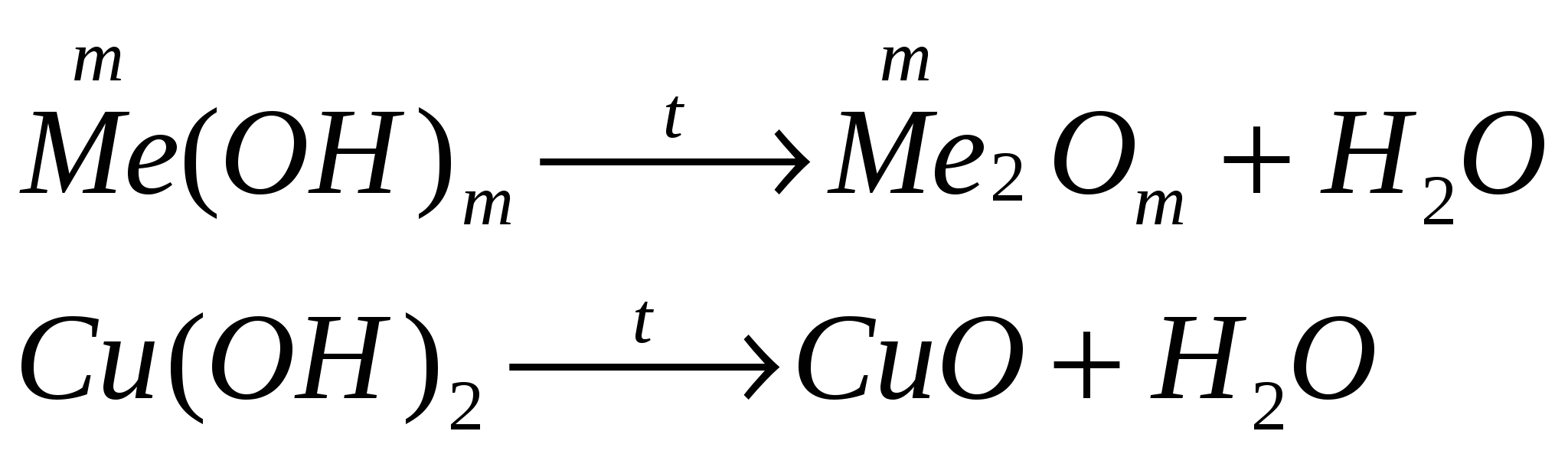
Химические свойства амфотерных гидроксидов.
взаимодействуют с кислотами
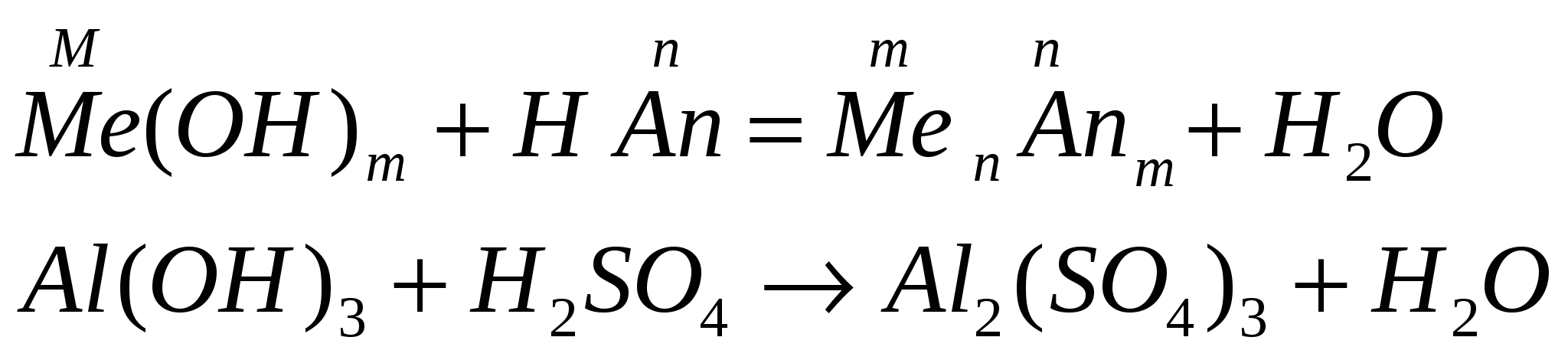
разлагаются при нагревании
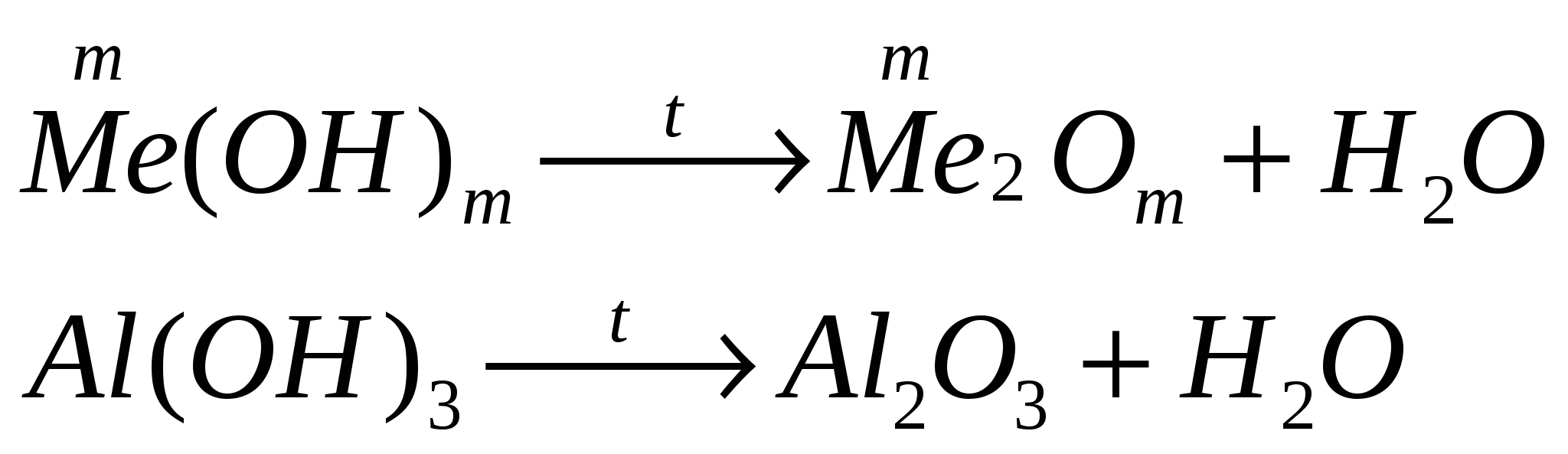
взаимодействуют с основаниями
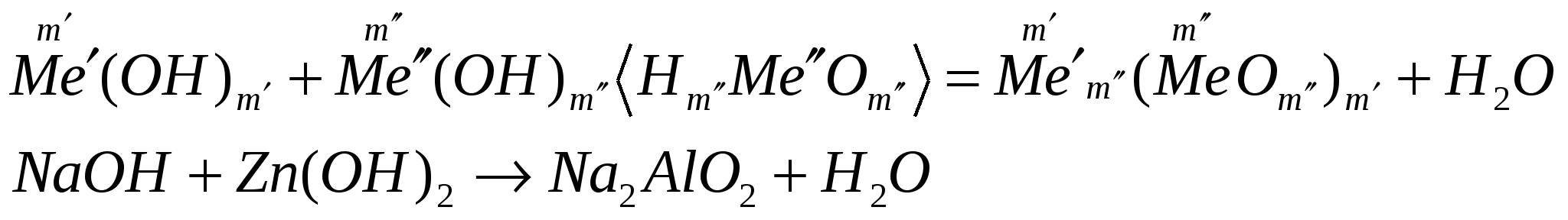
ПОЛУЧЕНИЕ ОСНОВАНИЙ
Щелочи
Нерастворимые и амфотерные основания
Взаимодействие металла с водой:
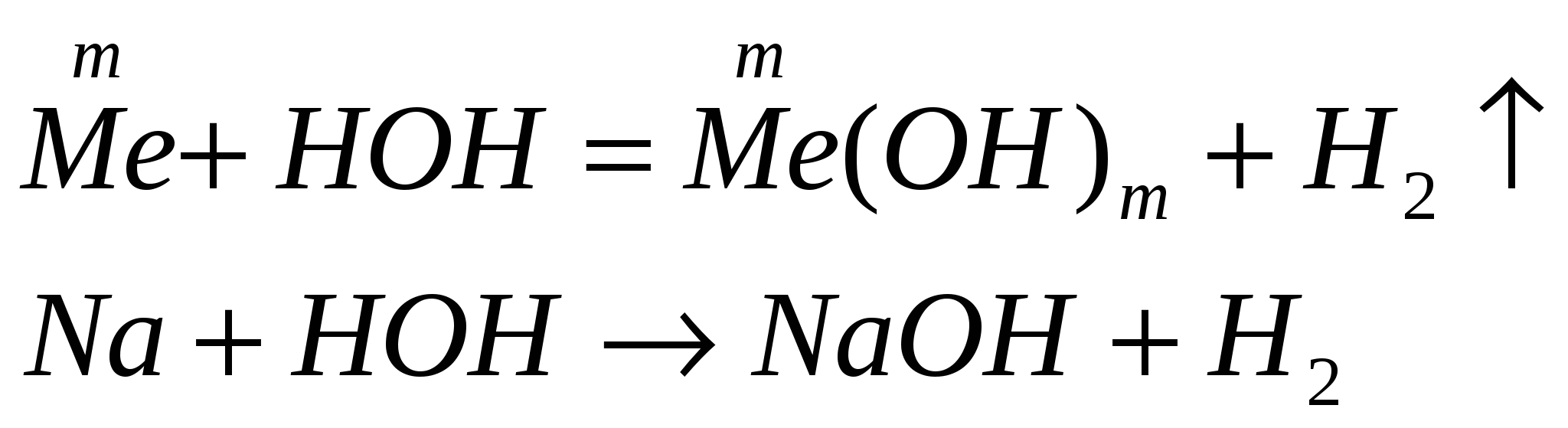
Действием щелочей с водными растворами солей:
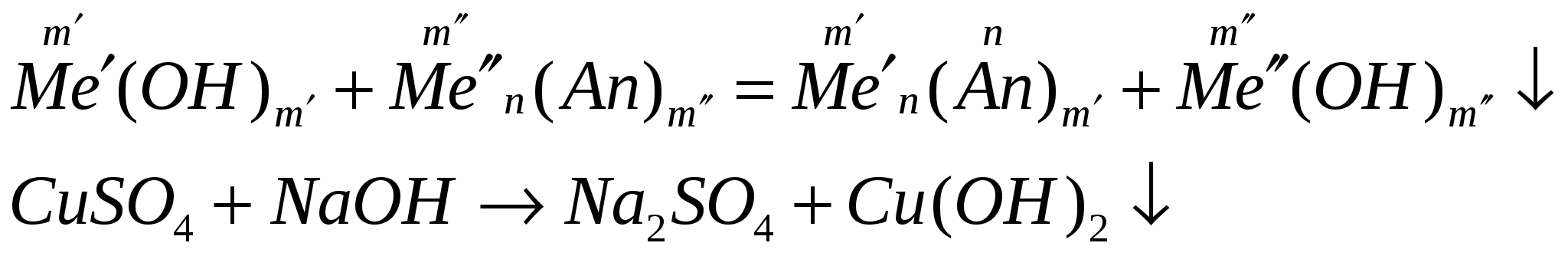
2. Взаимодействие оксида металла с водой
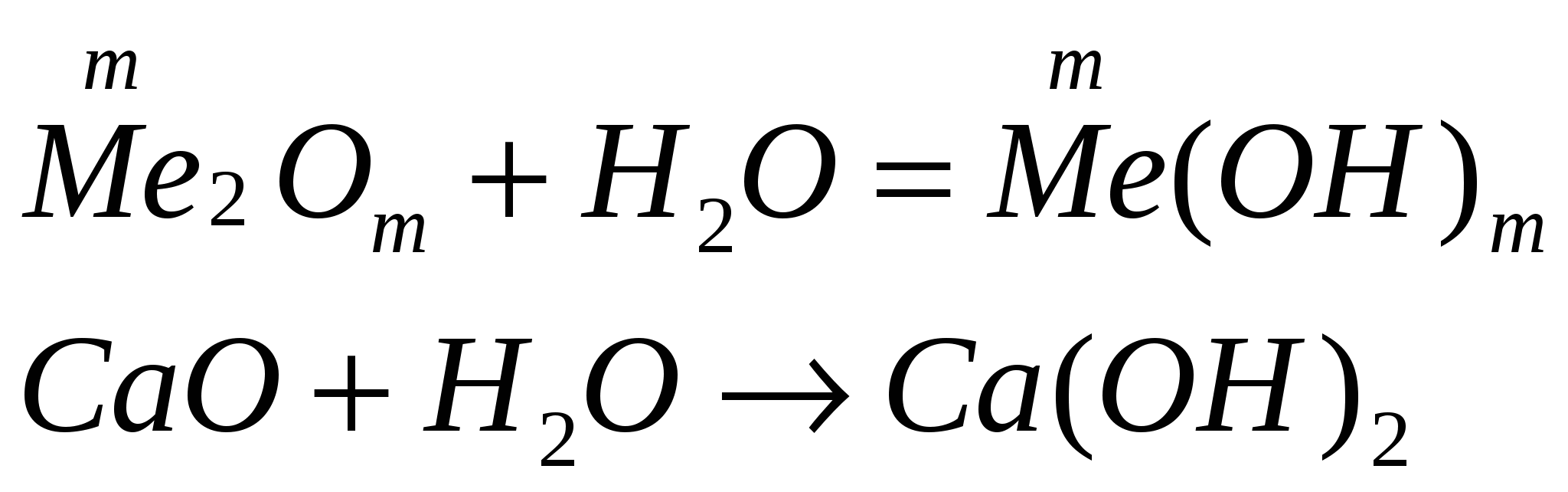
3. Электролиз растворов солей:
![]()

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ