Решение задач на вывод химических формул
Решение задач на вывод химических формул
С задачами на вывод химической формулы вещества учащиеся встречаются при прохождении программы химии с 8 по 11 классы. К тому же, данный тип задач довольно часто встречается в олимпиадных заданиях, контрольно – измерительных материалах ЕГЭ (части В и С). Диапазон сложности данных задач достаточно широк. Как показывает опыт, у школьников часто возникают затруднения уже на первых этапах решения при выводе молярной массы вещества.
В данной разработке предлагаются задачи на нахождение формулы вещества, исходя из разных параметров в условиях. В представленных задачах приведены различные способы нахождения молярной массы вещества. Задачи составлены таким образом, чтобы учащиеся могли освоить оптимальные методы и различные варианты решения. Наглядно демонстрируются наиболее общие приёмы решений. Для учащихся предлагаются решённые задачи по принципу нарастания сложности и задачи для самостоятельного решения.
Вывод химической формулы вещества:
Вычисление молярной массы вещества
Задачи для самостоятельного решения
- на основании массовых долей (%) атомов элементов
M![]() , где n - число атомов
, где n - число атомов
Определить химическую формулу соединения, имеющего состав: натрий – 27,06%; азот – 16,47 %; кислород – 57,47%. Ответ: NaNO3
- на основании массовых долей (%) атомов элементов и относительной плотности соединения
М (CхНу) = D(Н2) ·М (Н2)
Относительная плотность паров органического кислородсодержащего соединения по кислороду равна 3, 125. Массовая доля углерода равна 72%, водорода – 12 %. Выведите молекулярную формулу этого соединения. Ответ:C6H12О
- по относительной плотности вещества и общей формуле класса
М (CхНу) = D(Н2) ·М (Н2)
Относительная плотность паров предельного альдегида по кислороду равна 1,8125. Выведите молекулярную формулу альдегида. Ответ: C3Н6О
- на основании массовых долей (%) атомов элементов и плотности в газообразном состоянии
М находится по
М (в-ва)=Vm·ρ
Углеводород содержит 81,82 % углерода. Масса 1 л. этого углеводорода (н.у.) составляет 1,964 г. Найдите молекулярную формулу углеводорода.
Ответ: C3Н8
- по массе или объёму исходного вещества и продуктам горения
![]() М (CхНу) = D(Н2) ·М (Н2)
М (CхНу) = D(Н2) ·М (Н2)
Относительная плотность паров кислородсодержащего органического соединения по гелию равна 25,5. При сжигании 15,3 г. этого вещества образовалось 20,16 л. СО2 и 18,9 г. Н2О. Выведите молекулярную формулу этого вещества.Ответ: C6H14О
1)Определите молекулярную формулу предельного углеводорода, если
а) относительная плотность по водороду равна 43;
б ) относительная плотность по кислороду равна 4,44
) относительная плотность по кислороду равна 4,44
Дано: Решение:
D (CxHу) Н2 = 43 1.Найдём молекулярную массу
СnH2n+2 М CxHу = D(CxHу)Н2 ![]() Мr(Н2)
Мr(Н2)

X -: У- ? (n)
2. Найдём количество атомов, составив уравнение
СnH2n+2 =86 (Вместо С и Н подставим числовые значения их относительных атомных масс и придём к математическому уравнению)
12n + 2n + 2 = 86; 14n = 86 – 2; 14n = 84; n = 6 => C6H14
2) Вывести химическую формулу алкена, если его плотность равна 3,125 г/л.
3) Вывести химическую формулу алкина, если 1 литр его весит 3,04г.
4) Вывести химическую формулу альдегида, если его относительная плотность по воздуху равна 2.
5) Вывести химическую формулу карбоновой одноосновной кислоты, если плотность паров равна 3,93 г/л.
6) Вывести химическую формулу однозамещённого хлорпроизводного предельного углеводорода, если его относительная плотность по воздуху равна 2,224.
8-7. Какой газообразный алкан имеет при нормальных условиях плотность 1,339 г/л?
8-8. Алкан имеет плотность паров по воздуху 4,414. Определить формулу алкана.
8-9. Молекула алкана содержит 26 электронов. Установите его формулу.
8-24. При бромировании углеводорода было получено бромпроизводное, имеющее относительную плотность по кислороду, равную 5,094. Определите возможное строение углеводорода, предложите способ его получения из неорганических реагентов.
8-26.Приведите структурные формулы циклоалканов, в молекулах которых находится по 40 электронов.
8-27. Алкен имеет молекулярную массу – 84. Определите его молекулярную формулу.
8-28. В молекуле циклоалкена число атомов углерода и водорода различается на 4. Приведите структурные формулы этого соединения и его изомера, не относящегося к циклическим углеводородам.
8-29. Установите молекулярную формулу алкена и продукта взаимодействия его с 1 моль бромоводорода, если это монобромпроизводное имеет относительную плотность по воздуху 4,24. Укажите название одного изомера исходного алкена.
15-43. Относительная плотность паров хлоралкана по алкену, из которого он получен, равна 1,87. Установите строение алкена
15-2.Молекулярная масса алкина – 96. Что это за алкин?
15-1. Определить формулу ароматического углеводорода с относительной молекулярной массой 92.
15-7. Приведите структурную формулу ароматического углеводорода, имеющего в молекуле 50 электронов
1.18 (3) Относительная плотность паров алкана по водороду равна 57. Выведите молекулярную формулу алкана.
1.19 (3) Относительная плотность паров алкана по азоту равна 5,07. Выведите молекулярную формулу алкана.
2.7 (3) Относительная плотность паров циклоалкана по кислороду равна 3,5. Выведите молекулярную формулу циклоалкана.
2.8 (3) Плотность циклоалкана при нормальных условиях равна 1,875 г/л. Выведите молекулярную формулу циклоалкана.
2.13 (3) Углеводород имеет относительную плотность по азоту 2,5. Он не обесцвечивает бромную воду. Предположите возможную структуру углеводорода. Дайте название.
2.14 (3) Углеводород имеет относительную плотность по углекислому газу 1,9. Он не обесцвечивает холодный раствор перманганата калия. Предположите возможную структуру углеводорода. Дайте название.
3.12 (3) Относительная плотность паров алкена по водороду равна 42. Выведите молекулярную формулу алкена.
3.13 (3) Плотность алкена при н. у. равна 2,5 г/л. Выведите молекулярную формулу алкена.
4.11 (3) 2 л алкадиена при н.у. имеет массу, равную 4,82 г. Выведите молекулярную формулу алкадиена.
4.12 (3) Относительная плотность паров алкадиена по кислороду равна 3. Выведите молекулярную формулу алкадиена.
4.13 (3) Относительная плотность углеводорода по воздуху равна 2,345. Массовая доля углерода в нем равна 88,24%. Выведите молекулярную формулу углеводорода.
5.13 (3) 1 г алкина при н. у. занимает объем 0,86 л. Выведите молекулярную формулу алкина.
5.14 (3) Относительная плотность паров алкина по воздуху равна 2,83. Выведите молекулярную формулу алкина.
.
6.15 (3) Относительная плотность по гелию паров углеводорода ряда бензола равна 23. Выведите его молекулярную формулу.
6.16 (3) Пары арена имеют относительную плотность по воздуху 4,14. Выведите его молекулярную формулу.
7.17 (3) Относительная плотность паров предельного одноатомного спирта по водороду равна 37. Выведите молекулярную формулу спирта.
7.18 (3) Относительная плотность паров предельного простого эфира по гелию равна 15. Выведите молекулярную формулу эфира.
8.8 (3) Относительная плотность паров предельного двухатомного спирта по кислороду равна 3,25. Выведите молекулярную формулу спирта.
8.9 (3) Относительная плотность паров предельного трехатомного спирта по метану равна 5,75. Выведите молекулярную формулу спирта.
10.13 (3) Относительная плотность паров предельного альдегида по кислороду равна 1,8125. Выведите молекулярную формулу альдегида.
10.14 (3) Относительная плотность паров предельного альдегида по неону равна 5. Выведите молекулярную формулу альдегида.
10.15 (3) Относительная плотность паров органического соединения по водороду равна 36. Массовая доля углерода в этом веществе равна 66,67%, массовая доля водорода равна 11,11%, а остальное приходится на кислород. Выведите молекулярную формулу органического соединения и предложите структуру, если известно, что это вещество: а) не дает реакции «серебряного зеркала»; б) дает реакцию «серебряного зеркала».
11.15 (3) Относительная плотность паров предельной двухосновной карбоновой кислоты по воздуху равна 4,07. Выведите молекулярную формулу карбоновой кислоты.
13.12 (3) Относительная плотность паров предельного амина по кислороду равна 1,844. Выведите молекулярную формулу амина.
13.13 (3) Относительная плотность паров ароматического амина по метану равна 6,75. Выведите его молекулярную формулу.
7) Углеводород (относительная плотность по водороду равна 39) содержит 92,31 % углерода и 7,69% водорода. Найдите его молекулярную формулу.

Дано: Решение:
W% (С) = 92, 31 1.Найдём молекулярную массу
W% (Н) = 7, 69 Мr (CxHу) = 39 ![]() 2 = 78
2 = 78
D (CxHу)Н2 = 39 2. Найдём количество атомов, т.е. отношение

х : у = ? γ = т/Аr; х : у = ![]() ; => СН
; => СН
3. Убедимся, истинная это формула или простейшая. Для этого найдём молекулярную массу (СН); Мr(СН) = 12 + 1 = 13, а у нас 78 => нашли простейшую формулу. Чтобы вывести истинную формулу вещества нужно
узнать сколько раз 13 уложится в 78,. именно на столько нужно будет увеличить количество атомов в простейшей формуле.
78: 13 = 6 => С6Н6
Mr (С6Н6) = 12 ![]() 6 + 6 = 78
6 + 6 = 78
Или: m(С)=![]() ; m(Н)=78-72=6; х:у=
; m(Н)=78-72=6; х:у=![]() =6:6=>С6Н6
=6:6=>С6Н6
8)Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу кислоты.
Дано:
w (О) = 42,67%
Вывести формулу соединения
CnН2n (N Н2) CОOH
Решение:
Рассчитать молярную массу кислоты CnН2n (N Н2) CОOH
w (О) = ![]()
M кислоты![]() = 75 (г/моль)
= 75 (г/моль)
Найти число атомов углерода в молекуле кислоты и установить её формулу М = 12 n + 2 n + 16 + 45 =75
14 n = 14, n = 1
Ответ: формула кислоты NН2CН2CОOH
М (NН2CН2 CОOH) = 75 г/моль
Задача № 9. Относительная плотность углеводорода по водороду, имеющего состав: w(С) = 85,7 %; w (Н) = 14,3 %, равна 21. Выведите молекулярную формулу углеводорода.
Дано:
w (С) = 85,7 %
w (Н) = 14,3 %
D Н2 (CхНу) = 21
Решение:
Находим относительную молярную массу углеводорода, исходя из величины его относительной плотности: М (CхНу)= D (Н2) ·М (Н2)
![]() М (CхНу)= 21 · 2 = 42
М (CхНу)= 21 · 2 = 42
m(С) = 42г. /100% · 85, 7 %= 36 г.
m (Н) = 42г. /100% · 14,3 %= 6 г.
Находим количество вещества атомов углерода и водорода
n (С) = 36г :12 г/моль = 3 моль
n (Н) = 6г.: 1 г/моль = 6 моль
Ответ: истинная формула вещества C3Н6.
Вывести формулу соединения
CхНу- ?
Задача № 10 Определите молекулярную формулу алкана, если известно, что его пары в 2,5 раза тяжелее аргона.
Дано:
Пары алкана в 2,5 раза тяжелее аргона
Решение:
По относительной плотности можно найти молярную массу алкана: М (C n Н 2 n + 2) = 14 n + 2 = 2,5 · М(Ar) = 100 г/моль
Откуда n = 7.
Ответ: формула алкана C7Н14
Вывести формулу алкана
C n Н2 n + 2
Массовая доля углерода в соединении равна 39,97 %, водорода 6, 73 %, кислорода 53,30 %. Масса 300 мл. (н.у.) этого соединения равна 2,41 г. Выведите молекулярную формулу этого вещества.
Дано:
w (С) = 39,97 %
w (Н) = 6,73 %
w (0) = 53,30 %
Vн.у. (CхHуОz) = 300 мл.
m (CхHуОz) = 2,41 г.
Решение:
Для расчёта выбираем 100г. соединения. Тогда масса углерода равна 39,97 г; водорода 6,73 г; кислорода 53,30 г.
1. Определяем количество вещества:
n (С) = 39,97г :12 г/моль = 3,33 моль
n (Н) = 6,73г.: 1,008 г/моль = 6,66 моль
n (0) = 53,3г.: 16 г/моль = 3,33 моль
Определяем наименьшее общее кратное – 3,33.
n (С) : n (Н) : n (0) = 1 : 2 : 1
Простейшая формула соединения – CH2О
М (CH2О) = 30 г/моль
Определяем молярную массу соединения по соотношению:
0,3 л. – 2,41 г.
22,4 л. – х г.
х = (22,4 · 2,41)/0,3 = 180
Или по формуле М= Vm · m/ V
К = 180 : 30 = 6
Определяем молекулярную формулу соединения, умножая стехиометрические коэффициенты в простейшей формуле на 6.
Ответ: искомая формула - C6H12О6
Вывести формулу соединения
CхНуОz- ?
12. Определите формулу углеводорода, массовая доля углерода в котором
82,2 %, а плотность этого вещества составляет 2,59 г/л.
13. Определите формулу красителя-анилина. По данным анилина массовая доля углерода в нем 77,4%, водорода — 7,5 %, азота — 15,1 %. Относительная плотность паров этого вещества по воздуху равна 3,21.
14. Относительная молекулярная масса исследуемого вещества равна
237, массовая доля углерода в нем составляет 10,1 %, а хлора — 89,9. Установите формулу этого хлорзамещенного углеводорода.
15. Определите молекулярную формулу предельного углеводорода, плотность которого равна 1,97 г/л, а массовая доля углерода составляет — 0,82.
16. Какова формула вещества, при анализе состава которого
установлено: массовая доля углерода в нем равна 0,52; кислорода — 0,35, а
водорода — 0,13? Относительная плотность вещества по водороду составляет
23.
17. Определите молекулярную формулу кислородсодержащего органического вещества по данным анализа: массовая доля углерода — 54,55 %; массовая доля водорода — 9,09 %.
18. Углеводород содержит в массовых долях 0,8889 или 88,89 % углерод. Его плотность по воздуху равна 1,852. Найдите молекулярную формулу этого углеводорода.
19. Определите формулу вещества, если массовая доля азота в нем 30,43%, а кислорода — 69,57 %.
20. Химический анализ показал, что в 17 г соединения алюминия с кислородом содержится 9 г алюминия. Найдите простейшую формулу этого соединения.
21. Найдите простейшую формулу оксида хрома, содержащего 68,4 % хрома.
22. Найдите простейшую формулу вещества, содержащего 43,6 % натрия, 11,3 % углерода и 45,3 % кислорода.
23. При анализе навески 3,16 мт органического вещества обнаружено, что в его составе 0,96 мт углерода, 0,12 мг водорода и 0,8 мт кальция, а остальное приходится на кислород. Найдите простейшую формулу этого соединения.
24. Известно, что оксид некоторого металла содержит 11,11 % кислорода и в его молекуле на один атом кислорода приходится два атом, а металла. Определите, что это за металл, и о каком соединении идет речь.
25. Найдите формулу соединения, если известно, что в его состав входи-
1,59 % водорода, 22,22 % азота, 76,19 % кислорода.
26. Дано: углерода —92,3 %, водорода — 7,7 %, масса 1 л газа при н.у. 1,16 г. Определить молекулярную формулу.
27. Хлорпроизводное предельного углеводорода имеет молекулярную массу 237. Процентный состав этого соединения следующий: хлора — 89,9 %, углерода — 10,1 %. Найдите его молекулярную формулу.
1. Найдем массу хлора
237 ![]() 0,899 = 213
0,899 = 213
237—213 = 24
х : .у=24/12 : 213/35,5=2 : 6=>С2С16.
28. Определите формулы двух оксидов одного и того же элемента, если его массовая доля в этих оксидах равна 88,11 и 84,75%. Этот элемент образует также фторид, содержащий 32,47 % фтора по массе.
29. Элемент ниобий образует более двадцати галогенводородов. Установите две формулы соединений ниобия с одним из галогенов, если содержание металла в них составляет 15,47 и 21,54 % по массе.
30. Относительная плотность по водороду неизвестного газообразного вещества равна 22. Найдите молекулярную формулу этого вещества, если массовая доля (С) в нем 54,55 %, (Н) — 9,09 %, (О) — 36,36 %.31. Найдите простейшую формулу соединения, имеющего следующий состав: Nа —42,1 %, Р — 18,9 %, О — 39,0 %.
8-1. Определите молекулярную формулу органического соединения с составом 80% углерода и 20% водорода, если плотность его по воздуху равна 1,034.
8-2. Определите молекулярную формулу углеводорода, который содержит 85,7% углерода и имеет плотность по водороду 21.
8-3. Органическое вещество содержит 84,21% углерода и 15,79% водорода. Плотность паров вещества по воздуху 3,93. Определить формулу вещества.
8-4. Углеводород содержит 82,76% углерода и 17,24% водорода (по массе). При монохлорировании этот углеводород образует два изомерных алкилхлорида – первичный и третичный. Определить строение исходного углеводорода.
8-5. Органическое вещество содержит 91, 3% углерода и 8,7% водорода. Относительная плотность паров по кислороду равна 2,875. Вывести молекулярную формулу вещества.
8-6. Установите молекулярную формулу углеводорода, молекула которого содержит 40 электронов, а молекулярная масса которого 70.
8-10. Найти молекулярную формулу предельного углеводорода, массовая доля углерода в котором 83,3%.
8-11. Установите молекулярную формулу дибромалкана, содержащего 85,11% брома.
8-12. Установите молекулярную формулу монохлоралкана, содержащего 38,38% хлора. Приведите графические формулы и названия всех соединений, отвечающих данной формуле.
8-13. Монохлорпроизводное предельного углеводорода содержит 38.4% хлора. Определить формулу углеводорода.
8-14. Монохлорпроизводное предельного углеводорода содержит 38,4% хлора по массе. Определите, сколько атомов углерода содержится в молекуле этого вещества.
8-15. В монохлоралкане массовая доля хлора равна 55,04%. Определите формулу монохлоралкана.
8-16. Определите молекулярную формулу фторпроизводного алкана, в 34,27 г которого содержится 17,44 г фтора.
8-17. Определите молекулярную формулу хлорпроизводного алкана, в 35,24 г которого содержится 23,83 г хлора.
8-18. Дихлорпроизводное алкана содержит 5,31% водорода по массе. Определите молекулярную формулу дихлоралкана. Приведите структурную формулу одного из возможных изомеров и назовите его.
8-19. Вещество содержит 36.4% С, 6.1% Н и фтор. Молекулярная масса этого вещества меньше 110. Сколько всего атомов в этой молекуле?
8-20. Органическое вещество содержит 0,2424 доли углерода, 0,0404 доли водорода, 0,7172 хлора. Плотность паров по азоту составляет 3,5357. Определите химическую формулу этого вещества.
8-21. Органическое вещество содержит 0,2975 углерода, 0,0413 водорода, 0,6612 брома. Относительная плотность паров по воздуху равна 4,1724. Вывести молекулярную формулу вещества.
8-22. Хлорпроизводное предельного углеводорода имеет молекулярную массу 257. Процентный состав этого соединения следующий: хлор-89,9%, углерод-10,1%. Определите его молекулярную формулу.
8-23. При монохлорировании углеводорода, содержащего 83,72% С и 16,28% Н, образовалось 2 изомерных хлорпроизводных – первичное и третичное. Установите строение углеводорода, составьте формулы продуктов хлорирования
8-25. Содержание брома в соединении, полученном при взаимодействии алкена с бромом, составляет 69,56 мас.%. Определите структурную формулу алкена, если известно, что он может существовать в виде цис- и транс- изомеров.
.
15-10. Ароматическое соединение ряда бензола содержит 90.0% углерода. Нарисовать ео возможные изомеры.
15-48. Плотность по водороду вещества равна 22. Вещество имеет следующий состав: углерод - 54,55%, водород - 9,09%, кислород – 36,36% Вещество легко восстанавливает оксид серебра. Определить это вещество.
15-50. Органическое вещество природного происхождения содержит 40 мас.% углерода, 6,67 мас.% водорода и кислород. Сколько всего атомов содержит молекула этого соединения, если известно, что его молярная масса равна 180 г/моль?
15-26. В предельной одноосновной карбоновой кислоте массовая доля кислорода равна 43,24%. Определите формулу кислоты.
15-28. Предельная одноосновная карбоновая кислота содержит 48.6%С. Какая это кислота?
15-30. Установите молекулярную формулу предельной карбоновой кислоты, метиловый эфир которой содержит 9,09% водорода.
15-40. При взаимодействии первичного одноатомного спирта, содержащего 60% углерода и 13,3% водорода, с органической кислотой образовалось вещество, плотность паров которого по водороду равна
Определите молекулярную формулу каждого из веществ.
15-41. При взаимодействии одноатомного спирта, содержащего 52,17% углерода и 13,04% водорода, с органической кислотой, образуется вещество, плотность паров которого по водороду равна 51. Определите молекулярную формулу каждого вещества, участвующего в реакции, и дайте им название.
15-42. При взаимодействии одноатомного спирта, содержащего 37,5% углерода, 12,5% водорода, с органической кислотой образуется вещество, плотность паров которого по водороду равна 37. Определите молекулярную формулу каждого вещества, участвующего в реакции, и дайте им название.
15-49. Эфир с молярной массой 130 г/моль при гидролизе образует кислоту, в серебряной соли которой массовая доля серебра составляет 59,66%. Определите число атомов углерода в молекуле спирта, образовавшего эфир.
15-37. Определите молекулярную формулу предельного многоатомного спирта, в 31,25 г которого содержится 14,15 г кислорода.
15-39. Определите молекулярную формулу предельного многоатомного спирта, в 37,67 г которого содержится 16,62 г углерода.
15-14. Путресцин содержит 54,5% (С), 13,6% (Н), остальное приходится на азот. Плотность его паров по водороду равна 44. Установите молекулярную формулу путресцина.
15-15. Одно из важнейших химических соединений реагентов, относящихся к классу диаминов, содержит 40% (С) , 46,7% (N), остальное – водород. Установите молекулярную формулу этого органического соединения.
15-17. Вещество содержит 69,2 % С, 3,85 % Н и азот. Молекулярная масса этого вещества меньше 150. Сколько всего атомов в этой молекуле?
15-20. Предельный амин содержит 31.1% азота. Определите возможное строение этого амина.
15-21. Установите молекулярную формулу предельного третичного амина, содержащего 23,73% азота по массе.
15-29. Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу аминокислоты.
1.20 (3) Газообразный углеводород имеет относительную плотность по кислороду 1,375, а массовые доли углерода и водорода в нем составляют соответственно 81,8% и 18,2%. Какое это соединение?
1.21 (3) Относительная плотность паров углеводорода по кислороду равна 2,25. Массовая доля углерода в нем равна 83,33%. Выведите молекулярную формулу этого углеводорода.
1.22 (3) Плотность углеводорода при нормальных условиях равна 1,964 г/л. Массовая доля углерода в нем равна 81,82%. Выведите молекулярную формулу этого углеводорода.
2.9 (3) Относительная плотность паров углеводорода по азоту равна 3. Массовая доля углерода в нем равна 85,71%. Выведите его молекулярную формулу.
2.10 (3) Относительная плотность паров углеводорода по водороду равна 35. Массовая доля водорода в нем равна 14,285%. Выведите молекулярную формулу углеводорода.
3.14 (3) Относительная плотность паров углеводорода по азоту равна 3,5. Массовая доля углерода в нем равна 85,71%. Выведите молекулярную формулу углеводорода.
3.15 Углеводород массой 12,5 г при н. у. занимает объем 5 л. Массовая доля водорода в нем равна 14,29%. Выведите молекулярную формулу углеводорода.
5.15 Относительная плотность паров углеводорода по водороду равна 41. Массовая доля водорода в нем равна 12,2%. Выведите молекулярную формулу углеводорода
5.16 (3) Относительная плотность паров углеводорода по кислороду равна 2,125. Массовая доля углерода в нем равна 88,24%. Выведите молекулярную формулу углеводорода
6.17 (3) Относительная плотность паров углеводорода по углекислому газу равна 2,41. Массовая доля углерода равна 90,6%. Выведите молекулярную формулу углеводорода.
6.21 (1,3) При хлорировании на свету некоторого углеводорода получается единственное монохлорпроизводное, массовая доля хлора в котором равна 22,98%. Назовите исходный углеводород.
6.22 (1,3) При хлорировании на свету некоторого углеводорода получается единственное монохлорпроизводное, массовая доля хлора в котором равна 21,07%. Назовите исходный углеводород.
7.19 (3) Относительная плотность паров органического соединения по кислороду равна 2,75. Массовая доля углерода в этом веществе равна 68,18%, массовая доля водорода равна 13,64%, остальное — кислород. Выведите молекулярную формулу этого вещества.
7.20 (3) Относительная плотность паров органического соединения по воздуху равна 4. Массовая доля углерода в этом веществе равна 72,41%, массовая доля водорода равна 13,79%, массовая доля кислорода равна 13,79%. Выведите молекулярную формулу этого вещества.
8.7 (3) Относительная плотность паров органического вещества по углекислому газу равна 2,41. Массовая доля углерода в этом веществе равна 45,28%, массовая доля водорода равна 9,44%, а остальное приходится на кислород. Выведите молекулярную формулу этого вещества.
8.10 (3) Относительная плотность паров органического вещества по водороду равна 60. Массовая доля углерода в этом веществе равна 50%, массовая доля водорода равна 10%, массовая доля кислорода равна 40%. Выведите молекулярную формулу органического вещества.
9.5 (3) Относительная плотность паров органического соединения по метану равна 7,75. Массовая доля углерода в этом веществе равна 67,74%, массовая доля водорода равна 6,45%, а остальное приходится на кислород. Выведите молекулярную формулу этого соединения.
9.6 (3) Относительная плотность паров органического соединения по азоту равна 4,5. Массовая доля углерода в этом веществе равна 57,14%, массовая доля водорода равна 4,76%, массовая доля кислорода равна 38,10%. Выведите молекулярную формулу этого соединения.
10.16 (3) 10 л газообразного соединения при н. у. имеют массу 13,4 г. Массовые доли углерода и водорода в нем составляют соответственно 40% и 6,7%, остальное — кислород. Установите молекулярную формулу соединения.
10.17 (3) Относительная плотность паров органического соединения по кислороду равна 3,125. Массовая доля углерода в этом веществе равна 72%, массовая доля водорода равна 12%, остальное — кислород. Выведите молекулярную формулу этого соединения.
11.14 (3) Массовая доля углерода в предельной одноосновной карбоновой кислоте составляет 54,5%. Какая это кислота? Какие эфиры будут ее изомерами?
11.16 (3) Относительная плотность паров органического соединения по неону равна 5,4. Массовая доля углерода в этом веществе равна 58,82%, массовая доля водорода равна 9,8%, а остальное — кислород. Выведите молекулярную формулу органического соединения. Предложите возможные структуры.
11.17 (3) Относительная плотность паров органического соединения по кислороду равна 4,5. Массовая доля углерода в этом веществе равна 66,67%, массовая доля водорода равна 11,11%, массовая доля кислорода равна 22,22%. Выведите молекулярную формулу органического соединения.
13.14 (3) Массовая доля углерода в диамине равна 48,65%, массовая доля азота равна 37,84%. Выведите молекулярную формулу диамина.
13.15 (3) Массовая доля углерода в моноамине равна 63,16%, массовая доля азота равна 24,56%. Выведите молекулярную формулу амина.
14.10 (2) Выведите молекулярную формулу моноаминокарбоновой кислоты, массовая доля азота в которой составляет 11,97%.
14.11 (3) Массовая доля кислорода в предельном эфире аминоуксусной кислоты составляет 27,35%. Напишите возможные структурные формулы этого эфира.
Вывод формул по продуктам сгорания
Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г. его в кислороде образовалось 6,72 л. СО2 и 7,2 г. Н2О.
Дано:
M (CхHу) = 4,4 г.
ρ (н.у.) = 1,97 г/л
V (СО2) = 6,72 л.
m (Н2О) = 7,2 г.
Решение:
1. Находим относительную молярную массу углеводорода, исходя из величины его относительной плотности:
М (CхHу) = Vm · ρ
М (CхHу) = 22,4л/моль · 1,97г/л = 44г/моль
2. Записываем в алгебраическом виде уравнение реакции горения газа, выразив коэффициенты через х и у. 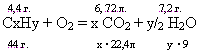
Составляем пропорции:
4,4 / 44 = 6, 72/ х · 22,4
х = 44 · 6, 72/ 4,4 · 22,4 = 3
у = 44 · 7,2/ 4,4 · 9 = 8
Формула соединения C3H8; М (C3H8) = 44 г/моль
Ответ: молекулярная формула соединения C3H8
Вывести формулу
CхHу - ?
1) При сгорании 3г. углеводорода было получено 8,8 г.углекислого газа,5,4 г. воды. Относительная плотность углеводорода по воздуху равна 1,03. Определите молекулярную формулу углеводорода.
3г. 8,8г. 5,4г.
CxHу + О2 = СО2 + Н2О
![]() 44г 18г
44г 18г
Т.к. -.это углеводород => кроме углерода и водорода в нём больше ничего не содержится. Весь углерод из углеводорода перешёл в 8,8г СО2, а водород в 5,4г Н2О.
1. Рассчитаем Мr (CxHу)
Мr (CxHу) = 1,03 ![]() 29 = 30
29 = 30
2.Рассчитаем массу углерода в 8,8г СО2
![]() Х = 2,4г
Х = 2,4г
3. Рассчитаем массу водорода в 5,4г Н2О.
![]() Х = 0,6
Х = 0,6
4. Рассчитаем количество атомов углерода и водорода
γ = т/Аr; х : у = ![]() ;=> С2Н6
;=> С2Н6
5. Устанавливаем простейшая формула или истинная
Мr (С2Н6) = 12 ![]() 2 + 6 = 30; Это истинная формула
2 + 6 = 30; Это истинная формула
2. При сгорании 1,84г органического вещества образовалось 2,64г углекислого газа и 1,44 г воды. Плотность горючего газа по кислороду равна 2,875. Определите молекулярную формулу вещества.
3. При сгорании 6,8 г газообразного неорганического вещества было получено 3,6 г воды и 12,8 г сернистого газа. Плотность горючего газа по кислороду равна 1,06. Определите молекулярную формулу вещества.
4. При сжигании 5,4 г паров неорганического вещества было получено
2,8 г. азота, 8,8 г углекислого газа и 1,8 г воды. Один литр паров этого вещества весит 1,205 г. Определите молекулярную формулу.
5. При сжигании 5,2 г вещества выделилось 8,96 л углекислого газа и 3,6 г воды. Определите молекулярную формулу вещества.
6. При сжигании 2,5 г вещества образовалось 3,42 г Н20 и 5,57 СО2. В состав вещества, кроме водорода и углерода, входит азот (23 %). Какова молекулярная формула.
7. При сжигании 3,1 г вещества (плотность по водороду 15,5), в котором обнаружены азот, водород и углерод, образуются 4,5 г воды; 4,4 г углекислого газа и 1,4 г азота. Определите молекулярную формулу вещества и процентный состав химических элементов.
8. При сжигании без остатка 4,3 г углеводорода получили 13,2 г оксида углерода (IV). Относительная плотность углеводорода по водороду равна 43. Определите молекулярную формулу вещества.
9. При сжигании 2,15 г органического вещества получено 6,6 г углекислого газа и 3,15 г воды. Относительная молекулярная масса этого вещества. равна 86. Установите формулу вещества.
10. Определите молекулярную формулу вещества, при сжигании 3,75 г которого получили 2,25 г водяного пара и 5,5 г оксида углерода (IV). Относительная плотность вещества по водороду равна 15.
11. При сжигании 2,8 л газа получили 8,4 л оксида углерода (IV) (н.у.) и
6,75 г паров воды. Плотность газа 1,875 г/л. Вычислите молекулярную
формулу вещества.
12. При сгорании 2,1 л органического вещества получили 6,6 г оксида углерода (IV), и 2,7 паров воды. Плотность паров исходного вещества по воздуху равна 2,9. Определите состав молекулы углеводорода.
13. При сжигании 2,6 г углеводорода получили 8,8 г оксида углерода (IV). Относительная плотность углеводорода по водороду равна 13. Определите формулу вещества.
14. При сжигании 4,5 г органического вещества получили 13,2 г оксида углерода (IV) и 8,1 г воды. Один литр исходного вещества имеет массу 1,35 г. Напишите его формулу.
15. В струе кислорода сожгли два образца вещества. При сгорании 0,9 г
вещества (А) образовалось 1,32 г углекислого газа и 0,54 г воды. При сгорании 1,71 г вещества (Б) выделилось 2,64 г углекислого газа и 0,99 г воды. Известно, что молярная масса вещества (А) 180 г/моль, а вещества (Б) 342 г/моль. Найдите молекулярные формулы этих веществ.
16. При сжигании углеводорода массой 8,8 г образовалось 26,4 г оксида углерода (IV). Плотность вещества (н.у.) равна 1,96 г/л. Найдите молекулярную формулу.
17. Найдите молекулярную формулу газообразного углеводорода, если при сжигании 5,6 л его (н.у.) было получено 16,8 л оксида углерода (IV) и 13,5 г воды.
18. Определите молекулярную формулу гомолога этилена, если известно, что
0,56 г могут присоединить 1,6 г брома.
19. При сжигании 0,72г летучей жидкости было получено 0,05 моль углекислого газа и 1,08 г воды. Плотность паров его по воздуху равна 2,5. Выведите формулу данного вещества.
20. Химическое соединение — газ, содержащий углерода 85,7% и водорода
14,3%. Образец этого соединения массой 5,25 г занимает при (н.у.) объем 2,8 л. Определите формулу соединения.
21. При сгорании вещества массой 4,25 г образовались углекислый газ массой 13,2 г и воды массой 5,85 г. Плотность паров вещества по воздуху равна 5,862. Определите формулу вещества.
9-1. При полном сгорании органического вещества массой 13,8г получен оксид углерода (IV) , массой 26,4г и вода, массой 16,2 г. Найдите формулу вещества, если для него плотность по водороду равна 23.
9-2. При сжигании газообразного углеводорода с плотностью по водороду 21 получено 8,4л оксида углерода(IV) (н.у.) и 6,75 г воды. Определите формулу углеводорода.
9-3. При сжигании 3,9 г органического вещества, плотность паров которого по водороду 39, образовалось 13,2 г оксида углерода(IV) и 2,7 г воды. Какова структурная формула исходного соединения?
9-4.При сжигании 29 г вещества образовалось 44,8 л СО2 (н.у.) и 45 г воды. Относительная плотность вещества по воздуху равна 2. Определить молекулярную формулу вещества.
9-5. При сжигании 8,4 г органического вещества получено 26,4г углекислого газа и 10,8 г воды. Плотность паров этого вещества по воздуху равна 2,9. Определите молекулярную формулу вещества. К какому гомологическому ряду оно относится?
9-6. При сжигании 28 мл газа получено 84 мл оксида углерода(IV) и 67,5 мг воды (н.у.). Плотность газа по водороду равна 21. Определите молекулярную формулу газа.
9-7. К какому классу органических соединений должно относиться вещество, при сжигании 11 г которого образуется 11,2 л (н.у.) оксида углерода(IV) и 9 г воды, если молярная масса этого вещества равно молярной массе углекислого газа?
9-8. При сгорании 1,86 г органического вещества образовалось 3,96 г углекислого газа и 0,54 г воды. Сколько всего атомов содержит молекула этого соединения, если известно, что его молярная масса меньше 200 г/моль?
9-9. Определите молекулярную формулу газа, если известно, что при сжигании 2,24 л его образовалось 4,48 л углекислого газа (н.у.) и 1,8 г воды. Плотность газа по воздуху равна 0,8966.
9-10. Определите молекулярную формулу углеводорода, если известно, что при сгорании его объемом 0,0112 м3 (н.у.) образуется углекислый газ объемом 0,0336 м3 и пары воды массой 0,036кг.
9-11. При сжигании углеводорода массой 8,4 г образовалось 26,4 г углекислого газа. Плотность вещества при н.у. равна 1,875 г/л. Найдите его молекулярную формулу.
9-12.При сгорании 11,2 л газа получилось 33,6 л СО2 и 27 г воды. 1 л газа при н.у. весит 1,875 г. Определить молекулярную формулу газа.
9-13. Определите молекулярную формулу углеводорода, если известно, что 1,3 г его при сжигании образуют 2,24 л оксида углерода (IV) и 0,9 г паров воды. Масса 1 мл этого углеводорода при н.у. равна 0,00116 г. К какому гомологическому ряду он относится?
9-14. Органическое вещество массой 1,875 г занимает объем 1 л (н.у.). При сжигании 4,2 г этого вещества образуется 13,2 г СО2 и 5,4 г воды. Определите молекулярную формулу вещества.
9-15. При сжигании 1 моль предельного углеводорода образуется 22,4 л углекислого газа (н.у.) и 36 г воды. Найдите молекулярную формулу этого соединения и рассчитайте, какой объем воздуха потребуется для полного сгорания 1л этого газа.
9-16.Для установления формулы газообразного углеводорода 5 мл его смешали с 12 мл О2, и смесь была взорвана. После конденсации водяных паров объем газообразного остатка СО2 + О2 равнялся 7 мл, а после обработки его щелочью для поглощения СО2 осталось 2 мл газа. Найти формулу углеводорода.
9-17.При взрыве смеси 8 мл газообразного углеводорода с 36 мл О2 образовалось 16 мл СО2 и некоторое количество водяных паров. После взрыва не прореагировало 8 мл О2. Найти формулу газообразного углеводорода.
9-18. Определите простейшую формулу газа, на сжигание 1 л которого израсходовано 2 л кислорода, причем образовалось 1 л углекислого газа и 2 л водяных паров (н.у.).
9-19. Углекислый газ, образующийся при полном сгорании 0,1 моль алкана, при пропускании в избыток известковой воды дает 60 г белого осадка. Что это за алкан?
9-20. Какой газ находится в цилиндре, если известно, что он гомолог этилена и для полного сгорания 60 см3 этого газа требуется 270 см3 кислорода (н.у.)?
9-21. Для сжигания алкана объемом 20,0 л потребовался кислород объемом 160 л (н.у.). Установите, какой алкан вступил в реакцию.
9-22. Для сжигания порции алкана, содержащей 1∙1023 молекул, требуется порция кислорода, содержащая 1,6∙1024 атомов. Установите состав и возможное строение (все изомеры) алкана.
9-23.Определите молекулярную формулу вещества, при сгорании 9 г которого образовалось 17,6 г СО2, 12,6 г воды и азот. Относительная плотность этого вещества по водороду – 22,5. Определить молекулярную формулу вещества.
9-24. При сгорании 9 г предельного вторичного амина выделилось 2,24 л азота и 8,96 л углекислого газа. Определите молекулярную формулу амина.
9-25. При сжигании органического вещества массой 1,78 г в избытке кислорода получили 0,28 г азота, 1,344 л (н.у.) СО2 и 1,26 г воды. Определите молекулярную формулу вещества, зная, что в указанной навеске вещества содержится 1,204∙1022 молекул.
9-26. При сжигания 6,45 г газообразного галогеналкана образовалось 4,48 л углекислого газа и 2,24 л хлороводорода (н.у.); плотность неизвестного вещества при н.у. равна 2,879 г/л. Выведите молекулярную формулу вещества.
9-27. При сгорании газообразного органического вещества выделилось 6,72 л (н.у.) углекислого газа, 5,4 г воды, 3,65 г хлороводорода. Установите молекулярную формулу сгоревшего вещества, рассчитайте его массу и приведите одно из возможных его названий.
9-28. При сгорании бескислородного органического вещества выделилось 4,48 л (н.у.) CO2, 3,6 г H2O и 3,65 г хлороводорода. Установите молекулярную формулу сгоревшего соединения, рассчитайте его объем и массу.
9-29. При полном сгорании органического вещества выделилось 8,96 л (н.у.) углекислого газа, 3,6 г воды, 14,6 г хлороводорода. Установите молекулярную формулу и возможное название сгоревшего вещества, рассчитайте его массу.
9-30. При полном сгорании газообразного органического вещества, не содержащего кислород, выделилось 4,48 л (н.у.) углекислого газа, 1,8 л воды и 4 г фтороводорода. Установите молекулярную формулу сгоревшего соединения, рассчитайте его объем и массу.
9-31. При сгорании газообразного органического вещества, не содержащего кислорода, выделилось 13,2 г углекислого газа, 5,4 г воды и 2 г фтороводорода. Установите молекулярную формулу сгоревшего соединения, рассчитайте его объем и массу.
9-32. Какова структурная формула предельной одноосновной кислоты, если объем CO2, образующегося при сжигании некоторого ее количества, в три раза больше объема CO2, выделившегося при действии на такое же количество данной кислоты избытка водного раствора гидрокарбоната натрия?
9-33. Полученную при сжигании 1.5 г аминокислоты в кислороде смесь газов пропускают через трубку с фосфорным ангидридом, а затем через известковую воду. Далее поглощают кислород и измеряют объем оставшегося газа. Какова формула аминокислоты, если масса Р2О5 после пропускания газов увеличилась на 0,9 г, масса осадка, выпавшего в известковой воде -4 г, объем оставшегося после поглощения кислорода газа - 224 мл.
9-34. При сжигании 5.76 г вещества образовалось 2,12 г Na2CO3 и 5,824 л СО2 (н.у.) и 1,8 г воды. Определить формулу вещества.
9-35.При полном сгорании 3,76 г органического бромсодержащего вещества получилось 1.76 г СО2 и 0,72 г воды. После поглощения всего брома, содержащегося в данном количестве вещества, в бромистое серебро, получено 7,52 г осадка. Относительная плотность паров вещества по водороду равна 94. Определить молекулярную формулу вещества.
9-36.При сжигании 12.6 г вещества образовалось 3,18 г Na2 CO3, 4,14 г К2 CO3, 4,032 л СО2 и 2,16г Н2О. Определить молекулярную формулу вещества.
9-37. При сжигании 5,34 г орг. вещества в избытке кислорода образовалось 3,78 г воды и 5,376 л (н.у) газовой смеси, объём которой при пропускании через избыток раствора щелочи уменьшился до 1,344 л (н.у). Предложите структурную формулу вещества, если известно, что оно содержит С, Н,О,N. Плотность по водороду оставшейся газовой смеси равна 15,00.
9-38. В состав вещества входят C H O S. При сжигании его навески массой 0,222 г были получены 0,396 г СО2, 0,162 г Н2О, а сера переведена в сульфат бария массой 0,3495г. Относительная плотность паров вещества по водороду равна 74. Определить истинную формулу вещества
9-39. 54 г амина сожгли в избытке кислорода. Полученную газовую смесь после удаления О2 пропустили через раствор КОН с массовой долей 20%. Объём газа, не поглощенного щелочью, составил 13,44 л (н.у). Определите формулу амина.
1.23 (3) Относительная плотность паров органического соединения по водороду равна 22. При сжигании 4,4 г этого вещества образуется 13,2 г диоксида углерода и 7,2 г воды. Выведите молекулярную формулу органического соединения.
1.24 (3) Относительная плотность паров органического соединения по хлору равна 2. При сжигании 2,84 г этого вещества образуется 4,48 л оксида углерода (IV) (н. у.) и 3,96 г воды. Выведите молекулярную формулу этого соединения.
1.25 (3) В некоторых условиях масса некоторого объема воздуха равна 0,369 г, а масса такого же объема углеводорода — 0,738 г. Определите формулу углеводорода, если известно, что при его пропускании через водный раствор брома изменения цвета раствора не происходит.
1.26 (3) К 80 мл газообразного углеводорода добавили избыток кислорода (500 мл) и подожгли. После приведения паров к н. у. объем их составил 340 мл, а после пропускания через избыток раствора гидроксида натрия объем уменьшился до 100 мл. Определите молекулярную формулу углеводорода.
1.27 (3) При сжигании 400 см3 предельного углеводорода образовалось 400 см3 углекислого газа. Определите молекулярную формулу углеводорода.
1.28 (3) При сжигании хлоропроизводного предельного углеводорода образовалось 1,344 л углекислого газа (н. у.) и 1,08 г воды, а из хлора, содержащегося в этой навеске исходного вещества, было получено 17,22 г хлорида серебра. Плотность паров вещества по гелию 42,5. Определите молекулярную формулу вещества.
1.29 (3) 448 мл (н. у.) газообразного предельного нециклического углеводорода сожгли и продукты реакции пропустили через избыток известковой воды, при этом образовалось 8 г осадка. Какой углеводород был взят?
2.11 (3) 7,5 г органического соединения при нормальных условиях занимает объем 4 л. При сжигании 2,1 г этого соединения образуется 6,6 г углекислого газа и 2,7 г воды. Выведите молекулярную формулу органического соединения.
2.12 (3) Относительная плотность паров органического соединения по азоту равна 2. При сжигании 9,8 г этого соединения образуется 15,68 л углекислого газа (н. у) и 12,6 г воды. Выведите молекулярную формулу органического соединения.
3.16 Относительная плотность паров органического соединения по воздуху равна 4,83. При сжигании 17,5 г этого соединения получен углекислый газ объемом 28 л и воду массой 22,5 г. Выведите молекулярную формулу органического соединения.
4.14 (3) Относительная плотность паров органического вещества по кислороду равна 2,125. При сжигании 10,2 г этого вещества образовалось 16,8 л диоксида углерода (н. у.) и 10,8 г воды. Выведите молекулярную формулу этого вещества.
4.15 (3) Относительная плотность паров органического вещества по водороду равна 48. При сжигании 2,4 г этого вещества образовалось 3,92 л углекислого газа (н. у.) и 2,7 г воды. Выведите молекулярную формулу алкадиена.
5.17 (3) 27 г органического вещества при н.у. занимают объем 11,2 л. При сжигании 21,6 г этого вещества образуется 35,84 л углекислого газа и 21,6 г воды. Выведите молекулярную формулу органического вещества.
5.18 (3) Плотность паров органического соединения по неону равна 4,1. При сжигании 8,2 г этого вещества образуется 26,4 г оксида углерода (IV) и 9 г воды. Выведите молекулярную формулу органического вещества.
5.19 (3) Углекислый газ, полученный при сгорании 3,4 г углеводорода, пропустили через избыток раствора гидроксида кальция и получили 25 г осадка. Выведите простейшую формулу углеводорода.
5.20 (3) При сгорании навески некоторого углеводорода плотностью по воздуху 1,38 образовалось 966 мл углекислого газа и 644 мл воды. Установите формулу углеводорода.
6.18 (3) Относительная плотность паров органического вещества по кислороду равна 2,44. При сгорании 3,9 г этого вещества образуется 13,2 г углекислого газа и 2,7 г воды. Выведите молекулярную формулу органического вещества.
7.21 (3) Относительная плотность паров органического соединения по гелию равна 25,5. При сжигании 15,3 г этого вещества образовалось 20,16 л (н.у.) углекислого газа и 18,9 г воды. Выведите молекулярную формулу органического соединения.
7.22 (3) Относительная плотность паров органического соединения по воздуху равна 4. При сжигании 14,5 г этого вещества образуется 38,5 г оксида углерода (IV) и 18 г воды. Выведите молекулярную формулу органического соединения.
7.23 (3) В результате сгорания 0,828 г органического соединения образовалось 1,584 г углекислого газа и 0,972 г воды. Относительная плотность паров этого соединения по метану 2,875. Установите формулу этого соединения и вычислите объем воздуха (н.у.), необходимого для полного сгорания 13,8 г этого вещества.
7.24 (3) При полном окислении 20,4 г органического вещества было получено 15,9 г карбоната натрия, 19,8 г углекислого газа и 13,5 г воды. Выведите молекулярную формулу органического вещества.
8.11 (3) Относительная плотность паров органического вещества по водороду равна 45. При сжигании 10,6 г этого вещества образовалось 8,96 л углекислого газа (н.у.) и 9 г воды. Выведите молекулярную формулу органического вещества.
8.12 (3) Относительная плотность паров органического вещества по кислороду равна 4,25. При сжигании 47,6 г этого вещества образовалось 77 г оксида углерода (IV) и 37,8 г воды. Выведите молекулярную формулу органического вещества.
9.7 (3) Относительная плотность паров органического соединения по водороду равна 47. При сжигании 14,1 г этого вещества образуется 39,6 г углекислого газа и 8,1 г воды. Выведите молекулярную формулу этого соединения.
9.8 (3) Относительная плотность паров органического соединения по кислороду равна 3,875. При сжигании 12,4 г этого вещества образуется 15,68 л углекислого газа (н. у.) и 7,2 г воды. Выведите молекулярную формулу этого соединения.
10.18 (3) Относительная плотность паров органического соединения по азоту равна 3,071. При сжигании 8,6 г этого вещества образуется 11,2 л углекислого газа и 9 мл воды (н.у.). Выведите молекулярную формулу этого соединения.
10.19 (3) Относительная плотность паров органического соединения по сернистому газу равна 2. При сжигании 19,2 г этого вещества образуется 52,8 г углекислого газа (н. у.) и 21,6 г воды. Выведите молекулярную формулу органического соединения.
11.18 (3) Относительная плотность паров органического соединения по гелию равна 15. При сжигании 18 г этого соединения образуется 26,4 г оксида углерода (IV) и 10,8 г воды. Выведите молекулярную формулу органического соединения.
11.19 (3) При прокаливании на воздухе из 0,395 г некоторого вещества получили 0,140 г оксида кальция, из 0,948 г этого же вещества — 537,6 мл (н.у) СО2, а из 0,869 г вещества — 0,297 г Н2О. Найдите формулу соединения.
11.20 (3) При полном окислении 4,8 г органического вещества было получено 2,8 л оксида углерода (IV) (н. у.), 2,25 г воды и 2,65 г карбоната натрия. Установите формулу вещества.
12.11 (3) При полном сгорании 5,4 г некоторого органического соединения, относительная молекулярная масса которого равна 180, образовалось 4,032 л (н.у.) углекислого газа и 3,24 г воды. Определите молекулярную формулу этого соединения и предложите возможные структуры.
13.11 (3) Для сгорания 6 молей вещества потребовалось 13,5 моля кислорода и образовалось 6 молей углекислого газа, 3 моля азота и 15 молей воды. Установите молекулярную формулу вещества,
13.16 (3) Относительная плотность паров органического соединения по водороду равна 43,5. При сгорании 17,4 г этого вещества образуется 44 г углекислого газа, 2,24 л азота (н. у.) и 23,4 г воды. Выведите молекулярную формулу органического соединения.
13.17 (3) Относительная плотность паров органического соединения по этану равна 1,5. При сгорании 9 г этого вещества образуется 8,96 л углекислого газа, 12,6 г воды и 2,24 л азота и 11,7 мл воды (н.у.). Выведите молекулярную формулу органического соединения.
22. На полное сгорание 0,2 моль алкена израсходовано 26,88 л кислорода (н.у.). Установите название, молекулярную и структурную формулу вещества.
Решение: 0,2моль 26,88л
СnH2n + О2— СО2+Н2О
1моль хл
1 .v(О2) =?
.v(О2) =? ![]() х = 134,4л
х = 134,4л
2. γ (О2)-? ![]() =6моль или γ (О2)-?
=6моль или γ (О2)-? ![]() =>
=>
. γСnH2n: . γ (О2) = 0,2 : 1,2 = 1:6
отсюда на 1 моль СnH2n надо 6 моль О2.
СnH2n + ![]() О2. = nСО2 + nН2О
О2. = nСО2 + nН2О
3 . γ (О2)-. в левой части известно — 12 атомов, а в правой — в СО2 2n и в - Н2Оn, отсюда 2n+n=12; Зn=12; n=4; С4Н8; С-С-С=С; С-С=С-С; С-С=С
. γ (О2)-. в левой части известно — 12 атомов, а в правой — в СО2 2n и в - Н2Оn, отсюда 2n+n=12; Зn=12; n=4; С4Н8; С-С-С=С; С-С=С-С; С-С=С
С
Н
 3С СН3 Н3С Н
3С СН3 Н3С Н
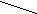


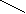 С=С С=С
С=С С=С
Н Н Н СН3
II способ: СnH2n + ![]() О2. + nСО2 + nН2О
О2. + nСО2 + nН2О
![]() =6; Зn=12; n=4; С4Н8
=6; Зn=12; n=4; С4Н8
23. При полном сжигании вещества, не содержащего (О), образуется азот и вода. D(NxHу)Н2=16. Объем необходимого на сжигание кислорода равен объему выделившегося азота. Определите общую формулу соединения и истинную формулу вещества.
NxHу + O2 → N2 + H2O; Мr (NxHу) = 16 ![]() 2=32. Так какV(О2) = V(N2) => количество (О2) = количеству(N2)
2=32. Так какV(О2) = V(N2) => количество (О2) = количеству(N2)
Так как (O) в левой части 2 атома, то перед водой в схеме уравнения запишем
коэффициент 2. Тогда количество (Н) будет в 2 раза больше количества атомов (N). Если количества атомов (N). выразим через х, то количество (Н) =2х. Составим алгебраическое выражение.
NxHу = 32. Аr (N)= 14. Аr(Н)=1 => 14х+2х=32; 16х=32; х=2); => N2H4
24. Найти простейшую формулу оксида ванадия зная, что в оксиде массой 2,73г содержится, 1,53 г метала.
Д ано: Решение:
ано: Решение:
m (vxoу)=2,73г т экв. (О)=16/2 = 8; ![]()
![]()
m (v)=1,53г т(О) =2,73- 1,53 = 1,2

Vx Oу=? тэкв(V) = ![]()
Ar(V) = 51 B(V) = ![]()
Или: т (О) =2,73 – 1,53 = 1,2; х : у = ![]()
![]()
![]() = 0,03 : 0,075 = 1 : 2,5 =2 : 5=>V2O5
= 0,03 : 0,075 = 1 : 2,5 =2 : 5=>V2O5
25. Объем СО2, выделившегося при сжигании предельного одноатомного спирта, в 8 раз превосходит объем водорода, выделившегося при действии избытка натрия на такое же количество спирта. Установите строение спирта, если известно, что при его окислении образуется кетон.
Решение:
СnH2n+2О + ![]() О2. = nСО2 + n+1Н2О (1)
О2. = nСО2 + n+1Н2О (1)
2СnH2n+1ОН + 2Na = H2 + 2 СnH2n+1ONa (2)
1 моль H2 из 2-х моль спирта 8 моль СО2 должно приходиться на то же количество спирта, следовательно 1 моль спирта при горении дает 4 моль СО2, =>
nСО2 = 4(1 уравнение). n ( Н2О) = n+1 = 5; n (O2) = 6.
СnH2n+2О + 6О2. = 4СО2 + 5Н2О, т. к. СО2 из 1 моль, следовательно в спирте 4 атома углерода. т. е. С4НI0О; Н3С-НCOH-СН2-СН3
26. Из I,16 г предельного углеводорода получили 1,85 г монохлорпроизводного. Определите молекулярную формулу предельного углеводорода.
Решение:
1.16 1.85
СnH2n+2 + С12 = СnH2n+1СI + НСI
14n+2 14n+1+З5.5
![]() 1,16(14n+ 36.5)=(14n+2)
1,16(14n+ 36.5)=(14n+2) ![]() 1,85= 16,24n+42,34 = 25,9n+3,7
1,85= 16,24n+42,34 = 25,9n+3,7
следовательно, n=4, значит С4Н10
II способ через массу приращения (.∆m)
СnH2n+1СI стал тяжелее, чем СnH2n+2 на m(С1) и меньше на m(Н).
1.16 1.85
СnH2n+2 + С12 = СnH2n+1СI + НСI
71
1 ) ∆m по задаче. =. 1,85-1,16=0,65; ∆m по уравнению 35,5(С1)-1(Н)=34.5.
) ∆m по задаче. =. 1,85-1,16=0,65; ∆m по уравнению 35,5(С1)-1(Н)=34.5.
2) mСI2-? ∆ mЗ4,5г----7IгС12
∆ m0,65г --- х гСI2 х = 1,42
3)Мг(СnH2n+2)-?
![]() x = 62; СnH2n+2 = 62; 14n+2 = 62; 14n = 60; n = 4, значит С4Н10
x = 62; СnH2n+2 = 62; 14n+2 = 62; 14n = 60; n = 4, значит С4Н10
I II Способ;
II Способ;
∆m 0,65 1,16 СnH2n+2 x =62
∆m 34,5-------x СnH2n+2
СnH2n+2 = 62; 14n+2 = 62; 14n = 60; n = 4, значит С4Н10
27. Из I,74 г предельного углеводорода получили 4,11г монобромпроизводного. Определите молекулярную формулу предельного углеводорода.
1,74 4,11
СnH2n+2 + Br2 = СnH2n+1Br + НBr
14n+2 14n+1+80
![]()
I,74 ![]() (14n+81) = (14n+2)
(14n+81) = (14n+2) ![]() 4,11
4,11
24,36n+140,94= 57,54n+8,22
132,72= 33,18n; n=4. следовательно, С4Н10
28.При гидрогалогенировании одинакового количества алкена получили 7,85 г хлорпроизводного и 12,3 г бромопроизводного. Вывести формулу а
Решение: 7.85 12.3
Количество алкена одинаково, следовательно, n(СnH2n+1СI) = n(СnH2n+1Br)
14n+36.5 14n+81
Тогда ![]() =.> n=3.
=.> n=3.
Или через массу прирощения;
1) ∆m зад. 12,3-7,85 = 4,5
2) ∆m у-я 81(HВr) – 36,5(НСI)=44,5
С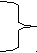 nH2n + НСI = СnH2n+1СI
nH2n + НСI = СnH2n+1СI
3) Мг-? ∆m 4,45 --- 7,85 г СnH2n+1СI
∆ m44,5------хг СnH2n+1СI х=78,5
4) n-? СnH2n+1СI = 78,5; 14n+1+35,5=78,5; n=3
5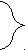 ) СnH2n + HBr = СnH2n+1Br
) СnH2n + HBr = СnH2n+1Br
Мг -? ∆m 4,45 г ------ 12,3 СnH2n+1Br х = 123
∆m44,5г----------х СnH2n+1Br
6) n —? СnH2n+1Br = 123; I4n+1+80=123; n=3, следовательно, С3Н6
29. Определите формулу одноатомного спирта ω(С) и ω(Н) = 60% и 13,3%. Если при взаимодействии с кислотой образуется вещество, относительная плотность которого по H2 = 58.
Решение:При взаимодействии спирта и кислоты образуется сложный эфир(СnH2nО2)
1)Мг (СnH2nО2) = 58 ![]() 2=116;
2=116;
2)n=? (СnH2nО2) = 116; 14n+32=116; n=6. следовательно, С6H12O2.
3) (СnH2n+2О) спирт (СxНуО,) %(O)= 100 - (60+13.3) = 26,7
Х : у : z = ![]() = 5:13,3:1,67= 2,99 : 7,96 : 1=3 : 8 : 1, следовательно С3Н8О3.
= 5:13,3:1,67= 2,99 : 7,96 : 1=3 : 8 : 1, следовательно С3Н8О3.
30. Массовая доля «О» в одноатомном предельном спирте = 26,67%. Выведите химическую формулу вещества.
Решение.
ω% =![]() ; 26,67% =
; 26,67% = ![]()
![]() 100%;
100%;
1600 = 373n +480; n = 3 =>C3H7OH;
II Способ:
![]() х = :60; СnH2n+2О = 60; 14n+18 = 60; 14n = 47; n = 3.
х = :60; СnH2n+2О = 60; 14n+18 = 60; 14n = 47; n = 3.
31.На сгорание одноатомного предельного спирта потребовалось 84л. Кислорода (н.у.). В результате реакции получилось СО2 и 60г. водяных паров. Определите молекулярную формулу исходного спирта.
Решение:
СnH2n+2О + ![]() О2 = n СО2 + (n+1)H2O
О2 = n СО2 + (n+1)H2O
γ(О2) =
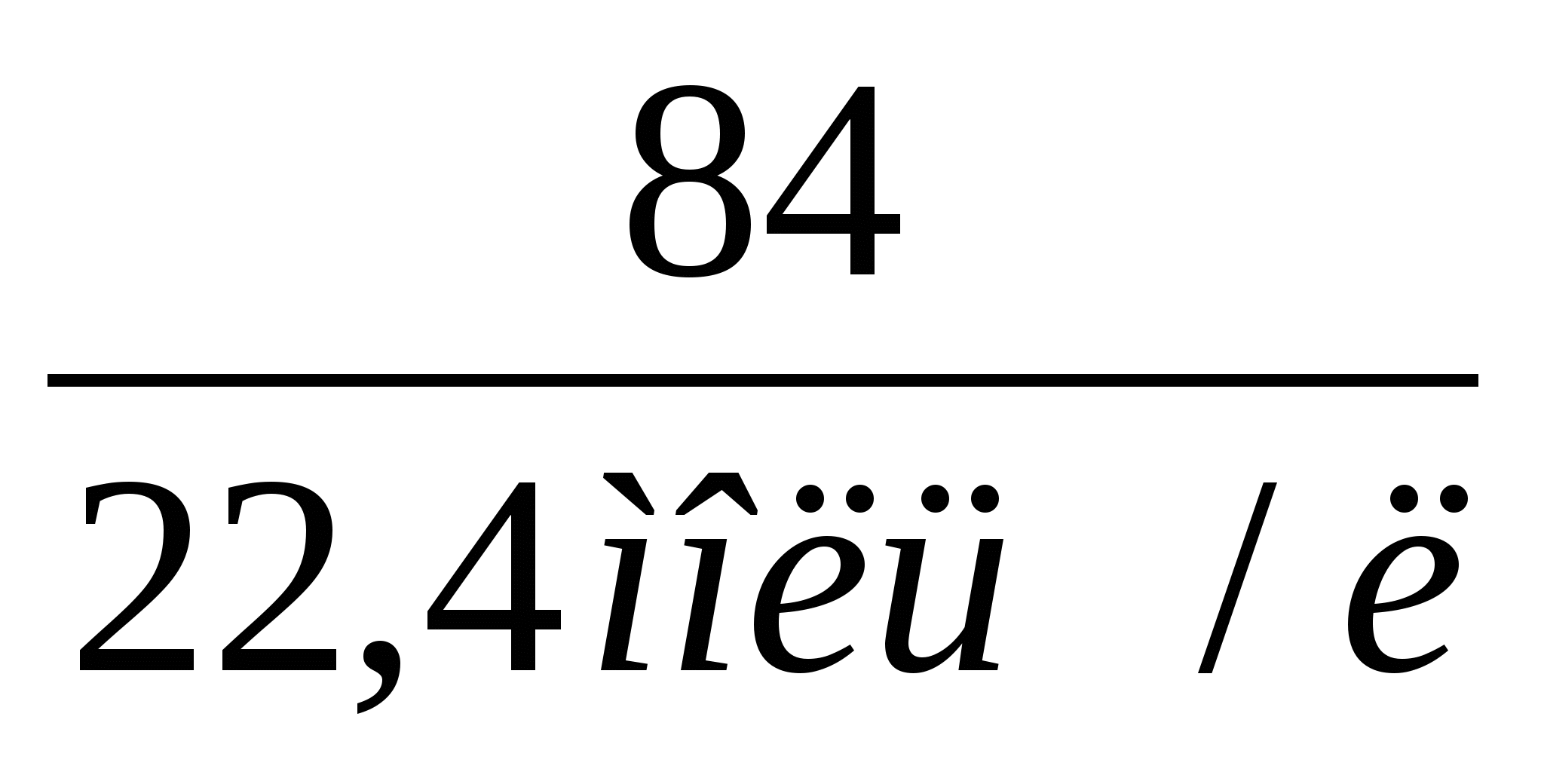 = 3,75 моль.
= 3,75 моль.γ(Н2О) =
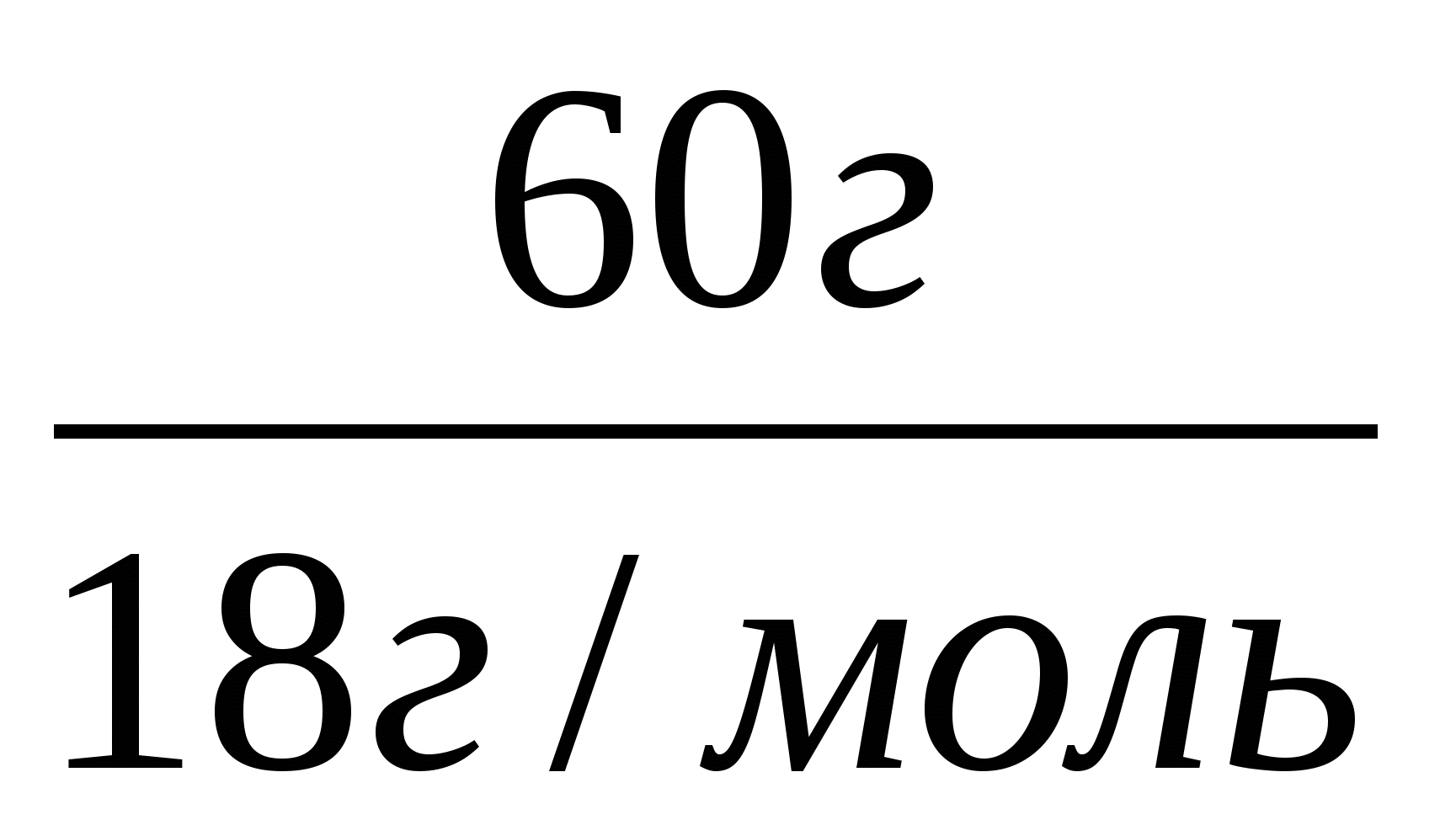 = 3,33г
= 3,33г
3)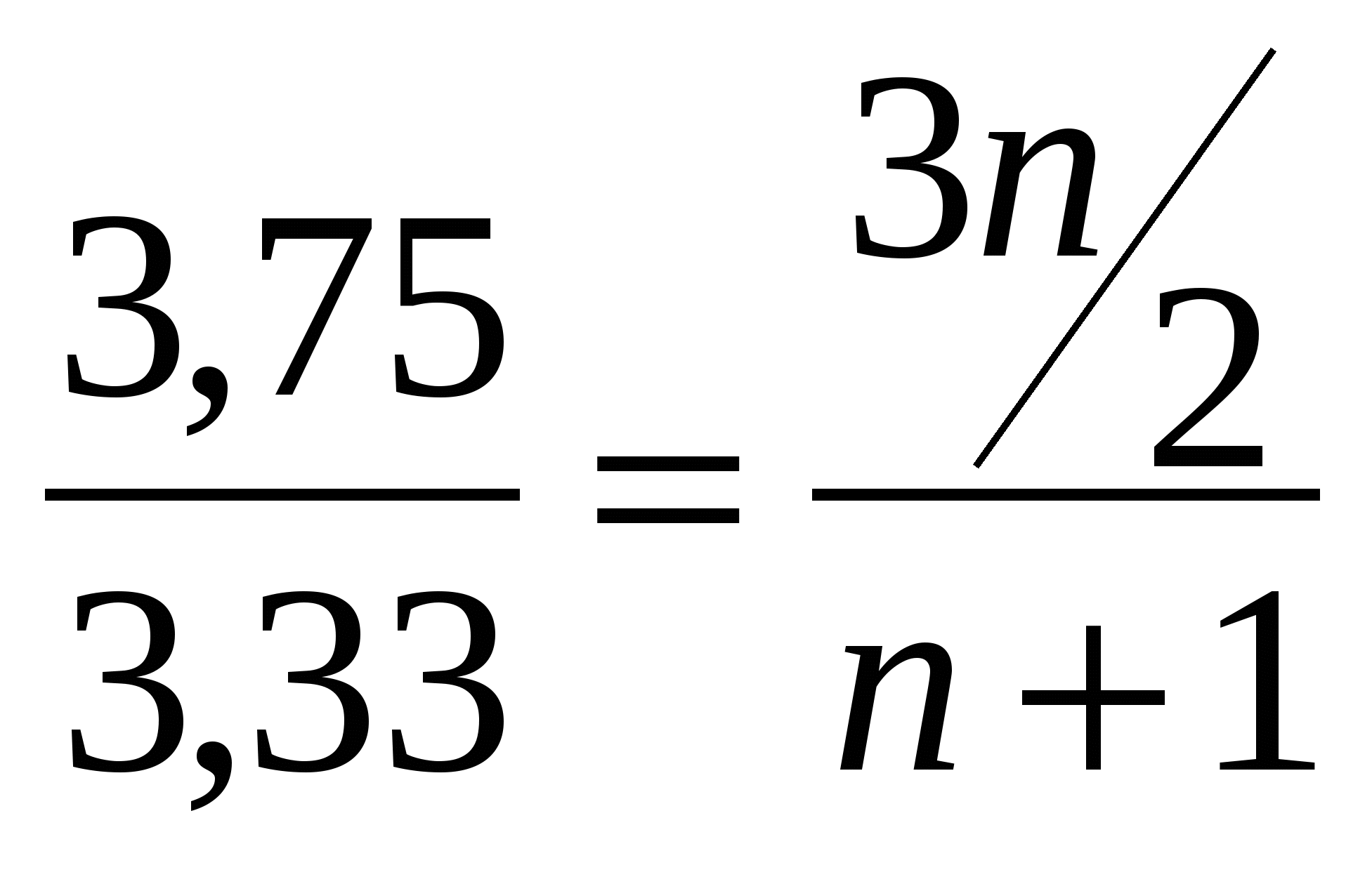 ; 3,75(n+1) = 3,33
; 3,75(n+1) = 3,33 ![]()
![]() ; 3,75n + 3,75 =
; 3,75n + 3,75 = ![]()
3,75n + 3,75 = 5n; 3,75 = 1,25n; n = 3 =>C3H7OH;
32. Определите формулу ацетиленового углеводорода, если малярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса углеводорода.
Решение:
CnH2n-2 +2HBr = CnH2nBr2
Мr(CnH2n-2)< в 4 раза Мr(CnH2n-Br2)
![]()
![]() = 4;
= 4; ![]() =4; 12n+2n +160= (12n+2n-2)
=4; 12n+2n +160= (12n+2n-2) ![]() 4 =
4 =
14n+160 = 56n -8; 42n = 168; n = 4=>C4H8
33.10л. смеси алкена с избытком водорода (н.у.) пропустили над катализатором. Объём смеси уменьшился до 7,2л.. При пропускании той же смеси через избыток бромной воды масса склянки увеличилась на 5,25г. Определите состав смеси.
СnH2n + Н2 = СnH2n+2 СnH2n + Br2 = СnH2nBr2
т.к. Н2 в избытке => весь алкен прореагировал.
Т.к. γ (СnH2n) = γ (Н2) => V (СnH2n) = V(Н2)
Объём уменьшился за счёт удаления водорода
V (СnH2n) = V (Н2) = 10 – 7,2 = 2,8л.
Т.к. бром в избытке => весь алкен прореагировал, склянка увеличилась за счёт алкена
m 1 моль =?
![]() ; х=42; СnH2n = 42; 14n=42; n=3;=> C3H6
; х=42; СnH2n = 42; 14n=42; n=3;=> C3H6
5)φ%(СnH2n) =?
φ%(СnH2n) = ![]()
![]() 100; φ(Н2) = 100-28=72%;
100; φ(Н2) = 100-28=72%;
34.Смесь 3-х мл. газообразного углеводорода и 10мл. О2 взорвали. После приведения условий к первоначальным и конденсации паров воды объём смеси газов составил 8,5 мл. После пропускания полученной смеси через избыток щёлочи объём её уменьшился до 2,5мл., оставшийся газ поддерживает горение. Определите формулу взорванного углеводорода.
3мл. 10мл.
СхHу + О2 = СО2 + Н2О; СО2 + 2NaOH = Na2CO3 + Н2О;
1)Рассчитаем объём О2 вступившего в реакцию; т. к 25мл. осталось =>
10-2,5=7,5; γ(О2) = ![]() =0,335ммоль
=0,335ммоль
2)Т.к. из 8,5мл. 2,5 осталось => V(СО2)=8,5-2,5=6мл; γ(СО2)=![]() =0,268ммоль
=0,268ммоль
3) γ (СхHу) =?
γ(СхHу) =![]() =0,134ммоль; γ (СхHу): γ(О2): γ(СО2) = 0,134:0,335:0268=1:2,5:2=2:5:4;
=0,134ммоль; γ (СхHу): γ(О2): γ(СО2) = 0,134:0,335:0268=1:2,5:2=2:5:4;
2СхHу + 5О2 = 4СО2 + 2Н2О; γ(С): γ(Н) = 4:4, но т.к. СхHу 2 моль =>С2Н2
35.При разложении 1,68 г неизвестного карбоната получилось 0,8г углекислого газа, какой это карбонат?
1,68 г 0,8г
Мех (СО3)у→ СО2 + МехОу
44г
1)γ(СО2) = γ(СО32-); γ(СО2) =![]() = 0,02моль => γ(СО32-); =0,02моль; М (СО32-) = 60
= 0,02моль => γ(СО32-); =0,02моль; М (СО32-) = 60
2)Рассчитаем массу СО32- в количестве 0,02моль ![]()
3) Рассчитаем массу М (Мех(СО3)У); ![]() х=84;
х=84;
4)m(Ме) =84- (1,2 + 48)= 24; Аr(Me) =24 =>это Mg
36 Вывести химическую формулу вещества если, ω% (Mg) =20%; ω%(О)=53,33%; , ω%(Э)=26,67%.
1)√ (Mg)=?![]() =0,83моль; 2) √(О)=
=0,83моль; 2) √(О)=![]() =3,33моль; Mg ЭО4MgхЭуОz
=3,33моль; Mg ЭО4MgхЭуОz
 100%
100%
20%
3)X:Z=0, 83:3, 33=1:4 => Mg ЭО4
4) Мr (Mg ЭО4) =? ![]() x=120
x=120
5) m (Э)=120-(24+64)=32; Аr(Э)=32 =>S; Mg SО4
37.При обработке предельного одноатомного спирта натрием получено 2,24л водорода (н.у.), а при дегидратации такой же порции спирта получено 11,2г алкена. Определите состав спирта.
2,24л
2СnH2n+1ОН + 2Na = H2 + 2 СnH2n+1ONa
11,2г
СnH2n+1ОН→ СnH2n+ Н2О
1) √( H2)=? ![]() =0,1моль; 2) √(СnH2n+1ОН): √(H2): √(СnH2n ) =2:1:2; 3)т.к. √( H2)=0,1моль =>√(СnH2n ) =0,2моль; рассчитаем массу 1 моль алкена; m=?
=0,1моль; 2) √(СnH2n+1ОН): √(H2): √(СnH2n ) =2:1:2; 3)т.к. √( H2)=0,1моль =>√(СnH2n ) =0,2моль; рассчитаем массу 1 моль алкена; m=? ![]() ; СnH2n=56; 14n=56; n=4; С4H8О;
; СnH2n=56; 14n=56; n=4; С4H8О;
И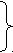 ли:
ли:
2,24л 11,2г
СnH2n+1ОН→ H2 → СnH2n х=112;
22,4л х
Это 2 моль=> m 1моль=112/ 2=56 и т.д.
38.Сложный эфир массой 30г. Подвергнут щелочному гидролизу. При этом получено 34г. Натриевой соли предельной одноосновной кислоты и 16 г. Спирта. Установите молекулярную формулу этого эфира.
30г Хг 34г. 16г
СnH2n О2 + NaОН→ СnH2n-1 О2Na + СnH2n+1ОН
14n+32 40г
По закону сохранения масс веществ масса левой части уравнения равна массе правой части. Отсюда, если от суммы масс правой части отнимем массу эфира, мы получим массу NaОН вступившего в реакцию.
m(NaОН) = (34+16) – 30 = 20
30г 20
СnH2n О2 + NaОН→ СnH2n-1 О2Na + СnH2n+1ОН
14n+32 40г
![]() ; формула эфира: С2Н4О2
; формула эфира: С2Н4О2
39.Установите молекулярную формулу предельной одноосновной карбоновой кислоты, кальциевая соль которой содержит 30,77% кальция

69,23% 30,77%
2 СnH2nО2 + Са = ( СnH2n-1О2)2Са + H2
14n-1+32 40
ω% =![]() ; 30.77% =
; 30.77% = ![]()
![]() 100%;
100%;
(28n +102) ![]() 30,77 =4000; 861,56n =861.46; n =1; Формула кислоты СН2О2- мурвьинная кислота
30,77 =4000; 861,56n =861.46; n =1; Формула кислоты СН2О2- мурвьинная кислота
Или можно по другому:
![]()
Или можно по другому: Сначала рассчитаем молекулярную массу.
![]()
( СnH2n-1О2)2Са = 130; 28n +102 =130; n =1; Формула кислоты СН2О2- муравьиная кислота
40. Установите формулу предельной одноосновной кислоты натриевая соль которой содержит 33,82% натрия.

66,18% 33,82%
2 СnH2nО2 + 2Na = 2СnH2n-1О2Nа + H2
14n-1+32 23
ω% =![]() ; 33,82% =
; 33,82% = ![]()
![]() 100%; 33,82% =
100%; 33,82% = ![]()
23=4,7348n + 18,2628; 4,7372=4,7348n; n =1; Формула кислоты СН2О2- муравьиная кислота
Или:
33,82% = ![]() 0,3382Х=23; Х=68; СnH2n-1О2Nа=68; 14n+54=68; 14n=14; n=1.
0,3382Х=23; Х=68; СnH2n-1О2Nа=68; 14n+54=68; 14n=14; n=1.
41.При сгорании 1г одноатомного спирта выделился углекислый газ объёмом 1,12л.. Установите молекулярную формулу этого спирта
1г 1,12л
СnH2n+2О + ![]() О2 = nСО2 + (n+1)H2O
О2 = nСО2 + (n+1)H2O
14+2+16 n22.4л
![]() ; Формула спирта: С3Н8О или С3Н7ОН
; Формула спирта: С3Н8О или С3Н7ОН
42.При взаимодействии 23г. предельного одноатомного спирта с концентрированной серной кислотой образуется газ. При взаимодействии этого газа с 11,2л водорода(н.у.) образуется алкан. Установите молекулярную формулу алкана.
23г
СnH2n+1ОН → кат. СnH2n + Н2О
11,2л
СnH2n + H2 → кат. CnH2n+2; νспирта :νалкена = 1:1, νН2 : ν алкена =1 : 1;
22,4л
Отсюда рассчитав количество Н2 мы будем знать количества всех веществ в реакции.
ν(Н2 ) = V/Vm; ν(Н2 ) = 11,2л / 22,4л/моль = 0,5 моль. Отсюда следует, что спирта в реакцию вступило тоже 0,5моль.
Рассчитаем молярную массу спирта.
Mr(СnH2n+1ОН) = m/ν; Mr(СnH2n+1ОН) = 23г/0,5моль = 46г/моль;
СnH2n+1ОН =46; 14n+18 =46; 14n =28; n = 2; Формула алкана: С2Н6
43. Соединение содержит 62,8% S и 37,2% F. Масса 118 мл данного соединения при 70 и 98,64 КПа равна 0,51 г. Вывести формулу соединения.
Дано:
w (S) = 62,8 %
w (F) = 37,2 %
m (CхHу) = 0,51 г
V (CхHу) = 118 мл.
Т = 70
Р = 98,64 кПа
1)Определяем простейшую формулу соединения:
n(S) : n(F) = 62,80/32 : 37,2/19 = 1,96 : 1,96 = 1 : 1
Простейшая формула S F
2)Находим молярную массу соединения:
M![]() = (0, 51 · 8,31 · 280)/(98,64 ·103·118 ·10-6) = =101,95 г/моль.
= (0, 51 · 8,31 · 280)/(98,64 ·103·118 ·10-6) = =101,95 г/моль.
3)М (S F) = 51 101,95: 51 = 2
Следовательно, формула соединения S2 F2
Ответ: S2F2
Вывести формулу соединения
SхFу - ?
44. Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода.
1)СnН2n-2 + 2НВr → СnН2nВr2 ;
2) рассчитана молярная масса углеводорода и продукта реакции:
М(Сn Н2n-2) = 14n – 2; М(Сn Н2nВr2) = 14n + 160;
3) установлена молекулярная формула углеводорода:
(14n + 160)/(14n – 2) = 4, n = 4;
Формула: С4Н6.
45. При сжигании 3 л газообразного углеводорода получено 6 л углекислого газа и некоторое количество воды. Определите молекулярную формулу углеводорода, если известно, что для полного сжигания потребовалось 10,5 л кислорода.
СхНу + О2 = СО2 + Н2О
ν(СхНу) :ν(О2) : ν(СО2) =![]() = 0,134:0,469:0,268+1:3,5:2/
= 0,134:0,469:0,268+1:3,5:2/![]() 2=2:7:4; тогда
2=2:7:4; тогда
2СхНу + 7О2 = 4СО2 + Н2О;
ν(СО2)= ν(С) тогда ν(С)=4; 4 атома приходится на 2 моль СхНу, тогда в 1 моль 2 атома углерода.
2СхНу + 7О2 = 4СО2 + 6Н2О;
ν(Н) в 6Н2О =12 атомов, следовательно в 2-х моль СхНу ν(Н) =12 атомов, а в 1 моль 6 атомов. Отсюда формула С2Н6-этан.
ν(О2) 7 моль, т.е. 14 атомов, в(СО2) кислорода 8 атомов, тогда в Н2О ν (О)= 14-8=6
46. Определите молекулярную формулу алкана, если известно, что для его сжигания потребовалось 10 л кислорода и при этом образовалось 6 л углекислого газа.
СnH2n+2 +![]() О2= nСО2 + n+1Н2О
О2= nСО2 + n+1Н2О
ν(О2) =![]() : ν(СО2) =
: ν(СО2) =![]()
![]()
Или: ![]() .
.
Ответ:С3H6
Определение формулы вещества по известной общей формуле и массовой доле одного из элементов.
47. Установите молекулярную формулу предельного трёхатомного спирта, массовая доля водорода в котором равна 10%.
Дано:
CnH2n+2 O3
W(H) =10%=0,10
Решение
![]()
Формула C5H12 O3
n=?
48. Монобромпроизводное алкана содержит 35% углерода по массе. Определите молекулярную формулу этого соединения.
Дано:
CnH2n+1Br
W(C) =35%=0,35
Решение
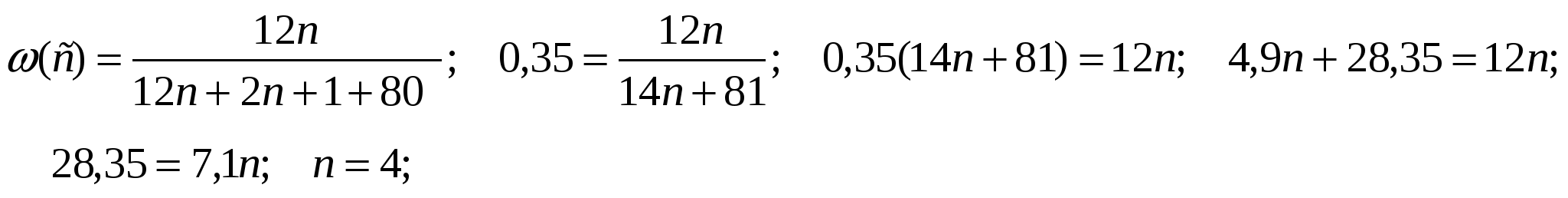 Формула C4H9Br
Формула C4H9Br
n=?
49. Монохлоралкан содержит 70,3% хлора по массе. Установите молекулярную формулу этого соединения.
50.Один из монобромалканов содержит 65,04% брома. Установите молекулярную формулу этого соединения.
51. Установите молекулярную формулу предельного двухатомного спирта, массовая доля водорода в котором равна 10,53%.
Дано:
CnH2n+2 O2
W(H) =10,53%=0,1053
Решение
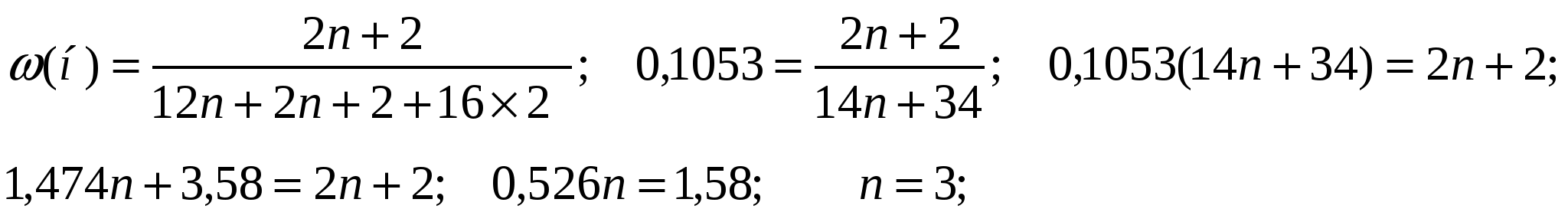 Формула C3H8 O2
Формула C3H8 O2
n=?
52. Установите молекулярную формулу предельного двухатомного спирта, массовая доля водорода в котором равна 11,11%.
53. Установите молекулярную формулу предельного двухатомного спирта, массовая доля углерода в котором равна 47,37%.
Дано:
CnH2n+2 O2
W(С) =47,37%=0,4737
Решение
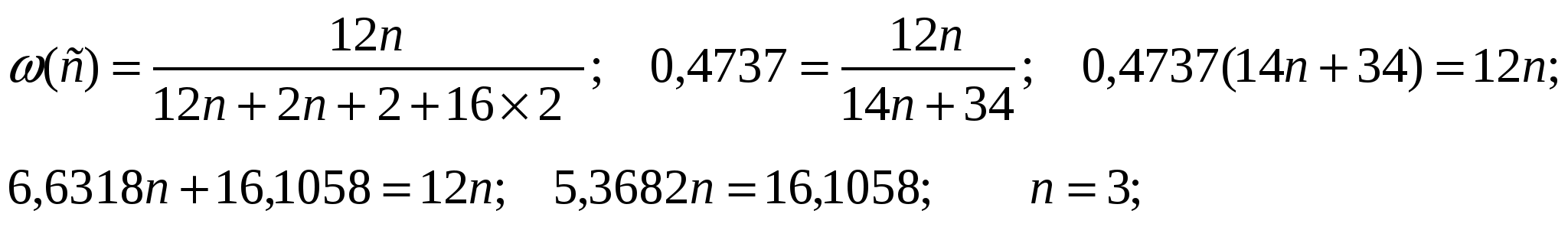 Формула C3H8 O2
Формула C3H8 O2
n=?
54. Установите молекулярную формулу предельного трёхатомного спирта, массовая доля водорода в котором равна 9,43%.
55. Установите молекулярную формулу предельного трёхатомного спирта, массовая доля кислорода в котором равна 45,28%.
Дано:
CnH2n+2 O3
W(О) =45,28%=0,4528
Решение
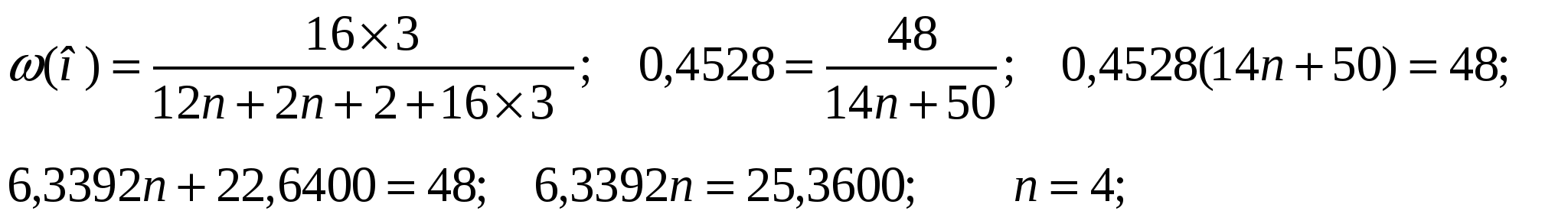
Формула C4H10 O3
n=?
56. Массовая доля кислорода в одноосновной карбоновой кислоте равна 43,24%. Установите молекулярную формулу кислоты.
Дано:
CnH2n O2
W(О) =43,24%=0,4324
Решение
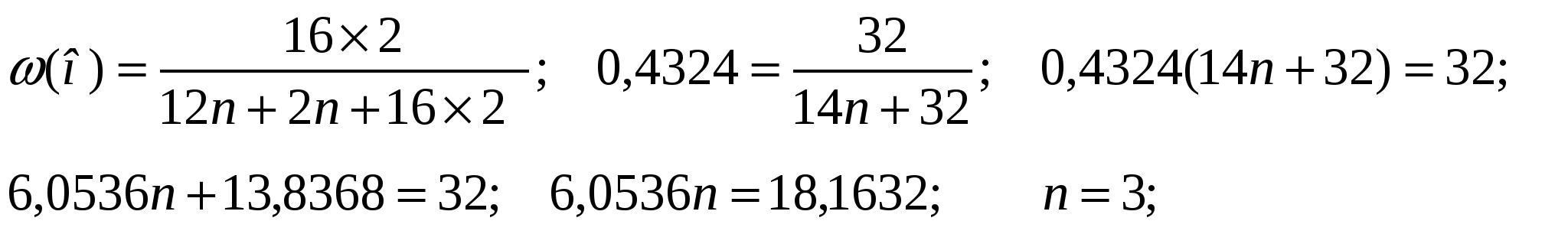
Формула C3H6 O2
n=?
57. Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу кислоты.
Определение формулы вещества по его реакционной способности.
58. При нагревании 120г предельного одноатомного спирта в присутствии концентрированной серной кислоты было получено 84г алкена. Установите формулу исходного спирта.
-
120г
84г
CnH2n+2 O
→
CnH2n
+ H2О
14n+2+16
12n+2n
![]() 120×14n=84(14n+18); 1680n=1176n+1512; 504n=1512; n=3;
120×14n=84(14n+18); 1680n=1176n+1512; 504n=1512; n=3;
Формула C3H8 O, или C3H7 OН
59. При взаимодействии одного и того же количества алкена с различными галогеноводородами образуется соответственно 7,85г хлорпроизводного или 12,3г бромпроизводного. Определите молекулярную формулу алкена, запишите его название и структурную формулу.
60. Ацетиленовый углеводород может максимально присоединить 80г брома с образованием продукта реакции массой 97г. Установите молекулярную формулу этого углеводорода.
80
97
CnH2n-2
+2Br2
→
CnH2nBr4
320
14n+320
![]() ; 80(14n+320)=97×320; 1120n + 25600 = 31040; 1120n =5440; n = 5;
; 80(14n+320)=97×320; 1120n + 25600 = 31040; 1120n =5440; n = 5;
Формула вещества: C5H8
61. В результате реакции предельного одноатомного спирта с хлороводородом массой 18,25 получили органический продукт массой 46,25г и воду. Определите молекулярную формулу исходного спирта.
62. На нейтрализацию 18,5г одноосновной карбоновой кислоты потребовался раствор, содержащий 10г гидроксида натрия. Определите молекулярную формулу исходной кислоты.
63. На нейтрализацию 25,5г одноосновной карбоновой кислоты потребовался раствор, содержащий 10г гидроксида натрия. Определите молекулярную формулу исходной кислоты.
64. Предельный одноатомный спирт обработали металлическим натрием. В результате реакции получили вещество массой 20,5г и выделился газ объёмом 2,8 л (н.у.). Определите молекулярную формулу исходного спирта.
65. При взаимодействии 30г предельного одноатомного спирта с металлическим натрием выделилось 5,6л (н.у.) газа. Определите молекулярную формулу исходного спирта.
66. При взаимодействии 23г предельного одноатомного спирта с металлическим натрием выделилось 5,6л (н.у.) газа. Определите молекулярную формулу исходного спирта.
67. При взаимодействии 22г предельной одноатомной кислоты с избытком раствора гидрокарбоната натрия выделилось 5,6л(н.у.) газа. Определите молекулярную формулу исходной кислоты.
68. Установите молекулярную формулу предельного трёхатомного спирта, массовая доля углерода в котором равна массовой доле кислорода
СnH(2n-1)(OH)3
m кислорода=16×3=48,следовательно углерода=48/12=4
C4H7(OH)3

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ