Урок по теме: "Химическая связь. Строение вещества. Кристаллические решетки"

 Дата ____________ Класс _____________
Дата ____________ Класс _____________
Тема: Химическая связь. Строение вещества. Кристаллические решетки.
Цели урока: закрепить и повторить такие понятия как «атомная орбиталь», «s-орбиталь», «p-орбиталь», «электронное строение атома», «химическая связь», «кристаллические решетки».
Ход урока
1. Организационный момент урока. Проверка домашнего задания.
2. Решение задач на закрепление.
Задание 1. (тест)
1. Чему равен заряд ядра атома натрия?
1) 0; 2) +11; 3) +1; 4) +23.
2. Сколько электронов в атоме азота?
1) 0; 2) 1; 3) 7; 4) 14.
3. Сколько нейтронов в атоме углерода C?
1) 0; 2) 12; 3) 6; 4) 7.
4. Укажите атом, в котором больше всего электронов:
1) H; 2) Al; 3) Ar; 4) K.
5. Сколько электронов содержится в молекуле CO2?
1) 6; 2) 12; 3) 8; 4) 22.
6. На внешнем энергоуровне элементов главных подгрупп число электронов:
1) равно 2;
2) равно номеру периода;
3) равно номеру группы;
4) равно 1.
7. Элементу 2-го периода до завершения внешнего уровня не хватает 3 электронов. Это элемент-…
1) бор; 2) углерод; 3) азот; 4) фосфор.
8. Элемент проявляет в соединениях максимальную степень окисления +7. Какую конфигурацию валентных электронов может иметь этот элемент в основном состоянии?
1) 3d7; 2) 2s22p5; 3) 3s23p5; 4) 3s24d5.
9. Формула высшего оксида некоторого элемента – ЭО3. Какую конфигурацию валентных электронов может иметь этот элемент в основном состоянии?
1) 4d6; 2) 2s22p4; 3) 3s23p4; 4) 3s13d5.
10. Строение внешнего и предвнешнего электронных слоёв атома меди
1) 3s23p63d94s2;
2) 3s23p63d104s0;
3) 3s23p64s13d10;
4) 3s23p63d11.
11. Относительная атомная масса хлора
1) 36; 2) 35; 3) 35,5; 4) 35,4
12. Менее яркие чем у кальция металлические свойства выражены у
1) калия; 2) радия; 3) франция; 4) алюминия
13. В ряду Al - Si - Cl увеличиваются
1) Металлические свойства,
2) Неметаллические свойства,
3) Радиус атома,
4) Способность отдавать электроны
Задание 2.
Используя таблицу, изучите закономерности изменения свойств элементов в периоде.
Таблица
группы
I
II
III
IV
V
VI
VII
VIII
Строение
атома
Li+3)2)1
Be+4)2)2
B+5)2)3
C+6)2)4
N+7)2)5
O+8)2)6
F+9)2)7
Ne+10)2)8
Высший
оксид
Li2O
BeO
B2O3
CO2
N2O5
-
-
-
Гидроксид
LiOH
осн
Be(OH)2
амф
H3BO3
кисл
H2CO3
кисл
HNO3
кисл
Ответьте на вопросы:
1. Что происходит в периоде с ростом № химического элемента:
- с зарядом ядра,
- числом электронов на внешнем энергоуровне,
- радиусом атома;
- притяжением электронов последнего уровня к ядру,
- способностью отдавать (металличность) и принимать (неметалличность) валентные электроны?
2. Как с ростом заряда ядра атома в периоде изменяются металлические, неметаллические, основные и кислотные свойства?
Задание 3.
Самостоятельно создайте аналогичную таблицу для элементов I группы «А»
Ответьте на вопросы:
1. Что происходит в группе с ростом № химического элемента:
- с зарядом ядра,
- числом электронов на внешнем энергоуровне,
- радиусом атома;
- притяжением электронов последнего уровня к ядру,
- способностью отдавать (металличность) и принимать (неметалличность) валентные электроны?
2. Как с ростом заряда ядра атома в группе изменяются металлические, неметаллические, основные и кислотные свойства?
3. Домашнее задание
Решить задачу
Дано.
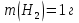
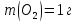
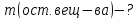

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ