Конспект урока по Химии "Соли" 8 класс
Соли
Соли – сложные вещества, состоящие из атомов металла и кислотного остатка, продукт полного.
Это определение характерно для средних солей
Соли – это сложные вещества, которые являются продуктом замещения водорода в молекулах кислот атомами металла или продуктами замещения гидроксидных групп в молекулах оснований на кислотный остаток.
1. Классификация солей.
Вид
Средние соли
Кислые соли
Основные соли
Двойные соли
Смешанные соли
Комплексные соли
Формула
NaCl
NaHS
Mg(OH)Cl
NaKSO4
CaCl(OCl)
K3[Fe(CN)6]
номенклатура
Хлорид натрия
Гидрохлорид натрия
гидроксохлорид магния
Сульфат калия натрия
Хлорид-гипохлорит кальция
гексацианоферрат (III) калия
Основные соли – сложные вещества, состоящие из атомов металла, гидроксогруппы и кислотного остатка, образуются в результате не полной реакции нейтрализации. Могут быть образованы только многокислотными основаниями Например:
![]()

 О-Н Cl
О-Н Cl
M g + H – Cl = Mg
g + H – Cl = Mg
 O-H O-H
O-H O-H
Кислые соли – сложные вещества, состоящие из атомов металла, водорода и кислотного остатка, образуются в результате не полной реакции нейтрализации. Могут быть образованы только многоосновными кислотами. Например:
![]()

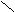
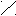
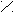
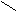

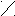 H – O O Na – O O
H – O O Na – O O
N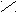


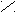
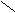
 a - O – H + S = S + H2O
a - O – H + S = S + H2O
H – O O H – O O
Двойные соли – сложные вещества, состоящие из атомов двух металлов и одного кислотного остатка. Например:
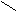

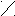 Na – O O
Na – O O
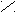
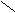
 S
S
К – O O
Смешанные соли – сложные вещества, состоящие из атомов металла и двух кислотных остатков
 Cl
Cl
 Сa
Сa
O – Cl
Комплексные соли – сложные вещества, имеющие в своем составе сложную комплексную группу.
2. Номенклатура
Средние соли:
название
кислотного
остатка
+
русское название металла (в род. пад.)
+
валентность
металла
Кислые соли:
Число «Н»
+
гидро
+
название кислотного
остатка
+
русское название металла (в род.пад.)
+
валентность
металла
Основные соли:
Число «ОН»
+
гидроксо
+
название кислотного остатка
+
русское название металла (в род.пад.)
+
валентность
металла
Двойные соли:
название кислотного остатка
+
русские названия металлов (в род.пад.)
+
валентность металлов
Смешанные соли:
название кислотных остатков (по усложнению)
+
русское название металла
+
валентность металла
Физические свойства солей.
Большинство солей – твердые вещества белого цвета, некоторые соли имеют окраску. По растворимости соли делятся на растворимые, малорастворимые и нерастворимые.
Химические свойства солей
Растворяются в воде (см. таблицу растворимости).
Соли взаимодействуют с металлами, если: а) соли растворимые; б) металл стоит левее соли; в) металл не щелочной и не щелочноземельный
![]()
Растворы солей взаимодействуют со щелочами, если образуется осадок
![]()
Растворы солей взаимодействуют с кислотами, если образуется газ или осадок
![]()
Растворы солей взаимодействуют между собой, если образуется осадок
![]()
Некоторые соли разлагаются при нагревании (нитраты, карбонаты)
![]()
Основные соли взаимодействуют с кислотами, а кислые с основаниями.
![]()
Получение солей
Неметалл
Кислотный оксид
Кислота
Соль
Металл
Соль (1)
-
Соль + Н2 (4)
Соль + металл (8)
Основной оксид
-
Соль (2)
Соль + вода (5)
-
Основание
-
Соль + вода (3)
Соль + вода (6)
Соль+основание (9)
Соль
-
-
Соль+кислота (7)
Соль+соль (10)
11) Разложение некоторых солей: NaNO3 → NaNO2 + O2↑

Нравится материал? Поддержи автора!
Ещё документы из категории химия:
Чтобы скачать документ, порекомендуйте, пожалуйста, его своим друзьям в любой соц. сети.
После чего кнопка «СКАЧАТЬ» станет доступной!
Кнопочки находятся чуть ниже. Спасибо!
Кнопки:
Скачать документ